1 . 尿素是一种适用于各种土壤和植物的有机态氮肥,是首个由无机物人工合成的有机物。以 等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。
等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。
(1)1828年,德国化学家维勒使用无机物质氰酸银(AgCNO)与 在一定条件下反应制得
在一定条件下反应制得 。
。
①该反应的化学方程式是___________ 。
② 晶体中含有的化学键有
晶体中含有的化学键有___________ (填序号)。
A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(2) 和
和 合成尿素
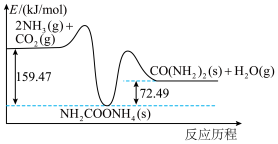
合成尿素 的能量变化如图所示,写出该反应的热化学方程式:
的能量变化如图所示,写出该反应的热化学方程式:___________ 。
(3)在恒容密闭容器中发生反应: ,下列能说明该反应达到平衡状态的是___________(填序号)。
,下列能说明该反应达到平衡状态的是___________(填序号)。
(4)在恒容密闭容器中发生反应: ,测得
,测得 的平衡转化率与起始投料比[
的平衡转化率与起始投料比[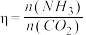 ,
, 分别为1∶1、2∶1、3∶1]和温度关系如图所示。
分别为1∶1、2∶1、3∶1]和温度关系如图所示。
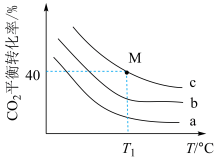
①曲线a代表的投料比为___________ ;
②若 ℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内,
℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内, 分压的平均变化率为
分压的平均变化率为___________  ,M点对应条件下的分压平衡常数为
,M点对应条件下的分压平衡常数为___________  (列出计算式即可)。
(列出计算式即可)。
 等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。
等为原料合成尿素能回收利用二氧化碳,实现碳的固定。按要求回答下列问题。(1)1828年,德国化学家维勒使用无机物质氰酸银(AgCNO)与
 在一定条件下反应制得
在一定条件下反应制得 。
。①该反应的化学方程式是
②
 晶体中含有的化学键有
晶体中含有的化学键有A.离子键 B.共价键 C.金属键 D.配位键 E.氢键
(2)
 和
和 合成尿素
合成尿素 的能量变化如图所示,写出该反应的热化学方程式:
的能量变化如图所示,写出该反应的热化学方程式:
(3)在恒容密闭容器中发生反应:
 ,下列能说明该反应达到平衡状态的是___________(填序号)。
,下列能说明该反应达到平衡状态的是___________(填序号)。A.单位时间内每消耗44g ,同时生成18g ,同时生成18g |
| B.容器中混合气体平均摩尔质量不变 |
C.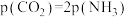 |
D. 的分压保持不变 的分压保持不变 |
(4)在恒容密闭容器中发生反应:
 ,测得
,测得 的平衡转化率与起始投料比[
的平衡转化率与起始投料比[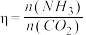 ,
, 分别为1∶1、2∶1、3∶1]和温度关系如图所示。
分别为1∶1、2∶1、3∶1]和温度关系如图所示。
①曲线a代表的投料比为
②若
 ℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内,
℃下,从反应开始至达到M点历时5min,测得M点对应的总压强为140kPa,则0~5min内, 分压的平均变化率为
分压的平均变化率为 ,M点对应条件下的分压平衡常数为
,M点对应条件下的分压平衡常数为 (列出计算式即可)。
(列出计算式即可)。
您最近一年使用:0次
名校
解题方法
2 . 由下列实验操作及现象推出的相应结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 向两份蛋白质溶液中分别滴加饱和氯化钠溶液和饱和硫酸铜溶液 | 均有固体析出 | 蛋白质均发生变性 |
B | 取1mL 20%的蔗糖溶液,加入3~5滴稀硫酸,水浴加热5min分钟后取少量溶液于一洁净的试管中,加入新制Cu(OH)2溶液,加热 | 无砖红色沉淀产生 | 蔗糖没有发生水解 |
C | 用c(Fe3+)相同的Fe2(SO4)3和FeCl3溶液,分别清洗做完银镜反应的试管 | 用FeCl3溶液清洗较干净 | Fe3++Ag Ag++Fe2+是可逆反应,且AgCl更难溶于水 Ag++Fe2+是可逆反应,且AgCl更难溶于水 |
D | 对于二氧化氮和四氧化二氮的平衡体系,缩小容器体积 | 混合气体颜色逐渐加深 | 符合勒夏特列原理 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-01-17更新
|
610次组卷
|
4卷引用:贵州省贵阳市五校2021-2022学年高三年级上学期联合考试(三)理科综合化学试题
2014·湖北黄冈·一模
3 . 工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5流程:

(1)步骤①所得废渣的成分是____________ (写化学式),操作I的名称__________ ;
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是_____________________________ ;
③中X试剂为(写化学式)______________________________________ ;
(3)④的离子方程式为___________________________________________ ;
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间关系如下表:
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为____________ ;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< _____________ ;(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有__________ 和_______________ 。

(1)步骤①所得废渣的成分是
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):R2(SO4)n (水层)+ 2nHA(有机层)
 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层) ②中萃取时必须加入适量碱,其原因是
③中X试剂为(写化学式)
(3)④的离子方程式为
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为
(5)该工艺流程中,可以循环利用的物质有
您最近一年使用:0次
2018-09-19更新
|
475次组卷
|
7卷引用:贵州省长顺县民族高级中学2018届高三下学期第一次月考理科综合化学试题
贵州省长顺县民族高级中学2018届高三下学期第一次月考理科综合化学试题(已下线)2013-2014湖北省黄冈中学高三5月模拟考试理综化学试卷(已下线)2014届湖北省黄冈中学高三5月模拟考试理综化学试卷2015届湖南省长沙市长郡中学高三第二次联考理综化学试卷2020届高三化学大二轮增分强化练——化学工艺流程题(已下线)专题讲座(八) 无机化工流程题的解题策略(精讲)-2022年一轮复习讲练测(已下线)专题讲座(八) 无机化工流程题的解题策略(讲)-2023年高考化学一轮复习讲练测(全国通用)



