名校
1 . 相同温度和压强下,研究Cl2在不同溶液中的溶解度(用溶解Cl2的物质的量浓度表示)随溶液浓度的变化。在NaCl溶液和盐酸中Cl2的溶解度以及各种含氯微粒的浓度变化如图。
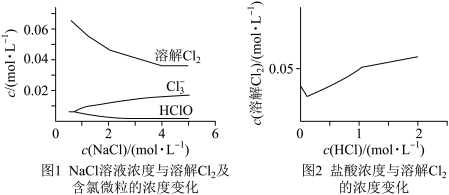
下列说法正确的是

下列说法正确的是
| A.由图1可知,Cl-的存在对Cl2的溶解只起到抑制作用 |
B.随NaCl溶液浓度增大,Cl2+H2O H++C1-+HC1O平衡正移,Cl2溶解度减小 H++C1-+HC1O平衡正移,Cl2溶解度减小 |
C.随盐酸浓度增加,Cl2与H2O的反应被抑制,生成 为主要反应从而促进Cl2溶解 为主要反应从而促进Cl2溶解 |
| D.由图2变化趋势可推测氯气在稀硫酸中溶解度大于在水中的溶解度 |
您最近一年使用:0次
2022-09-06更新
|
356次组卷
|
2卷引用:浙江省宁波市2021-2022学年上学期普通高二化学竞赛试题
2 . 已知[Co(H2O)6]2+呈粉红色,[CoCl4]2-呈蓝色,[ZnCl4]2-为无色。现将CoCl2溶于水,加入浓盐酸后,溶液由粉红色变为蓝色,存在平衡:[Co(H2O)6]2++4Cl-⇌[CoCl4]2-+6H2O ΔH。用该溶液做实验,溶液的颜色变化如图:

| A.等物质的量的[Co(H2O)6]2+和[CoCl4]2-中σ键数之比为3:2 |
| B.由实验①可推知∆H>0 |
| C.实验②是由于c(H2O)增大,导致平衡逆向移动 |
| D.由实验③可知配离子的稳定性: [ZnCl4]2->[CoCl4]2- |
您最近一年使用:0次
3 . 下列说法正确的是
| A.铜的金属活泼性比铁的弱,可在海轮外壳上镶入若干铜块以减缓其腐蚀 |
| B.若反应过程中断开化学键放出的能量大于形成化学键所吸收的能量,则反应放热 |
C.一定温度下,增大反应2BaO2(s) 2BaO(s)+O2(g)容器的体积,平衡不移动 2BaO(s)+O2(g)容器的体积,平衡不移动 |
D.反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH>0能自发进行,可知该反应ΔS>0 CO(g)+H2O(g) ΔH>0能自发进行,可知该反应ΔS>0 |
您最近一年使用:0次



