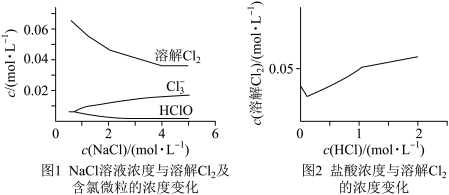
相同温度和压强下,研究Cl2在不同溶液中的溶解度(用溶解Cl2的物质的量浓度表示)随溶液浓度的变化。在NaCl溶液和盐酸中Cl2的溶解度以及各种含氯微粒的浓度变化如图。
下列说法正确的是

下列说法正确的是
| A.由图1可知,Cl-的存在对Cl2的溶解只起到抑制作用 |
B.随NaCl溶液浓度增大,Cl2+H2O H++C1-+HC1O平衡正移,Cl2溶解度减小 H++C1-+HC1O平衡正移,Cl2溶解度减小 |
C.随盐酸浓度增加,Cl2与H2O的反应被抑制,生成 为主要反应从而促进Cl2溶解 为主要反应从而促进Cl2溶解 |
| D.由图2变化趋势可推测氯气在稀硫酸中溶解度大于在水中的溶解度 |
更新时间:2022/09/06 16:59:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列有关实验操作、现象、解释或结论都正确的是
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 充分吸收了Na2SiO3 饱和溶液的小木条,沥干后放在酒精灯外焰加热 | 小木条不燃烧 | Na2SiO3 可作防火剂 |
| B | 将H2 在充满Cl2 的集气瓶中燃烧 | 集气瓶口上方有白烟生成 | H2、Cl2 化合生成HCl |
| C | 将SO2 通入酸性高锰酸钾溶液中 | 溶液褪色 | SO2 具有漂白性 |
| D | 用分别蘸有浓盐酸和浓氨水的玻璃棒相互靠近 | 冒白烟 | NH3 具有还原性 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
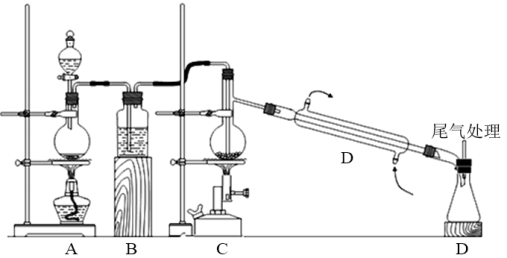
【推荐2】四氯化钛是无色液体,沸点为136℃,极易水解。在650-850℃高温下,将Cl2通入TiO2和炭粉的混合物可得到TiCl4和一种有毒气体。下图是实验室制备TiCl4的部分装置,下列说法正确的是

| A.装置A同样适合实验室制备氨气 |
| B.装置B中试剂是饱和食盐水,其作用是除HCl气体 |
C.装置C处发生的反应的化学方程式为2Cl2+C+TiO2 TiCl4+CO2 TiCl4+CO2 |
| D.装置D处的直形冷凝管可更换为球形冷凝管 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
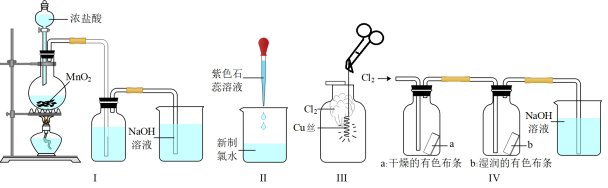
【推荐3】某同学用以下装置制备并检验 的性质。下列说法正确的是
的性质。下列说法正确的是
 的性质。下列说法正确的是
的性质。下列说法正确的是
A.图Ⅰ:若 过量,则浓盐酸可全部消耗完 过量,则浓盐酸可全部消耗完 |
| B.图Ⅱ:只证明新制氯水具有酸性 |
| C.图Ⅲ:产生了棕黄色的雾 |
| D.图Ⅳ:湿润的有色布条褪色 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列图示与对应叙述相符的是

| A.图①表示向20 mL 0.1 mol/L氨水中逐滴加入0.1 mol/L醋酸,溶液导电性随加入酸体积的变化 |
B.图②表示压强对可逆反应A(g)+2B(g)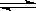 3C(g)+D(s)的影响,乙的压强比甲的压强大 3C(g)+D(s)的影响,乙的压强比甲的压强大 |
C.图③中曲线表示反应3A(g) + B(g) 2C(g)△H<0,正、逆反应的平衡常数K随温度的变化 2C(g)△H<0,正、逆反应的平衡常数K随温度的变化 |
| D.据图④,若要除去CuSO4溶液中的Fe3+,可加入NaOH溶液至pH在4左右 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】催化加氢生成乙烯和水是综合利用 CO2的热点研究领域。理论计算表明,在某刚性容器内,原料初始组成 n(CO2)∶n(H2)=1∶3,反应达到平衡时,四种组分的物质的量浓度 c 随温度 T 的变化如图所示。下列说法不正确的是


| A.曲线a 代表 H2 |
| B.该反应为放热反应 |
| C.E 点的正反应速率大于 F点的逆反应速率 |
D.450K 时,该反应平衡常数的数值为  |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】已知阿仑尼乌斯公式是反应速率常数随温度变化关系的经验公式,可写作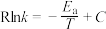 (k为反应速率常数,
(k为反应速率常数, 为反应活化能,R和C为大于0的常数),为探究m、n两种催化剂对某反应的催化效能,进行了实验探究,依据实验数据获得曲线如图所示。下列说法正确的是
为反应活化能,R和C为大于0的常数),为探究m、n两种催化剂对某反应的催化效能,进行了实验探究,依据实验数据获得曲线如图所示。下列说法正确的是
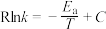 (k为反应速率常数,
(k为反应速率常数, 为反应活化能,R和C为大于0的常数),为探究m、n两种催化剂对某反应的催化效能,进行了实验探究,依据实验数据获得曲线如图所示。下列说法正确的是
为反应活化能,R和C为大于0的常数),为探究m、n两种催化剂对某反应的催化效能,进行了实验探究,依据实验数据获得曲线如图所示。下列说法正确的是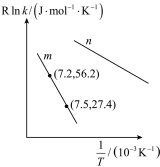
A.在m催化剂作用下,该反应的活化能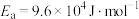 |
| B.对该反应催化效能较高的催化剂是m |
| C.不改变其他条件,升高温度,会降低反应的活化能 |
| D.可以根据该图像判断升高温度时平衡移动的方向 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】向容积为1L的恒容密闭容器中充入一定量 气体,发生反应:
气体,发生反应: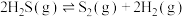 ,平衡时三种组分的物质的量与温度的关系如图所示,下列说法不正确的是
,平衡时三种组分的物质的量与温度的关系如图所示,下列说法不正确的是
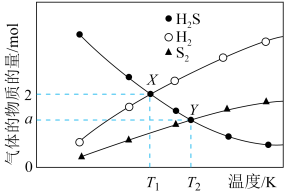
 气体,发生反应:
气体,发生反应: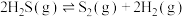 ,平衡时三种组分的物质的量与温度的关系如图所示,下列说法不正确的是
,平衡时三种组分的物质的量与温度的关系如图所示,下列说法不正确的是
A.该反应在温度为 时的平衡常数小于温度为 时的平衡常数小于温度为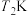 时的平衡常数 时的平衡常数 |
B.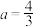 |
C.X点时压缩容器容积, 的平衡转化率减小 的平衡转化率减小 |
D.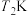 时,向Y点容器中再充入 时,向Y点容器中再充入  和 和  ,此时 ,此时 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】对于可逆反应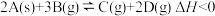 ,在一定条件下达到平衡状态,下列有关叙述正确的是( )
,在一定条件下达到平衡状态,下列有关叙述正确的是( )
①增大物质A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动, 减小
减小
③压强增大一倍,平衡不移动, 、
、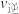 不变
不变
④增大物质B的浓度,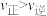
⑤加入催化剂,物质B的转化率提高
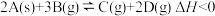 ,在一定条件下达到平衡状态,下列有关叙述正确的是( )
,在一定条件下达到平衡状态,下列有关叙述正确的是( )①增大物质A的量,平衡向正反应方向移动
②升高温度,平衡向逆反应方向移动,
 减小
减小③压强增大一倍,平衡不移动,
 、
、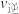 不变
不变④增大物质B的浓度,
⑤加入催化剂,物质B的转化率提高
| A.①②⑤ | B.④ | C.②③④ | D.④⑤ |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已建立平衡的某可逆反应,当改变条件使平衡向正反应方向移动时,下列叙述正确的是
①正反应速率一定大于逆反应速率 ②反应物的转化率一定增加
③反应物的浓度一定降低 ④生成物的产量一定增加
⑤生成物的体积分数一定增加 ⑥正逆反应速率均增大
①正反应速率一定大于逆反应速率 ②反应物的转化率一定增加
③反应物的浓度一定降低 ④生成物的产量一定增加
⑤生成物的体积分数一定增加 ⑥正逆反应速率均增大
| A.①②④ | B.②③⑤ | C.①④ | D.③⑤⑥ |
您最近半年使用:0次

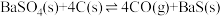 ,其
,其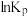 与
与 的关系如图所示。下列说法正确的是
的关系如图所示。下列说法正确的是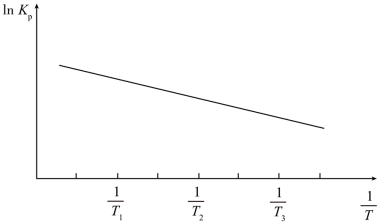


 为例,探究影响平衡移动的因素。
为例,探究影响平衡移动的因素。 溶液,分别进行下列实验,对实验现象的分析
溶液,分别进行下列实验,对实验现象的分析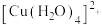 和
和 同时存在
同时存在 溶液,静置,上层清液为蓝色
溶液,静置,上层清液为蓝色 片,静置,上层清液为浅黄绿色
片,静置,上层清液为浅黄绿色

