名校
解题方法
1 . 氢燃料电池汽车所用的有机物液体储氢技术应用前景广阔。该技术的化学反应原理是在一定条件下,环己烷发生气相脱氢反应释放出氢气(反向即为储氢过程):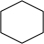 (g)⇌
(g)⇌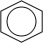 (g)+3H2(g),已知该反应平衡常数与温度的关系如下表:
(g)+3H2(g),已知该反应平衡常数与温度的关系如下表:
140℃时,在体积为2L的密闭容器中充入1mol环己烷(g),发生上述反应。完成下列填空:
(1)元素周期表中,碳元素的位置是_______ 。列举一个能说明硫元素非金属性比碳元素强的事实_______ 。
(2)该反应的化学平衡常数表达式_______ ,正反应是_______ (填“吸热”或“放热”)反应。
(3)若5min时,容器中气体的物质的量增大为原来的2.2倍,此时环己烷的转化率为_______ ,v(正)_______ v(逆)(填“>”、“=”或“<”)。
(4)恒压下,环己烷起始浓度相同时,该反应在有、无分子筛膜时环己烷的平衡转化率随温度的变化如下图所示,其中分子筛膜能选择性分离出H2。

用化学平衡移动原理解释分子筛膜对环己烷平衡转化率的影响_______ 。
 (g)⇌
(g)⇌ (g)+3H2(g),已知该反应平衡常数与温度的关系如下表:
(g)+3H2(g),已知该反应平衡常数与温度的关系如下表:| 温度/℃ | 120 | 140 | 160 |
| 平衡常数 | 5.343×10-2 | 1.152 | 18.70 |
140℃时,在体积为2L的密闭容器中充入1mol环己烷(g),发生上述反应。完成下列填空:
(1)元素周期表中,碳元素的位置是
(2)该反应的化学平衡常数表达式
(3)若5min时,容器中气体的物质的量增大为原来的2.2倍,此时环己烷的转化率为
(4)恒压下,环己烷起始浓度相同时,该反应在有、无分子筛膜时环己烷的平衡转化率随温度的变化如下图所示,其中分子筛膜能选择性分离出H2。

用化学平衡移动原理解释分子筛膜对环己烷平衡转化率的影响
您最近半年使用:0次



