21-22高三上·吉林·期末
名校
解题方法
1 . 以CO和CO2为原料合成乙烯、二甲醚(CH3OCH3)等有机物,一直是当前化学领域研究的热点。回答下列问题:
(1)已知相关物质能量变化示意图如下:
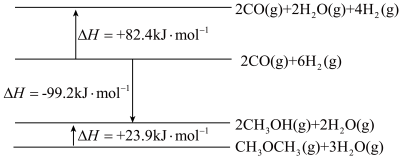
①写出由CO(g)和H2(g)反应生成CH3OCH3(g)和H2O(g)的热化学方程式:_______ 。
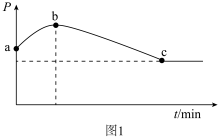
②在一绝热的恒容密闭容器中,通入CO和H2(物质的量之比1 :2)发生反应2CO(g)+4H2(g) C2H4(g) +2H2O(g) ΔH<0,反应过程中容器内压强(p)与时间(t)变化如图1所示,随着反应进行,a~b段压强增大的原因是
C2H4(g) +2H2O(g) ΔH<0,反应过程中容器内压强(p)与时间(t)变化如图1所示,随着反应进行,a~b段压强增大的原因是_______ 。
③CO2与H2催化重整制备CH3OCH3的过程中存在反应:
Ⅰ.2CO2(g) + 6H2(g) CH3OCH3(g)+3H2O(g);
CH3OCH3(g)+3H2O(g);
Ⅱ.CO2(g) +H2(g) CO(g) + H2O(g)。
CO(g) + H2O(g)。
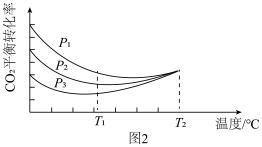
向密闭容器中以物质的量之比为1:3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图2所示。p1、p2、p3由大小的顺序为_______ ;T2℃时主要发生反应_______ (填“Ⅰ”或“Ⅱ”),平衡转化率随温度变化先降后升的原因为_______ 。
(2)一定温度和压强为3. 3p MPa条件下,将CO和H2按物质的量之比为2: 3通入密闭弹性容器中发生催化反应,假设只发生反应:3CO(g) + 3H2 (g) CH3OCH3(g)+CO2(g) 、2CO(g) + 4H2(g)
CH3OCH3(g)+CO2(g) 、2CO(g) + 4H2(g)  C2H4(g) + 2H2O(g)。平衡时,CO平衡转化率为60%,C2H4选择性为50%(C2H4的选择性=
C2H4(g) + 2H2O(g)。平衡时,CO平衡转化率为60%,C2H4选择性为50%(C2H4的选择性=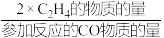 )。该温度下。反应C2H4(g)+ 2H2O(g)
)。该温度下。反应C2H4(g)+ 2H2O(g)  2CO(g) +4H2(g)的Kp=
2CO(g) +4H2(g)的Kp=_______ MPa3(用含字母p的代数式表示,已知Kp是用反应体系中气体物质的分压来表示的平衡常数,即将K表达式中平衡浓度用平衡分压代替),若要提高C2H4的选择性,则应考虑的因素是_______ 。
(1)已知相关物质能量变化示意图如下:

①写出由CO(g)和H2(g)反应生成CH3OCH3(g)和H2O(g)的热化学方程式:
②在一绝热的恒容密闭容器中,通入CO和H2(物质的量之比1 :2)发生反应2CO(g)+4H2(g)
 C2H4(g) +2H2O(g) ΔH<0,反应过程中容器内压强(p)与时间(t)变化如图1所示,随着反应进行,a~b段压强增大的原因是
C2H4(g) +2H2O(g) ΔH<0,反应过程中容器内压强(p)与时间(t)变化如图1所示,随着反应进行,a~b段压强增大的原因是
③CO2与H2催化重整制备CH3OCH3的过程中存在反应:
Ⅰ.2CO2(g) + 6H2(g)
 CH3OCH3(g)+3H2O(g);
CH3OCH3(g)+3H2O(g);Ⅱ.CO2(g) +H2(g)
 CO(g) + H2O(g)。
CO(g) + H2O(g)。向密闭容器中以物质的量之比为1:3充入CO2与H2,实验测得CO2的平衡转化率随温度和压强的变化关系如图2所示。p1、p2、p3由大小的顺序为

(2)一定温度和压强为3. 3p MPa条件下,将CO和H2按物质的量之比为2: 3通入密闭弹性容器中发生催化反应,假设只发生反应:3CO(g) + 3H2 (g)
 CH3OCH3(g)+CO2(g) 、2CO(g) + 4H2(g)
CH3OCH3(g)+CO2(g) 、2CO(g) + 4H2(g)  C2H4(g) + 2H2O(g)。平衡时,CO平衡转化率为60%,C2H4选择性为50%(C2H4的选择性=
C2H4(g) + 2H2O(g)。平衡时,CO平衡转化率为60%,C2H4选择性为50%(C2H4的选择性=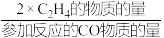 )。该温度下。反应C2H4(g)+ 2H2O(g)
)。该温度下。反应C2H4(g)+ 2H2O(g)  2CO(g) +4H2(g)的Kp=
2CO(g) +4H2(g)的Kp=
您最近一年使用:0次
2022-07-29更新
|
289次组卷
|
3卷引用:反应原理题



