名校
1 . 2018年,美国退出了《巴黎协定》实行再工业化战略,而中国却加大了环保力度,生动诠释了我国负责任的大国形象。近年我国大力加强温室气体CO2催化氢化合成甲醇技术的工业化量产研究,实现可持续发展。已知:3H2(g)+CO2(g)⇌CH3OH(g)+H2O(g) ΔH=-48.9kJ/mol
(1)为提高CH3OH转化率,理论上应采用的条件是________ (填字母)。
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),如图为不同投料比[ ]时某反应物X平衡转化率变化曲线。
]时某反应物X平衡转化率变化曲线。
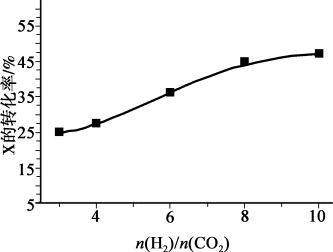
反应物X是_________ (填“CO2”或“H2”),理由是_________ 。
(3)250℃、在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得n(CH3OH)=1.5mol,这段时间内H2的平均速率为______ ,化学平衡常数K=___ 。
(1)为提高CH3OH转化率,理论上应采用的条件是
A.高温高压 B.低温低压 C.高温低压 D.低温高压
(2)250℃、在恒容密闭容器中由CO2(g)催化氢化合成CH3OH(g),如图为不同投料比[
 ]时某反应物X平衡转化率变化曲线。
]时某反应物X平衡转化率变化曲线。
反应物X是
(3)250℃、在体积为2.0L的恒容密闭容器中加入6molH2、2molCO2和催化剂,10min时反应达到平衡,测得n(CH3OH)=1.5mol,这段时间内H2的平均速率为
您最近一年使用:0次
真题
2 . 溴及其化合物广泛应用于医药、农药、纤维、塑料组燃剂等,回答下列问题:
(1)海水提溴过程中,向浓缩的海水中通入_______ ,将其中的Br-氧化,再用空气吹出溴;然后用碳酸钠溶液吸收溴,溴歧化为Br-和BrO ,其离子方程式为
,其离子方程式为_______ 。
(2)溴与氯能以共价键结合形成BrCl。BrCl分子中,_______ 显正电性。BrCl与水发生反应的化学方程式为_______ 。
(3)CuBr2分解的热化学方程式为:2CuBr2(s)=2CuBr(s)+ Br2(g) ∆H=+105.4kJ/mol在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa。
①如反应体系的体积不变,提高反应温度,则p(Br2)将会_______ (填“增大”、“不变”或“减小”)。
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为_______ 。
(1)海水提溴过程中,向浓缩的海水中通入
 ,其离子方程式为
,其离子方程式为(2)溴与氯能以共价键结合形成BrCl。BrCl分子中,
(3)CuBr2分解的热化学方程式为:2CuBr2(s)=2CuBr(s)+ Br2(g) ∆H=+105.4kJ/mol在密闭容器中将过量CuBr2于487K下加热分解,平衡时p(Br2)为4.66×103Pa。
①如反应体系的体积不变,提高反应温度,则p(Br2)将会
②如反应温度不变,将反应体系的体积增加一倍,则p(Br2)的变化范围为
您最近一年使用:0次
2019-01-30更新
|
1460次组卷
|
4卷引用:2013年全国普通高等学校招生统一考试化学(海南卷)



