1 . 二氧化碳是用途非常广泛的化工基础原料,回答下列问题:
(1)工业上可以用CO2来生产燃料甲醇。
已知;:CO2(g)+3H2(g) CH3OH(l)+H2O(l) △H=-131.0kJ/mol;
CH3OH(l)+H2O(l) △H=-131.0kJ/mol;
H2(g)+ O2(g)= H2O(l) △H=-285.8 kJ/mol。
O2(g)= H2O(l) △H=-285.8 kJ/mol。
CH3OH的燃烧热△H=_______ 。
(2)在催化剂作用下,CO2和CH4可以直接转化为乙酸:CO2(g)+CH4(g) CH3COOH(g) △H=+36.0kJ/mol。在不同温度下乙酸的生成速率变化如右图所示。
CH3COOH(g) △H=+36.0kJ/mol。在不同温度下乙酸的生成速率变化如右图所示。
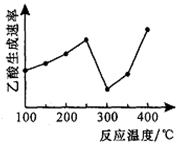
①当温度在250℃~300℃范围时,乙酸的生成速率减慢的主要原因是______ ;当温度在300℃~400℃范围时,影响乙酸生成速率的主要因素是________ 。
②欲使乙酸的平衡产率提高,应采取的措施是________ (填标号)。
A.升高温度 B.降低温度 C.增大压强 D.降低压强
(3)高温下,CO2与足量的碳在密闭容器中实现反应:C(s)+CO2(g) 2CO(g)。
2CO(g)。
①向容积为1L的恒容容器中加入0.2mol CO2,在不同温度下达到平衡时CO2的物质的量浓度c(CO2)随温度的变化如右图所示,则该反应为_____ (填“放热”或“吸热”)反应。某温度下,若向该平衡体系中再通入0.2mol CO2,平衡____ (填“正向”、“逆向”或“不”)移动,达到新平衡后,体系中CO的百分含量________ (填“变大”、“变小”或“不变”)。
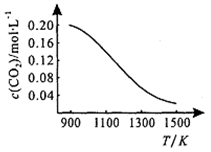
②向压强为p,体积可变的恒压容器中充入一定量CO2,650℃时反应达平衡,CO的体积分数为40.0%,则CO2的转化率为_________ 。气体分压(p分)=气体总压(p总)×体积分数,用某物质的平衡分压代替物质的量浓度也可以表示化学平衡常数(记作Kp),此温度下,该反应的化学平衡常数Kp=_________ (用含p的代数式表示),若向平衡体系中再充入V(CO2): V(CO)=5:4的混合气体,平衡______ (填“正向”、“逆向”或“不”)移动。
(1)工业上可以用CO2来生产燃料甲醇。
已知;:CO2(g)+3H2(g)
 CH3OH(l)+H2O(l) △H=-131.0kJ/mol;
CH3OH(l)+H2O(l) △H=-131.0kJ/mol;H2(g)+
 O2(g)= H2O(l) △H=-285.8 kJ/mol。
O2(g)= H2O(l) △H=-285.8 kJ/mol。CH3OH的燃烧热△H=
(2)在催化剂作用下,CO2和CH4可以直接转化为乙酸:CO2(g)+CH4(g)
 CH3COOH(g) △H=+36.0kJ/mol。在不同温度下乙酸的生成速率变化如右图所示。
CH3COOH(g) △H=+36.0kJ/mol。在不同温度下乙酸的生成速率变化如右图所示。
①当温度在250℃~300℃范围时,乙酸的生成速率减慢的主要原因是
②欲使乙酸的平衡产率提高,应采取的措施是
A.升高温度 B.降低温度 C.增大压强 D.降低压强
(3)高温下,CO2与足量的碳在密闭容器中实现反应:C(s)+CO2(g)
 2CO(g)。
2CO(g)。①向容积为1L的恒容容器中加入0.2mol CO2,在不同温度下达到平衡时CO2的物质的量浓度c(CO2)随温度的变化如右图所示,则该反应为

②向压强为p,体积可变的恒压容器中充入一定量CO2,650℃时反应达平衡,CO的体积分数为40.0%,则CO2的转化率为
您最近一年使用:0次
2017-11-03更新
|
795次组卷
|
4卷引用:第02章 化学反应速率与化学平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)
(已下线)第02章 化学反应速率与化学平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)四川省绵阳市2018届高三第一次诊断性考试理综化学试题四川省邻水实验学校2017-2018学年高二上学期第三次月考化学试题(已下线)黄金30题系列 高三化学 大题易丢分



