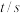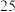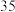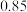名校
解题方法
1 . 恒温恒容下,将2 mol红棕色气体A和1.5 mol无色气体B通入体积为1 L的密闭容器中发生如下反应: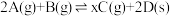 ,2 min时反应达到平衡状态,此时剩余1.1 mol B,并测得C的浓度为1.2 mol/L。
,2 min时反应达到平衡状态,此时剩余1.1 mol B,并测得C的浓度为1.2 mol/L。
(1)从开始反应至达到平衡状态,生成C的平均反应速率为_______ mol/(L·min)
(2)x=_______ ;A的转化率与B的转化率之比为_______
(3)写出该温度下的平衡常数表达式_______ (用相关字母表示),数值_______
(4)向平衡后的容器中继续充入0.8 molA(g)、0.9 molB(g)、0.8 molC(g)、1.2mol D(s),此时,v(正)_______ v(逆)。(填“>”、“=”或“<”)
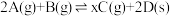 ,2 min时反应达到平衡状态,此时剩余1.1 mol B,并测得C的浓度为1.2 mol/L。
,2 min时反应达到平衡状态,此时剩余1.1 mol B,并测得C的浓度为1.2 mol/L。(1)从开始反应至达到平衡状态,生成C的平均反应速率为
(2)x=
(3)写出该温度下的平衡常数表达式
(4)向平衡后的容器中继续充入0.8 molA(g)、0.9 molB(g)、0.8 molC(g)、1.2mol D(s),此时,v(正)
您最近一年使用:0次
2022-06-02更新
|
806次组卷
|
7卷引用:辽宁省朝阳市建平县建平县实验中学2023-2024学年高二上学期开学考试化学试题
辽宁省朝阳市建平县建平县实验中学2023-2024学年高二上学期开学考试化学试题江苏省徐州市沛县2021-2022学年高二下学期第一次学情调研化学试题(已下线)第12练 用“三段式”模型突破化学平衡的计算-2022年【暑假分层作业】高二化学(2023届一轮复习通用)江西省抚州市南城县第二中学2022-2023学年高二上学期第一次月考化学试题江苏省连云港市赣榆智贤中学2022-2023学年高二上学期第一次学情检测化学试题辽宁省鞍山市普通高中2022-2023学年高二上学期第一次月考化学试题云南省大理白族自治州民族中学2023-2024学年高二上学期10月月考化学试题
名校
2 . 化学科学家采用丙烯歧化法制取乙烯和丁烯的反应原理为2C3H6(g) C2H4(g)+C4H8(g) ∆H。回答下列问题:
C2H4(g)+C4H8(g) ∆H。回答下列问题:
(1)向恒温恒容反应器中加入一定量的C3H6,生成C2H4的物质的量与时间的关系如表所示:
①a=_______ ,p初始:p5min=_______ 。
②其他条件不变,若缩小反应器的体积,则C3H6转化率_______ (填“增大”“减小”或“不变”)。
(2)将2 mol C3H6置于体积为1 L的恒容反应器中,反应进行15min时丙烯的转化率与温度的关系如图所示:
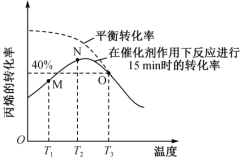
①N点_______ (填“有”或“没有”)达到平衡状态,原因是_______ 。
②M→N过程中C3H6转化率升高的原因是_______ 。
③T3时Kc=_______ ,若其他条件不变,往反应器中再加入2 mol C3H6,反应重新达到平衡时混合体系中乙烯的体积分数为_______ 。
 C2H4(g)+C4H8(g) ∆H。回答下列问题:
C2H4(g)+C4H8(g) ∆H。回答下列问题:(1)向恒温恒容反应器中加入一定量的C3H6,生成C2H4的物质的量与时间的关系如表所示:
| 反应时间/min | 0 | 5 | 10 | 15 | 20 | 25 |
| C2H4的物质的量/mol | 0 | 0.8 | 1.2 | 1.5 | a | 1.5 |
①a=
②其他条件不变,若缩小反应器的体积,则C3H6转化率
(2)将2 mol C3H6置于体积为1 L的恒容反应器中,反应进行15min时丙烯的转化率与温度的关系如图所示:

①N点
②M→N过程中C3H6转化率升高的原因是
③T3时Kc=
您最近一年使用:0次
2021-03-21更新
|
212次组卷
|
3卷引用:安徽省江淮名校2020-2021学年高二下学期开学联考化学试题
3 . 一定温度下,向 恒容容器中充入
恒容容器中充入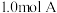 和
和 ,发生反应
,发生反应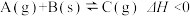 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
(1)前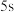 的平均反应速率
的平均反应速率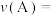
_______ ,达平衡时 的平衡体积分数为
的平衡体积分数为_______ 。
(2)由表中数据计算该温度下该反应的平衡常数为_______ ,随着反应温度升高,该反应的平衡常数_______ (选填“增大”、“减小”或“不变”)。
(3)保持温度不变,起始时向容器中充入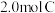 ,达平衡时,
,达平衡时, 的转化率为
的转化率为_______ 。
 恒容容器中充入
恒容容器中充入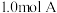 和
和 ,发生反应
,发生反应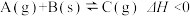 ,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
,经过一段时间后达到平衡。反应过程中测定的部分数据如表,回答下列问题:
|
|
|
|
|
|
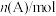 |
|
|
|
|
|
(1)前
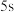 的平均反应速率
的平均反应速率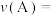
 的平衡体积分数为
的平衡体积分数为(2)由表中数据计算该温度下该反应的平衡常数为
(3)保持温度不变,起始时向容器中充入
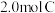 ,达平衡时,
,达平衡时, 的转化率为
的转化率为
您最近一年使用:0次
2021-02-03更新
|
212次组卷
|
2卷引用:四川省乐山市沫若中学2020-2021学年高二下学期入学考试化学试题
名校
解题方法
4 . T℃ 时,在一容积为 2 L 的恒容密闭容器中加入 2 mol A 和 3 mol B,压强为 P0, 在催化剂存在的条件下进行下列反应:2A(g)+3B(g) ⇌3C(g),2 分钟达到平衡,平衡混合气中 C 的体积分数为 37.5%。 已知该反应某一时刻的瞬时速率计算公式为v正=k正·[A]2·[B]3,v逆=k逆·[C]3,其中 k正、k逆为速率常数。
(1)计算上述条件下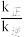 的值。 (写出必要的计算过程,下同)
的值。 (写出必要的计算过程,下同)_____
(2)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数,记作 Kp。已知某气体分压(P分)=气体总压(P总) ×该气体的物质的量分数,计算 T℃ 时上述反应 Kp 的值(用含 P0 的数值表示)。____________
(1)计算上述条件下
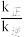 的值。 (写出必要的计算过程,下同)
的值。 (写出必要的计算过程,下同)(2)用某物质的平衡分压代替其物质的量浓度也可以表示化学平衡常数,记作 Kp。已知某气体分压(P分)=气体总压(P总) ×该气体的物质的量分数,计算 T℃ 时上述反应 Kp 的值(用含 P0 的数值表示)。
您最近一年使用:0次
2020-03-27更新
|
348次组卷
|
3卷引用:山西省汾阳市汾阳中学2020-2021学年高二下学期开学考试化学试题
12-13高二上·河南·期中
名校
5 . 一定温度下的密闭容器中存在如下反应:CO(g)+H2O(g)  CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol·L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol·L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
(1)当CO转化率为25%时,该反应是否达到平衡,若未达到,向哪个方向进行?
(2)达到平衡时,CO的转化率为多少?
(3)当CO的起始浓度仍为2mol·L-1,H2O(g)的起始浓度为6mol·L-1,求平衡时CO的转化率?
 CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol·L-1,经测定该反应在该温度下的平衡常数K=1,试判断:
CO2(g)+H2(g),已知CO(g)和H2O(g)的起始浓度均为2mol·L-1,经测定该反应在该温度下的平衡常数K=1,试判断:(1)当CO转化率为25%时,该反应是否达到平衡,若未达到,向哪个方向进行?
(2)达到平衡时,CO的转化率为多少?
(3)当CO的起始浓度仍为2mol·L-1,H2O(g)的起始浓度为6mol·L-1,求平衡时CO的转化率?
您最近一年使用:0次
2013-11-28更新
|
1044次组卷
|
9卷引用:2014-2015学年湖北咸宁鄂南高级中学高二起点考试化学(B类)试卷
(已下线)2014-2015学年湖北咸宁鄂南高级中学高二起点考试化学(B类)试卷(已下线)2012-2013学年河南省河南大学附中高二上学期期中考试化学试卷(已下线)2013-2014学年江西省南昌市四校联考高二上学期期中考试化学试卷(已下线)2013-2014学年江西省南昌市高二上学期期中测试理科化学试卷(甲)河北省大名县第一中学2017-2018学年高二上学期第一次月考化学试题黑龙江省双鸭山市第一中学2017-2018学年高二9月月考化学试题甘肃省白银市会宁县第一中学2019-2020学年高二上学期期中考试化学(理)试题(已下线)2.2.3 化学平衡常数(重点练)——2020-2021学年高二化学上学期十分钟同步课堂专练(苏教版选修4)江苏省镇江第一中学2020-2021学年高二上期末测试化学试题