1 . 酸碱盐等电解质溶液中存在的电离平衡、水解平衡和沉淀溶解平衡都与生命活动、日常生活、工农业生产和环境保护等息息相关。请回答下列问题:
(1) 水溶液显
水溶液显_______ 性(填“酸”、“碱”或“中”),原因是_______ (用离子方程式表示)。
(2)用离子方程式表示泡沫灭火器的工作原理_______ 。
(3)物质的量浓度相同的下列溶液:① ②
② ③
③ ④
④ ,其中
,其中 由大到小的顺序是
由大到小的顺序是_______ (填序号)。
(4)25℃时, 的盐酸和
的盐酸和 的NaOH溶液混合后溶液
的NaOH溶液混合后溶液 (忽略溶液混合时体积的变化),则
(忽略溶液混合时体积的变化),则
_______ 。
(5)25℃时,某溶液中 白的浓度为
白的浓度为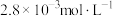 ,使
,使 开始沉淀的
开始沉淀的
_______ 。(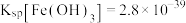 )
)
(6)25℃时,将: 溶液与
溶液与 溶液等体积混合,反应后的溶液中
溶液等体积混合,反应后的溶液中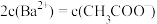 ,用含a和b的代数式表示醋酸的电离常数
,用含a和b的代数式表示醋酸的电离常数
_______ 。
(1)
 水溶液显
水溶液显(2)用离子方程式表示泡沫灭火器的工作原理
(3)物质的量浓度相同的下列溶液:①
 ②
② ③
③ ④
④ ,其中
,其中 由大到小的顺序是
由大到小的顺序是(4)25℃时,
 的盐酸和
的盐酸和 的NaOH溶液混合后溶液
的NaOH溶液混合后溶液 (忽略溶液混合时体积的变化),则
(忽略溶液混合时体积的变化),则
(5)25℃时,某溶液中
 白的浓度为
白的浓度为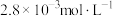 ,使
,使 开始沉淀的
开始沉淀的
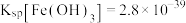 )
)(6)25℃时,将:
 溶液与
溶液与 溶液等体积混合,反应后的溶液中
溶液等体积混合,反应后的溶液中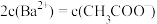 ,用含a和b的代数式表示醋酸的电离常数
,用含a和b的代数式表示醋酸的电离常数
您最近一年使用:0次
2 . 数学计算令人头大,物理公式也难拿下,化学计算数字不大,得个高分不在话下。请认真完成以下计算,让化学成绩为你舔砖加瓦。
(1)常温下,0.05mol/L硫酸溶液中,C(H+)=___________ mol/L
(2)某温度,纯水中C(H+)=3×10-7mol/L,则:纯水中C(OH-)=___________ mol/L,此时温度___________ (填“高于”“低于”或“等于”)25℃。若温度不变,滴入盐酸后C(H+)=5×10-4mol/L,则溶液中C(OH-)=___________ mol/L,由水电离的C(H+)=___________ mol/L。
(3)室温下,pH=3的盐酸与pH=5的H2SO4溶液等体积混合(忽略体积变化),混合溶液的pH=___________ 。
(4)常温向水中加入少量碳酸钠固体,得到pH为11的溶液,溶液中c(OH-)=_____ mol·L-1。
(1)常温下,0.05mol/L硫酸溶液中,C(H+)=
(2)某温度,纯水中C(H+)=3×10-7mol/L,则:纯水中C(OH-)=
(3)室温下,pH=3的盐酸与pH=5的H2SO4溶液等体积混合(忽略体积变化),混合溶液的pH=
(4)常温向水中加入少量碳酸钠固体,得到pH为11的溶液,溶液中c(OH-)=
您最近一年使用:0次
3 . 常温下,若在实验室中配制500mL 溶液,为使配制过程中不出现浑浊现象,至少需要
溶液,为使配制过程中不出现浑浊现象,至少需要 的盐酸的体积是
的盐酸的体积是_______ (已知 的
的 为
为 )。
)。
 溶液,为使配制过程中不出现浑浊现象,至少需要
溶液,为使配制过程中不出现浑浊现象,至少需要 的盐酸的体积是
的盐酸的体积是 的
的 为
为 )。
)。
您最近一年使用:0次
名校
解题方法
4 . Ⅰ、某实验小组用100mL0.55mol·L NaOH溶液与100mL0.5mol·L
NaOH溶液与100mL0.5mol·L 盐酸进行中和热的测定,装置如图所示。
盐酸进行中和热的测定,装置如图所示。
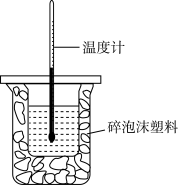
(1)回答下列问题:
①图中装置缺少的仪器是___________ 。
②若将盐酸改为相同体积、相同浓度的醋酸,测得中和热为ΔH1,NaOH溶液与盐酸反应中和热为ΔH,则ΔH1___________ ΔH (填写<、>、=);若测得该反应放出的热量为2.84kJ,请写出盐酸与NaOH溶液反应的中和热的热化学方程式:___________
Ⅱ、已知1g的甲烷完全燃烧生成液态水放出akJ的热量。
(2)写出表示甲烷燃烧热的热化学方程式为___________ 。
Ⅲ、发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:

 kJ·mol
kJ·mol

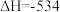 kJ·mol
kJ·mol
(3)写出肼和二氧化氮反应的热化学方程式为:___________ 。
(4)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463kJ·mol ,O=O键能为498kJ·mol
,O=O键能为498kJ·mol ,计算H-H键能为
,计算H-H键能为___________ kJ·mol 。
。
 NaOH溶液与100mL0.5mol·L
NaOH溶液与100mL0.5mol·L 盐酸进行中和热的测定,装置如图所示。
盐酸进行中和热的测定,装置如图所示。
(1)回答下列问题:
①图中装置缺少的仪器是
②若将盐酸改为相同体积、相同浓度的醋酸,测得中和热为ΔH1,NaOH溶液与盐酸反应中和热为ΔH,则ΔH1
Ⅱ、已知1g的甲烷完全燃烧生成液态水放出akJ的热量。
(2)写出表示甲烷燃烧热的热化学方程式为
Ⅲ、发射卫星可用肼做燃料,二氧化氮做氧化剂,两者反应生成氮气和水蒸气。已知:

 kJ·mol
kJ·mol

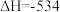 kJ·mol
kJ·mol
(3)写出肼和二氧化氮反应的热化学方程式为:
(4)有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463kJ·mol
 ,O=O键能为498kJ·mol
,O=O键能为498kJ·mol ,计算H-H键能为
,计算H-H键能为 。
。
您最近一年使用:0次
2023-01-08更新
|
320次组卷
|
2卷引用:四川省宜宾市叙州区第二中学校2022-2023学年高二下学期开学考试化学试题
5 . 已知在25 ℃时Ksp[Mg(OH)2]=3.2×10-11,Ksp[Cu(OH)2]=2.2×10-20。
(1)假设饱和Mg(OH)2溶液的密度为1 g·mL-1,试求Mg(OH)2的溶解度为_______ g。
(2)在25 ℃时,向0.02 mol·L-1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为_______ mol·L-1。
(3)25 ℃时,向浓度均为0.02 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入NaOH溶液,先生成_______ 沉淀(填化学式);生成该沉淀的离子方程式为_______ ;当两种沉淀共存时,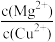 =
=_______ 。
(1)假设饱和Mg(OH)2溶液的密度为1 g·mL-1,试求Mg(OH)2的溶解度为
(2)在25 ℃时,向0.02 mol·L-1的MgCl2溶液中加入NaOH固体,如要生成Mg(OH)2沉淀,应使溶液中的c(OH-)最小为
(3)25 ℃时,向浓度均为0.02 mol·L-1的MgCl2和CuCl2混合溶液中逐滴加入NaOH溶液,先生成
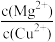 =
=
您最近一年使用:0次
2022-12-14更新
|
240次组卷
|
2卷引用:云南省广南县二中2021-2022年学年高二下学期开学考试化学试题
名校
6 . CO、 、
、 是工业上重要的化工原料。
是工业上重要的化工原料。
已知:①
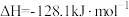
②
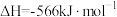
③
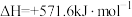
请回答下列问题:
(1)上述反应中属于放热反应的是_______ (填标号)。
(2)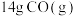 完全燃烧放出的热量为
完全燃烧放出的热量为_______ 。
(3)表示 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为_______ 。
(4)1.5mol由CO和 组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、
组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、 的物质的量分别为
的物质的量分别为_______ mol、_______ mol。
(5)等质量的 、
、 、
、 完全燃烧,放热最多的是
完全燃烧,放热最多的是_______ (填化学式)。
(6)某些常见化学键的键能数据如下表:
则

_______  。
。
 、
、 是工业上重要的化工原料。
是工业上重要的化工原料。已知:①

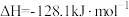
②

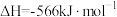
③

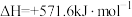
请回答下列问题:
(1)上述反应中属于放热反应的是
(2)
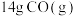 完全燃烧放出的热量为
完全燃烧放出的热量为(3)表示
 的燃烧热的热化学方程式为
的燃烧热的热化学方程式为(4)1.5mol由CO和
 组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、
组成的混合气体在足量氧气中充分燃烧放出的热量为425.9kJ,则混合气体中CO、 的物质的量分别为
的物质的量分别为(5)等质量的
 、
、 、
、 完全燃烧,放热最多的是
完全燃烧,放热最多的是(6)某些常见化学键的键能数据如下表:
| 化学键 | C=O | H—O | H—H |  |
键能 | 803 | 463 | 436 | 1076 |


 。
。
您最近一年使用:0次
2022-11-07更新
|
346次组卷
|
6卷引用:河北省保定市保定市部分高中2023-2024学年高二上学期开学考试化学试题
名校
7 . 计算25 ℃时下列溶液的pH:
(1)1 mL pH=2的 溶液加水稀释至100 mL,pH=
溶液加水稀释至100 mL,pH=_______ ;
(2)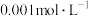 的盐酸,pH=
的盐酸,pH=_______ ;
(3) 的NaOH溶液,pH=
的NaOH溶液,pH=_______ ;
(1)1 mL pH=2的
 溶液加水稀释至100 mL,pH=
溶液加水稀释至100 mL,pH=(2)
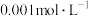 的盐酸,pH=
的盐酸,pH=(3)
 的NaOH溶液,pH=
的NaOH溶液,pH=
您最近一年使用:0次
2022-10-06更新
|
372次组卷
|
2卷引用:黑龙江省佳木斯市第八中学2021-2022学年高二下学期开学考试化学试题
解题方法
8 . 反应4NH3(g)+5O2(g) 4NO(g)+6H2O(g)在2L的密闭容器中进行,1min后,氨气减少了0.12mol。求:
4NO(g)+6H2O(g)在2L的密闭容器中进行,1min后,氨气减少了0.12mol。求:
(1)1min内,以氨气表示的化学反应速率_______ 。
(2)1min内,以氧气表示的化学反应速率_______ 。
(3)1min内,用水表示的化学反应速率_______ 。
(4)分别用NH3、O2、NO、H2O表示的化学反应速率之比为_______ 。
 4NO(g)+6H2O(g)在2L的密闭容器中进行,1min后,氨气减少了0.12mol。求:
4NO(g)+6H2O(g)在2L的密闭容器中进行,1min后,氨气减少了0.12mol。求:(1)1min内,以氨气表示的化学反应速率
(2)1min内,以氧气表示的化学反应速率
(3)1min内,用水表示的化学反应速率
(4)分别用NH3、O2、NO、H2O表示的化学反应速率之比为
您最近一年使用:0次
名校
解题方法
9 . 完成下列问题。
(1)已知完全断裂物质的量均为1mol的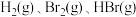 中的化学键时吸收能量分别为
中的化学键时吸收能量分别为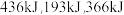 。则在该条件下,
。则在该条件下, 与
与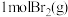 完全反应会
完全反应会_______ (填“吸收”或“放出”)_______  能量。
能量。
(2)将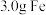 和
和 的混合粉末完全溶于
的混合粉末完全溶于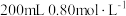 盐酸中,生成标准状况下
盐酸中,生成标准状况下 (假设气体被完全收集);反应后的溶液中滴入2滴
(假设气体被完全收集);反应后的溶液中滴入2滴 溶液后不显血红色。请通过分析计算回答:
溶液后不显血红色。请通过分析计算回答:
①则混合粉末中Fe的物质的量是_______ mol;
②若在反应后的混合液中加入锌,则理论上最多可溶解锌的质量是_______ g。
(1)已知完全断裂物质的量均为1mol的
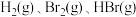 中的化学键时吸收能量分别为
中的化学键时吸收能量分别为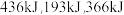 。则在该条件下,
。则在该条件下, 与
与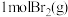 完全反应会
完全反应会 能量。
能量。(2)将
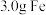 和
和 的混合粉末完全溶于
的混合粉末完全溶于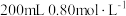 盐酸中,生成标准状况下
盐酸中,生成标准状况下 (假设气体被完全收集);反应后的溶液中滴入2滴
(假设气体被完全收集);反应后的溶液中滴入2滴 溶液后不显血红色。请通过分析计算回答:
溶液后不显血红色。请通过分析计算回答:①则混合粉末中Fe的物质的量是
②若在反应后的混合液中加入锌,则理论上最多可溶解锌的质量是
您最近一年使用:0次
解题方法
10 . 向500mL 和NaOH的混合溶液中持续通入
和NaOH的混合溶液中持续通入 。通入
。通入 的体积和溶液中沉淀的关系如图所示(气体体积均已换算为标准状况下的体积,忽略
的体积和溶液中沉淀的关系如图所示(气体体积均已换算为标准状况下的体积,忽略 与水的反应和溶液体积变化等)。请回答:
与水的反应和溶液体积变化等)。请回答:

(1)混合溶液中 的物质的量浓度为
的物质的量浓度为_______ mol/L。
(2)当通入的 总体积为2240mL时,溶液中
总体积为2240mL时,溶液中 与
与 的物质的量之比为
的物质的量之比为_______ 。
 和NaOH的混合溶液中持续通入
和NaOH的混合溶液中持续通入 。通入
。通入 的体积和溶液中沉淀的关系如图所示(气体体积均已换算为标准状况下的体积,忽略
的体积和溶液中沉淀的关系如图所示(气体体积均已换算为标准状况下的体积,忽略 与水的反应和溶液体积变化等)。请回答:
与水的反应和溶液体积变化等)。请回答:
(1)混合溶液中
 的物质的量浓度为
的物质的量浓度为(2)当通入的
 总体积为2240mL时,溶液中
总体积为2240mL时,溶液中 与
与 的物质的量之比为
的物质的量之比为
您最近一年使用:0次



