解题方法
1 . 在密闭容器中进行反应: X(g)+Y(g)  3Z(g) ΔH < 0,下列图象不正确的是
3Z(g) ΔH < 0,下列图象不正确的是
 3Z(g) ΔH < 0,下列图象不正确的是
3Z(g) ΔH < 0,下列图象不正确的是A. | B.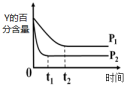 | C.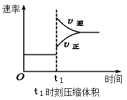 | D.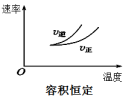 |
您最近一年使用:0次
2 . 一定温度下,向一容积为5L的恒容密闭容器中充入0.4 molSO2和0.2mol O2发生反应: 2SO2(g)+O2(g) 2SO3(g) △H=-196 kJ/mol. 当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
2SO3(g) △H=-196 kJ/mol. 当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是__________ (填字母)。
a. SO2、O2、SO3三者的浓度之比为2:1:2 b.发容器内气体的压强不再变化
c.容器内混合气体的密度保持不变 d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)①有利于提高SO2的平衡转化率的措施有:______
a.使用催化剂 b.降低温度 c.及时分离出SO3
②其他条件不变时,减小压强(拉升容器使容积为原来的两倍),平衡将向逆反应方向移动,请利用K、Q 的关系说明理由:_________________ 。
(3)①SO2的平衡转化率为______________ 。
②此温度下该反应的平衡常数K=_____________ 。
(4)如图所示平衡时SO3的体积分数随压强和温度变化的曲线,则:
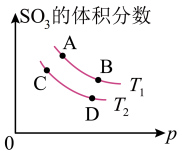
①温度关系:T1______ T2(填“>”“<”“=”,下同)
②平衡常数文关系:KA_____ KB,KA______ KD。
 2SO3(g) △H=-196 kJ/mol. 当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:
2SO3(g) △H=-196 kJ/mol. 当反应达到平衡时,容器内压强变为起始时的0.7倍。请回答下列问题:(1)判断该反应达到平衡状态的标志是
a. SO2、O2、SO3三者的浓度之比为2:1:2 b.发容器内气体的压强不再变化
c.容器内混合气体的密度保持不变 d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)①有利于提高SO2的平衡转化率的措施有:
a.使用催化剂 b.降低温度 c.及时分离出SO3
②其他条件不变时,减小压强(拉升容器使容积为原来的两倍),平衡将向逆反应方向移动,请利用K、Q 的关系说明理由:
(3)①SO2的平衡转化率为
②此温度下该反应的平衡常数K=
(4)如图所示平衡时SO3的体积分数随压强和温度变化的曲线,则:

①温度关系:T1
②平衡常数文关系:KA
您最近一年使用:0次
2020-11-13更新
|
243次组卷
|
2卷引用:福建省厦门市湖滨中学2021-2022学年高二上学期期中考试化学试题



