1 . 为探究外界条件对反应: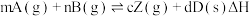 的影响,以A和B物质的量之比为
的影响,以A和B物质的量之比为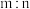 开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是

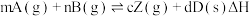 的影响,以A和B物质的量之比为
的影响,以A和B物质的量之比为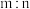 开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
| A.在恒温恒容条件下,向已达到平衡的体系中加入少量A,平衡正向移动,A的百分含量减小 |
B.降低温度, 比 比 减少更多 减少更多 |
| C.不断增加A的投料量,Z的体积分数可能减少 |
D.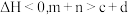 |
您最近半年使用:0次
2 . 某化学科研小组研究在其他条件不变时,改变某一条件对反应[可用 表示]化学平衡的影响,得到如图所示图像(图中
表示]化学平衡的影响,得到如图所示图像(图中 表示压强,
表示压强, 表示温度,
表示温度, 表示物质的量,
表示物质的量, 表示平衡转化率,
表示平衡转化率, 表示平衡体积分数):
表示平衡体积分数):
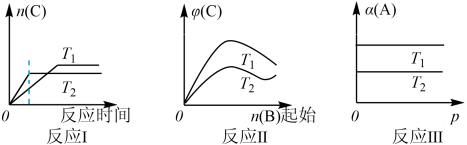
分析图像,回答下列问题:
(1)在反应I中,T1___________ (填“>”“<”或“=”)T2,该正反应为___________ (填“吸热”或“放热”)反应。
(2)在反应Ⅱ中,若此正反应为吸热反应,则T1___________ (填“>”“<”或“=”)T2。
(3)在反应Ⅲ中,a+b___________ c(填“>”“<”或“=”)。
 表示]化学平衡的影响,得到如图所示图像(图中
表示]化学平衡的影响,得到如图所示图像(图中 表示压强,
表示压强, 表示温度,
表示温度, 表示物质的量,
表示物质的量, 表示平衡转化率,
表示平衡转化率, 表示平衡体积分数):
表示平衡体积分数):
分析图像,回答下列问题:
(1)在反应I中,T1
(2)在反应Ⅱ中,若此正反应为吸热反应,则T1
(3)在反应Ⅲ中,a+b
您最近半年使用:0次
名校
解题方法
3 . 在2L恒容密闭容器中充入2mol X和1mol Y发生反应
 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
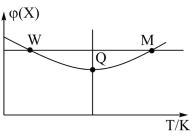

 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
| A.Q点时,Y的转化率最大 |
| B.W点X的正反应速率等于M点X的正反应速率 |
| C.升高温度,平衡常数增大 |
| D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
您最近半年使用:0次
2023-10-22更新
|
385次组卷
|
3卷引用:福建省福州三中2023-2024学年高二上学期期中考试化学试题
名校
解题方法
4 . 甲醇制烯烃(MTO)是煤制烯烃工艺路线的核心技术。煤制烯烃主要包括煤的气化、液化、烯烃化三个阶段。
(1)煤的液化发生的主要反应之一为
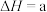 kJ⋅mol
kJ⋅mol ,在不同温度下,K(500°C)
,在不同温度下,K(500°C)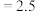 (mol⋅L
(mol⋅L ),K(700°C)
),K(700°C)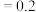 (mol⋅L
(mol⋅L )
)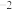 。
。
①
___________ 0(填“>”、“<”、“=”)。
②若反应在容积为2L的密闭容器中进行,500℃测得某一时刻体系内 、CO、
、CO、 物质的量分别为2 mol、1 mol、3 mol,则此时生成
物质的量分别为2 mol、1 mol、3 mol,则此时生成 的速率
的速率___________ 消耗 的速率(填“>”、“<”、“=”)。
的速率(填“>”、“<”、“=”)。
(2)通过研究外界条件对反应的影响,尽可能提高甲醇生成乙烯或丙烯的产率。
甲醇制烯烃的主要反应有:
Ⅰ.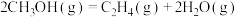
 kJ⋅mol
kJ⋅mol
Ⅱ.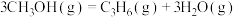
 kJ⋅mol
kJ⋅mol
Ⅲ.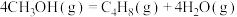
 kJ⋅mol
kJ⋅mol
① 转化为
转化为 的热化学方程式为Ⅳ:
的热化学方程式为Ⅳ: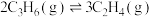
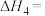
___________ 。
②加入 作为稀释剂,反应Ⅰ中
作为稀释剂,反应Ⅰ中 的产率将
的产率将___________ (填“增大”、“减小”或“不变”)。
(3)为研究不同条件对反应的影响,测得不同温度下平衡时 、
、 和
和 的物质的量分数变化,如图所示:
的物质的量分数变化,如图所示:
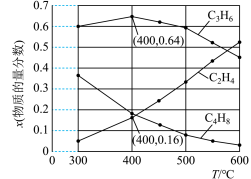
①随着温度的升高, 的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是
的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是___________ 。
②体系总压为0.1 MPa,400℃时反应Ⅳ的平衡常数
___________ 。
(1)煤的液化发生的主要反应之一为

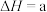 kJ⋅mol
kJ⋅mol ,在不同温度下,K(500°C)
,在不同温度下,K(500°C)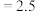 (mol⋅L
(mol⋅L ),K(700°C)
),K(700°C)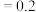 (mol⋅L
(mol⋅L )
)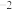 。
。①

②若反应在容积为2L的密闭容器中进行,500℃测得某一时刻体系内
 、CO、
、CO、 物质的量分别为2 mol、1 mol、3 mol,则此时生成
物质的量分别为2 mol、1 mol、3 mol,则此时生成 的速率
的速率 的速率(填“>”、“<”、“=”)。
的速率(填“>”、“<”、“=”)。(2)通过研究外界条件对反应的影响,尽可能提高甲醇生成乙烯或丙烯的产率。
甲醇制烯烃的主要反应有:
Ⅰ.
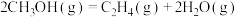
 kJ⋅mol
kJ⋅mol
Ⅱ.
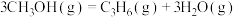
 kJ⋅mol
kJ⋅mol
Ⅲ.
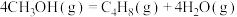
 kJ⋅mol
kJ⋅mol
①
 转化为
转化为 的热化学方程式为Ⅳ:
的热化学方程式为Ⅳ: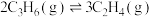
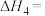
②加入
 作为稀释剂,反应Ⅰ中
作为稀释剂,反应Ⅰ中 的产率将
的产率将(3)为研究不同条件对反应的影响,测得不同温度下平衡时
 、
、 和
和 的物质的量分数变化,如图所示:
的物质的量分数变化,如图所示:
①随着温度的升高,
 的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是
的物质的量分数呈现先增大后减小的趋势。温度高于400℃时,原因是②体系总压为0.1 MPa,400℃时反应Ⅳ的平衡常数

您最近半年使用:0次
名校
解题方法
5 . 下列图示与对应的叙述相符的是
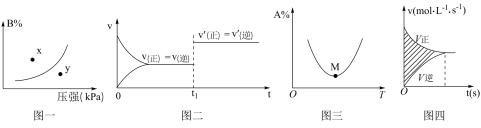

A.图一表示反应:  ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 |
B.图二是可逆反应  的速率时间图像,在 的速率时间图像,在 时刻改变条件一定是加入催化剂 时刻改变条件一定是加入催化剂 |
C.图三表示对于化学反应 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 |
D.图四所示图中的阴影部分面积的含义是( ) ) |
您最近半年使用:0次
2023-10-10更新
|
446次组卷
|
4卷引用:福建省南安市华侨中学2023-2024学年高二上学期10月月考化学试题
6 . 二甲醚是一种重要的清洁燃料,工业上可以通过 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。
Ⅰ. 分子间脱水制二甲醚
分子间脱水制二甲醚

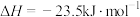 。在
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
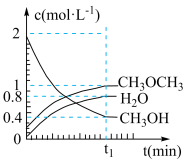
(1) 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡_____ (填“向右”、“向左”或“不发生”)移动,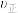 将
将_____ (填“增大”或“减小”)
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为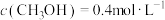 、
、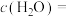
 、
、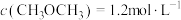 ,此时
,此时
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
Ⅱ.合成气制取二甲醚的原理如下:
反应1:
反应2:
(3)500K时,在2L密闭容器中充入4molCO和8mol ,4min达到平衡,平衡时CO的转化率为80%,且
,4min达到平衡,平衡时CO的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率
_____ ,反应1的平衡常数
_____ (结果需化成最简比)。
(4)由天然气获得合成气过程中可能发生以下反应:

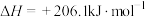
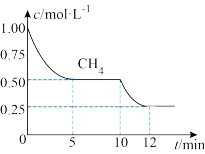
在一密闭容器中进行上述反应,测得 随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。Ⅰ.
 分子间脱水制二甲醚
分子间脱水制二甲醚
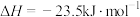 。在
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。 
(1)
 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡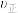 将
将(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为
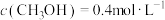 、
、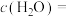
 、
、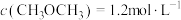 ,此时
,此时
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。Ⅱ.合成气制取二甲醚的原理如下:
反应1:

反应2:

(3)500K时,在2L密闭容器中充入4molCO和8mol
 ,4min达到平衡,平衡时CO的转化率为80%,且
,4min达到平衡,平衡时CO的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率

(4)由天然气获得合成气过程中可能发生以下反应:

在一密闭容器中进行上述反应,测得
 随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
| A.压缩体积 | B.增大体积 | C.升高温度 | D.加入催化剂 |
您最近半年使用:0次
2023-08-20更新
|
303次组卷
|
2卷引用:福建省宁德市部分一级达标中学2022-2023学年高二上学期11月期中考试化学(C卷)试题
名校
解题方法
7 . 已知反应:
反应①: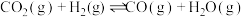
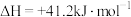
反应②: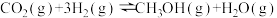
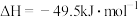
反应③:
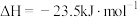
在2 MPa,起始投料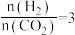 时,CO2的平衡转化率及CH3OCH3和CH3OH的平衡体积分数随温度变化如图-1所示。
时,CO2的平衡转化率及CH3OCH3和CH3OH的平衡体积分数随温度变化如图-1所示。

(1)①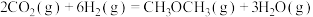 ΔH=
ΔH=___________
②从453-553℃,升高温度CO2平衡转化率降低的原因是___________ 。
③为提高单位时间内CH3OCH3产率。研发的催化剂需具备的特点是___________ 。
(2)在催化剂作用下,二甲醚还原NO的反应原理为 ΔH<0。在有氧和无氧的环境下,NO的去除率随温度变化如图-2所示。
ΔH<0。在有氧和无氧的环境下,NO的去除率随温度变化如图-2所示。
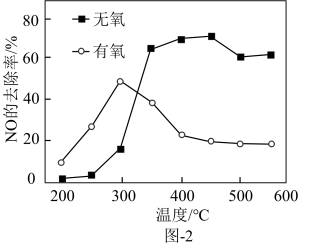
①无氧环境下,在250~450℃范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是___________ 。
②温度高于400℃时,NO去除率明显低于无氧环境的可能原因有___________ 。
反应①:
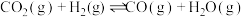
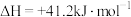
反应②:
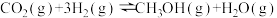
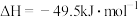
反应③:

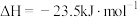
在2 MPa,起始投料
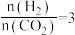 时,CO2的平衡转化率及CH3OCH3和CH3OH的平衡体积分数随温度变化如图-1所示。
时,CO2的平衡转化率及CH3OCH3和CH3OH的平衡体积分数随温度变化如图-1所示。
(1)①
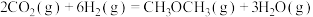 ΔH=
ΔH=②从453-553℃,升高温度CO2平衡转化率降低的原因是
③为提高单位时间内CH3OCH3产率。研发的催化剂需具备的特点是
(2)在催化剂作用下,二甲醚还原NO的反应原理为
 ΔH<0。在有氧和无氧的环境下,NO的去除率随温度变化如图-2所示。
ΔH<0。在有氧和无氧的环境下,NO的去除率随温度变化如图-2所示。
①无氧环境下,在250~450℃范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是
②温度高于400℃时,NO去除率明显低于无氧环境的可能原因有
您最近半年使用:0次
名校
解题方法
8 . 可逆反应aA(g)+bB(s) cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是

 cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
| A.使用催化剂C的物质的量分数增加 |
| B.已知T2>T1,升高温度能提高A的转化率 |
| C.已知p2>p1,则化学计量数:a<c+d |
| D.若该反应在恒容中进行,通入氦气(不参与反应),使压强增大,将加快该反应的速率 |
您最近半年使用:0次
名校
解题方法
9 .  在化工生产中有重要作用.天然气法合成
在化工生产中有重要作用.天然气法合成 相关反应如下:
相关反应如下:
反应I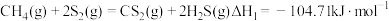
反应Ⅱ
(1) 、
、 随温度变化不大。温度不同时,反应体系中
随温度变化不大。温度不同时,反应体系中 不同。合成
不同。合成 总反应
总反应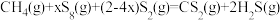 的
的 随温度T变化如图。
随温度T变化如图。
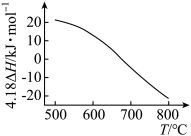
①

________  。
。
②为提高 平衡转化率,控制温度范围在
平衡转化率,控制温度范围在________ (填标号),理由是________ 。
A.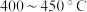 B.
B.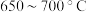 C.
C.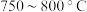 D.
D. 以上
以上
(2)合成 总反应中硫蒸气达到饱和时,反应时间t与
总反应中硫蒸气达到饱和时,反应时间t与 初始浓度
初始浓度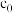 和
和 转化率
转化率 满足关系
满足关系 ,式中k为速率常数。
,式中k为速率常数。
① 、
、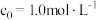 时,测得
时,测得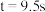 、
、 ,则
,则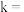
________ 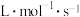 。
。
② 时,计划在
时,计划在 内转化率达
内转化率达 ,应控制初始浓度
,应控制初始浓度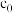 大于
大于________  。
。
(3)利用工业废气 替代硫磺矿生产
替代硫磺矿生产 的反应为
的反应为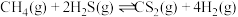 。反应物投料比采用
。反应物投料比采用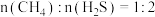 ,维持体系压强为
,维持体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
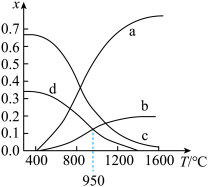
①图中表示 的曲线是
的曲线是________ (填“a”“b”“c”或“d”)。
② 时,该反应的
时,该反应的
________ (以分压表示,分压 总压
总压 物质的量分数)。
物质的量分数)。
③相比以硫磺矿为原料,使用 的优点是
的优点是________ ,缺点是________ 。
 在化工生产中有重要作用.天然气法合成
在化工生产中有重要作用.天然气法合成 相关反应如下:
相关反应如下:反应I
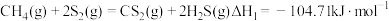
反应Ⅱ

(1)
 、
、 随温度变化不大。温度不同时,反应体系中
随温度变化不大。温度不同时,反应体系中 不同。合成
不同。合成 总反应
总反应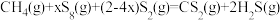 的
的 随温度T变化如图。
随温度T变化如图。
①


 。
。②为提高
 平衡转化率,控制温度范围在
平衡转化率,控制温度范围在A.
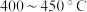 B.
B.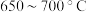 C.
C.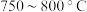 D.
D. 以上
以上(2)合成
 总反应中硫蒸气达到饱和时,反应时间t与
总反应中硫蒸气达到饱和时,反应时间t与 初始浓度
初始浓度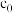 和
和 转化率
转化率 满足关系
满足关系 ,式中k为速率常数。
,式中k为速率常数。①
 、
、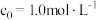 时,测得
时,测得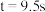 、
、 ,则
,则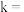
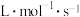 。
。②
 时,计划在
时,计划在 内转化率达
内转化率达 ,应控制初始浓度
,应控制初始浓度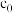 大于
大于 。
。(3)利用工业废气
 替代硫磺矿生产
替代硫磺矿生产 的反应为
的反应为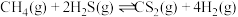 。反应物投料比采用
。反应物投料比采用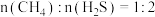 ,维持体系压强为
,维持体系压强为 ,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
,反应达到平衡时,四种组分的物质的量分数x随温度T的变化如图。
①图中表示
 的曲线是
的曲线是②
 时,该反应的
时,该反应的
 总压
总压 物质的量分数)。
物质的量分数)。③相比以硫磺矿为原料,使用
 的优点是
的优点是
您最近半年使用:0次
2023-03-08更新
|
877次组卷
|
3卷引用:福建省厦门市2023届高三毕业班3月第二次质量检测化学试题
名校
解题方法
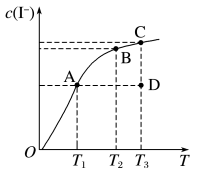
10 .  在KI溶液中存在下列平衡:
在KI溶液中存在下列平衡:
 。某
。某 、KI混合溶液中,
、KI混合溶液中, 的物质的量浓度
的物质的量浓度 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
 在KI溶液中存在下列平衡:
在KI溶液中存在下列平衡:
 。某
。某 、KI混合溶液中,
、KI混合溶液中, 的物质的量浓度
的物质的量浓度 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
A.该反应 |
B.若在 、 、 温度下,反应的平衡常数分别为 温度下,反应的平衡常数分别为 、 、 ,则 ,则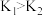 |
C.若反应进行到状态D时,一定有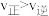 |
D.状态A与状态B相比,状态A的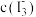 大 大 |
您最近半年使用:0次
2022-11-27更新
|
262次组卷
|
9卷引用:【全国百强校】福建省厦门市双十中学2018-2019学年高二下学期第一次月考化学试题
【全国百强校】福建省厦门市双十中学2018-2019学年高二下学期第一次月考化学试题【市级联考】山东省烟台市2019届高三上学期期末考试化学试题黑龙江省牡丹江市东宁市第一中学2020-2021学年高二上学期第一次月考化学试题河北省衡水市第十四中学2020-2021学年高二上学期三调考试(校内)化学试题黑龙江省实验中学2021-2022学年高二上学期期中考试化学试题黑龙江省哈尔滨市第二十四中学2022-2023学年高二10月月考化学试题四川省成都市树德中学2022-2023学年高二上学期11月阶段性测试化学试题吉林省延边第二中学2022-2023学年高二上学期期末考试化学试题新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题



