1 . 为探究外界条件对反应: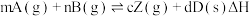 的影响,以A和B物质的量之比为
的影响,以A和B物质的量之比为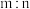 开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
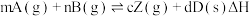 的影响,以A和B物质的量之比为
的影响,以A和B物质的量之比为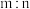 开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
开始反应,通过实验得到不同条件下达到平衡时Z的物质的量分数,实验结果如图所示。下列判断正确的是
| A.在恒温恒容条件下,向已达到平衡的体系中加入少量A,平衡正向移动,A的百分含量减小 |
B.降低温度, 比 比 减少更多 减少更多 |
| C.不断增加A的投料量,Z的体积分数可能减少 |
D.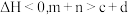 |
您最近半年使用:0次
名校
解题方法
2 . 下列图示与对应的叙述相符的是
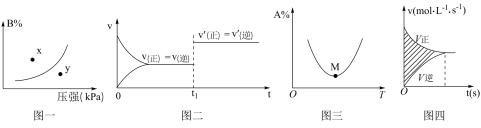

A.图一表示反应:  ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 |
B.图二是可逆反应  的速率时间图像,在 的速率时间图像,在 时刻改变条件一定是加入催化剂 时刻改变条件一定是加入催化剂 |
C.图三表示对于化学反应 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 |
D.图四所示图中的阴影部分面积的含义是( ) ) |
您最近半年使用:0次
2023-10-10更新
|
447次组卷
|
4卷引用:福建省南安市华侨中学2023-2024学年高二上学期10月月考化学试题
3 . 二甲醚是一种重要的清洁燃料,工业上可以通过 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。
Ⅰ. 分子间脱水制二甲醚
分子间脱水制二甲醚

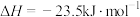 。在
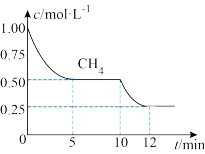
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
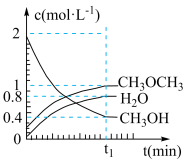
(1) 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡_____ (填“向右”、“向左”或“不发生”)移动,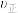 将
将_____ (填“增大”或“减小”)
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为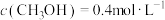 、
、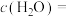
 、
、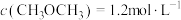 ,此时
,此时
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
Ⅱ.合成气制取二甲醚的原理如下:
反应1:
反应2:
(3)500K时,在2L密闭容器中充入4molCO和8mol ,4min达到平衡,平衡时CO的转化率为80%,且
,4min达到平衡,平衡时CO的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率
_____ ,反应1的平衡常数
_____ (结果需化成最简比)。
(4)由天然气获得合成气过程中可能发生以下反应:

在一密闭容器中进行上述反应,测得 随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。Ⅰ.
 分子间脱水制二甲醚
分子间脱水制二甲醚
 。在
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。 
(1)
 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡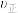 将
将(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为
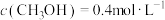 、
、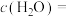
 、
、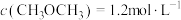 ,此时
,此时
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。Ⅱ.合成气制取二甲醚的原理如下:
反应1:

反应2:

(3)500K时,在2L密闭容器中充入4molCO和8mol
 ,4min达到平衡,平衡时CO的转化率为80%,且
,4min达到平衡,平衡时CO的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率

(4)由天然气获得合成气过程中可能发生以下反应:

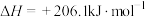
在一密闭容器中进行上述反应,测得
 随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
| A.压缩体积 | B.增大体积 | C.升高温度 | D.加入催化剂 |
您最近半年使用:0次
2023-08-20更新
|
303次组卷
|
2卷引用:福建省宁德市部分一级达标中学2022-2023学年高二上学期11月期中考试化学(C卷)试题
名校
解题方法
4 . 已知反应:
反应①: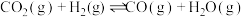
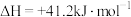
反应②: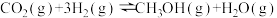
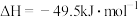
反应③:
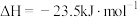
在2 MPa,起始投料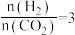 时,CO2的平衡转化率及CH3OCH3和CH3OH的平衡体积分数随温度变化如图-1所示。
时,CO2的平衡转化率及CH3OCH3和CH3OH的平衡体积分数随温度变化如图-1所示。

(1)①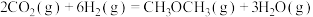 ΔH=
ΔH=___________
②从453-553℃,升高温度CO2平衡转化率降低的原因是___________ 。
③为提高单位时间内CH3OCH3产率。研发的催化剂需具备的特点是___________ 。
(2)在催化剂作用下,二甲醚还原NO的反应原理为 ΔH<0。在有氧和无氧的环境下,NO的去除率随温度变化如图-2所示。
ΔH<0。在有氧和无氧的环境下,NO的去除率随温度变化如图-2所示。
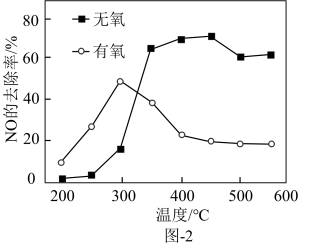
①无氧环境下,在250~450℃范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是___________ 。
②温度高于400℃时,NO去除率明显低于无氧环境的可能原因有___________ 。
反应①:
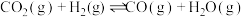
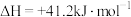
反应②:
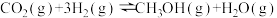
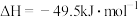
反应③:

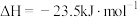
在2 MPa,起始投料
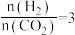 时,CO2的平衡转化率及CH3OCH3和CH3OH的平衡体积分数随温度变化如图-1所示。
时,CO2的平衡转化率及CH3OCH3和CH3OH的平衡体积分数随温度变化如图-1所示。
(1)①
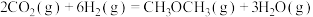 ΔH=
ΔH=②从453-553℃,升高温度CO2平衡转化率降低的原因是
③为提高单位时间内CH3OCH3产率。研发的催化剂需具备的特点是
(2)在催化剂作用下,二甲醚还原NO的反应原理为
 ΔH<0。在有氧和无氧的环境下,NO的去除率随温度变化如图-2所示。
ΔH<0。在有氧和无氧的环境下,NO的去除率随温度变化如图-2所示。
①无氧环境下,在250~450℃范围内随着温度的升高,NO的去除率先迅速上升后上升缓慢的主要原因是
②温度高于400℃时,NO去除率明显低于无氧环境的可能原因有
您最近半年使用:0次
名校
解题方法
5 . 可逆反应aA(g)+bB(s) cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是

 cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
| A.使用催化剂C的物质的量分数增加 |
| B.已知T2>T1,升高温度能提高A的转化率 |
| C.已知p2>p1,则化学计量数:a<c+d |
| D.若该反应在恒容中进行,通入氦气(不参与反应),使压强增大,将加快该反应的速率 |
您最近半年使用:0次
名校
解题方法
6 .  在KI溶液中存在下列平衡:
在KI溶液中存在下列平衡:
 。某
。某 、KI混合溶液中,
、KI混合溶液中, 的物质的量浓度
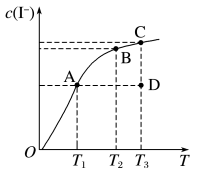
的物质的量浓度 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
 在KI溶液中存在下列平衡:
在KI溶液中存在下列平衡:
 。某
。某 、KI混合溶液中,
、KI混合溶液中, 的物质的量浓度
的物质的量浓度 与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
与温度T的关系如图所示(曲线上任何一点都表示平衡状态)。下列说法不正确的是
A.该反应 |
B.若在 、 、 温度下,反应的平衡常数分别为 温度下,反应的平衡常数分别为 、 、 ,则 ,则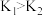 |
C.若反应进行到状态D时,一定有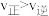 |
D.状态A与状态B相比,状态A的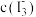 大 大 |
您最近半年使用:0次
2022-11-27更新
|
263次组卷
|
9卷引用:【全国百强校】福建省厦门市双十中学2018-2019学年高二下学期第一次月考化学试题
【全国百强校】福建省厦门市双十中学2018-2019学年高二下学期第一次月考化学试题【市级联考】山东省烟台市2019届高三上学期期末考试化学试题黑龙江省牡丹江市东宁市第一中学2020-2021学年高二上学期第一次月考化学试题河北省衡水市第十四中学2020-2021学年高二上学期三调考试(校内)化学试题黑龙江省实验中学2021-2022学年高二上学期期中考试化学试题黑龙江省哈尔滨市第二十四中学2022-2023学年高二10月月考化学试题四川省成都市树德中学2022-2023学年高二上学期11月阶段性测试化学试题吉林省延边第二中学2022-2023学年高二上学期期末考试化学试题新疆阿克苏市实验中学2022-2023学年高二上学期期末考试化学试题
名校
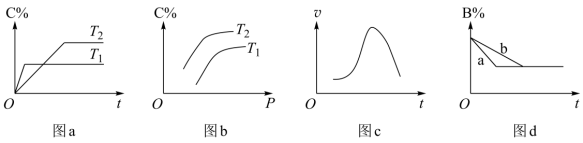
7 . 某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响,图像如图,下列判断正确的是
pC(g)的速率和平衡的影响,图像如图,下列判断正确的是
 pC(g)的速率和平衡的影响,图像如图,下列判断正确的是
pC(g)的速率和平衡的影响,图像如图,下列判断正确的是
| A.图d中,曲线a一定增加了催化剂 |
| B.图c是绝热条件下速率和时间的图像,由此说明该反应吸热 |
| C.由图b可知,该反应m+n<p |
| D.由图a可知,T1>T2,该反应的逆反应为吸热反应 |
您最近半年使用:0次
2022-11-08更新
|
153次组卷
|
2卷引用:福建省南平市高级中学2022-2023学年高二上学期期中考试化学(选考)试题
8 . I.据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
二氧化碳重整:CH4(g)+CO2(g) 2CO(g)+2H2(g) △H3③
2CO(g)+2H2(g) △H3③
则反应①自发进行的条件是____ ,△H3=____ kJ·mol-1。
II.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氮的体积分数(φ)如图所示。
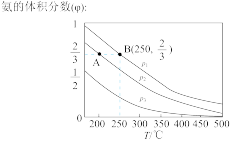
①其中,p1、p2和p3由大到小的顺序是____ ,其原因是____ 。
②若分别用VA(N2)和VB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则VA(N2)____ VB(N2)(填“>”“<”或“=”)。
③若在250℃、p1为104Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为_____ Pa(分压=总压×物质的量分效,保留一位小数)。
III.以连二硫酸根(S2O )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
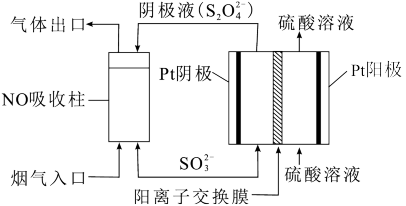
(3)①阴极区的电极反应式为____ 。
②NO吸收转化后的主要产物为NH ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为____ mL。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+3H2(g) △H1=+205.9kJ·mol-1①CO(g)+H2O(g)
 CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
CO2(g)+H2(g) △H2=-41.2kJ·mol-1②二氧化碳重整:CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H3③
2CO(g)+2H2(g) △H3③则反应①自发进行的条件是
II.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2(g)+3H2(g)
 2NH3(g)。
2NH3(g)。(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氮的体积分数(φ)如图所示。

①其中,p1、p2和p3由大到小的顺序是
②若分别用VA(N2)和VB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则VA(N2)
③若在250℃、p1为104Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为
III.以连二硫酸根(S2O
 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
(3)①阴极区的电极反应式为
②NO吸收转化后的主要产物为NH
 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
您最近半年使用:0次
2022-09-22更新
|
108次组卷
|
8卷引用:福建泉州实验中学2021-2022学年高三上学期12月月考化学试题
福建泉州实验中学2021-2022学年高三上学期12月月考化学试题福建省宁德第一中学2022-2023学年高二上学期第二次月考化学试题广东省揭阳市2018高三高考第一次模拟考试理综化学试题云南省昆明市寻甸一中2020届高三第一次全真模拟考试理综化学试题甘肃省高台县第一中学2020届高三上学期期中考试化学试题山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题(已下线)一轮巩固卷10-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习
名校
9 . 给定物质A、B、C的量,在一定条件下发生反应,建立如下化学平衡: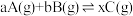 ,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
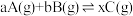 ,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指
,符合下图所示的关系(c%表示平衡混合气中产物C的百分含量。T表示温度,P表示压强)。在图中,Y轴是指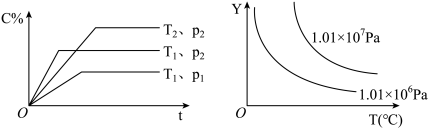
| A.反应物A的百分含量 | B.平衡混合气的总物质的量 | C.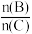 比值 比值 | D.反应物B的平衡转化率 |
您最近半年使用:0次
2022-09-13更新
|
673次组卷
|
4卷引用:福建省厦门第一中学2020-2021学年高二上学期期中考试化学试题
名校
解题方法
10 . 在密闭容器中进行反应: ,下列说法错误的是
,下列说法错误的是
 ,下列说法错误的是
,下列说法错误的是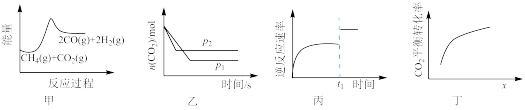
| A.由图甲可知,该反应为吸热反应 |
B.由图乙可知,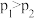 |
C.由图丙可知, 时刻改变的条件可能是加入了催化剂 时刻改变的条件可能是加入了催化剂 |
D.由图丁可知,横坐标 可能是指投料比 可能是指投料比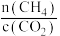 |
您最近半年使用:0次
2022-09-03更新
|
646次组卷
|
10卷引用:福建省泉州市2021-2022学年高二上学期期末教学质量监测化学试题
福建省泉州市2021-2022学年高二上学期期末教学质量监测化学试题福建省三明第一中学2022-2023学年高二上学期中考试化学试题福建省福州市外国语学校2022-2023学年高二上学期12月阶段性测试化学试题福建省厦门外国语学校石狮分校2022-2023学年高二上学期期中考试化学试题福建省福州第三中学2023-2024学年高二上学期1月期末考试化学试题福建省莆田五中2023-2024学年高二上学期第三次月考化学试卷 河南省中原名校2022-2023学年高二上学期第二次联考化学试题广东省惠州市第一中学2022-2023学年高二上学期第一次月考化学试题陕西省榆林市绥德中学2022-2023学年高二上学期第二次阶段性考试化学试题山东省济南市莱钢高级中学2022-2023学年高二上学期期中考试化学试题



