1 . 二甲醚是一种重要的清洁燃料,工业上可以通过 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。
Ⅰ. 分子间脱水制二甲醚
分子间脱水制二甲醚

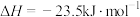 。在
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
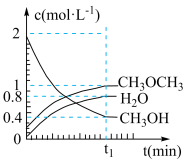
(1) 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡_____ (填“向右”、“向左”或“不发生”)移动, 将
将_____ (填“增大”或“减小”)
(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为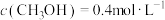 、
、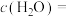
 、
、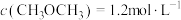 ,此时
,此时
_____  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
Ⅱ.合成气制取二甲醚的原理如下:
反应1:
反应2:
(3)500K时,在2L密闭容器中充入4molCO和8mol ,4min达到平衡,平衡时CO的转化率为80%,且
,4min达到平衡,平衡时CO的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率
_____ ,反应1的平衡常数
_____ (结果需化成最简比)。
(4)由天然气获得合成气过程中可能发生以下反应:

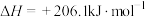
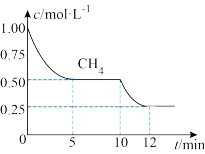
在一密闭容器中进行上述反应,测得 随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
 、合成气(主要成分是一氧化碳和氢气)制得。
、合成气(主要成分是一氧化碳和氢气)制得。Ⅰ.
 分子间脱水制二甲醚
分子间脱水制二甲醚
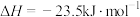 。在
。在 ℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。
℃,恒容密闭容器中建立上述平衡,体系中各组分浓度随时间变化如图所示。 
(1)
 时刻反应达平衡后,其他条件不变,升高温度,平衡
时刻反应达平衡后,其他条件不变,升高温度,平衡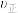 将
将(2)相同条件下,若改变起始浓度,某时刻各组分浓度依次为
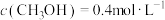 、
、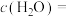
 、
、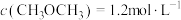 ,此时
,此时
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。Ⅱ.合成气制取二甲醚的原理如下:
反应1:

反应2:

(3)500K时,在2L密闭容器中充入4molCO和8mol
 ,4min达到平衡,平衡时CO的转化率为80%,且
,4min达到平衡,平衡时CO的转化率为80%,且 ,则反应2中
,则反应2中 的转化率
的转化率

(4)由天然气获得合成气过程中可能发生以下反应:

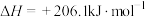
在一密闭容器中进行上述反应,测得
 随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
随反应时间的变化如图所示,10min时,改变的外界条件可能是_____(填代号)
| A.压缩体积 | B.增大体积 | C.升高温度 | D.加入催化剂 |
您最近半年使用:0次
2023-08-20更新
|
303次组卷
|
2卷引用:福建省宁德市部分一级达标中学2022-2023学年高二上学期11月期中考试化学(C卷)试题
名校
解题方法
2 . 可逆反应aA(g)+bB(s) cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是

 cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(p)的关系如图所示,其中正确的是
| A.使用催化剂C的物质的量分数增加 |
| B.已知T2>T1,升高温度能提高A的转化率 |
| C.已知p2>p1,则化学计量数:a<c+d |
| D.若该反应在恒容中进行,通入氦气(不参与反应),使压强增大,将加快该反应的速率 |
您最近半年使用:0次
3 . I.据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g) CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+H2O(g) CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
二氧化碳重整:CH4(g)+CO2(g) 2CO(g)+2H2(g) △H3③
2CO(g)+2H2(g) △H3③
则反应①自发进行的条件是____ ,△H3=____ kJ·mol-1。
II.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2(g)+3H2(g) 2NH3(g)。
2NH3(g)。
(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氮的体积分数(φ)如图所示。
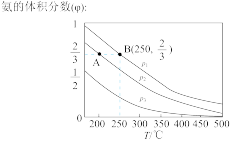
①其中,p1、p2和p3由大到小的顺序是____ ,其原因是____ 。
②若分别用VA(N2)和VB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则VA(N2)____ VB(N2)(填“>”“<”或“=”)。
③若在250℃、p1为104Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为_____ Pa(分压=总压×物质的量分效,保留一位小数)。
III.以连二硫酸根(S2O )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
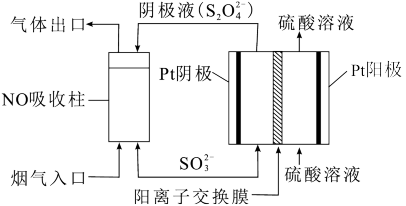
(3)①阴极区的电极反应式为____ 。
②NO吸收转化后的主要产物为NH ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为____ mL。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:CH4(g)+H2O(g)
 CO(g)+3H2(g) △H1=+205.9kJ·mol-1①
CO(g)+3H2(g) △H1=+205.9kJ·mol-1①CO(g)+H2O(g)
 CO2(g)+H2(g) △H2=-41.2kJ·mol-1②
CO2(g)+H2(g) △H2=-41.2kJ·mol-1②二氧化碳重整:CH4(g)+CO2(g)
 2CO(g)+2H2(g) △H3③
2CO(g)+2H2(g) △H3③则反应①自发进行的条件是
II.氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为N2(g)+3H2(g)
 2NH3(g)。
2NH3(g)。(2)在不同温度、压强和相同催化剂条件下,初始N2、H2分别为0.1mol、0.3mol时,平衡后混合物中氮的体积分数(φ)如图所示。

①其中,p1、p2和p3由大到小的顺序是
②若分别用VA(N2)和VB(N2)表示从反应开始至达平衡状态A、B时的化学反应速率,则VA(N2)
③若在250℃、p1为104Pa条件下,反应达到平衡时容器的体积为1L,则该条件下B点N2的分压p(N2)为
III.以连二硫酸根(S2O
 )为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
)为媒介,使用间接电化学法也可处理燃煤烟气中的NO,装置如图所示:
(3)①阴极区的电极反应式为
②NO吸收转化后的主要产物为NH
 ,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
,若通电时电路中转移了0.3mole-,则此通电过程中理论上吸收的NO在标况下的体积为
您最近半年使用:0次
2022-09-22更新
|
108次组卷
|
8卷引用:福建省宁德第一中学2022-2023学年高二上学期第二次月考化学试题
福建省宁德第一中学2022-2023学年高二上学期第二次月考化学试题广东省揭阳市2018高三高考第一次模拟考试理综化学试题云南省昆明市寻甸一中2020届高三第一次全真模拟考试理综化学试题甘肃省高台县第一中学2020届高三上学期期中考试化学试题山西省太原市第五中学2021-2022学年上学期高三第四次模块诊断化学试题(已下线)一轮巩固卷10-【赢在高考·黄金20卷】备战2022年高考化学模拟卷(全国卷专用)(已下线)专题12 化学反应原理综合题—2022年高考化学二轮复习讲练测(全国版)-练习福建泉州实验中学2021-2022学年高三上学期12月月考化学试题
名校
解题方法
4 . 碳酸钠作固硫剂并用氢还原辉钼矿的原理为MoS2(s)+4H2(g)+2Na2CO3(s) Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。

(1)该反应的平衡常数表达式为K=___ 。
(2)由图1可知,该反应ΔH__ 0(填“>”或“<”),p1、p2、p3由大到小的顺序为___ 。
(3)由图2可知,A点时H2的平衡转化率为___ 。
 Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。
(1)该反应的平衡常数表达式为K=
(2)由图1可知,该反应ΔH
(3)由图2可知,A点时H2的平衡转化率为
您最近半年使用:0次
2020-05-16更新
|
108次组卷
|
2卷引用:福建省宁德市2019-2020学年高二上学期期末考试化学试题
名校
解题方法
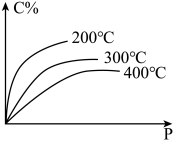
5 . 对于mA(s)+nB(g)⇌eC(g)+fD(g),反应过程中,当其它条件不变时,C的百分含量(C%)和压强(P)的关系如图,下列叙述正确的是

| A.化学方程式中n<e+f |
| B.达到平衡后,若升温,平衡逆向移动 |
| C.达到平衡后,加入催化剂,则C%增大 |
| D.达到平衡后,增加A的量,平衡正向移动 |
您最近半年使用:0次
2020-02-17更新
|
283次组卷
|
14卷引用:福建省霞浦第一中学2018-2019学年高二下学期第一次月考化学试题
福建省霞浦第一中学2018-2019学年高二下学期第一次月考化学试题(已下线)2010年福建省福州八中高二第二学期期末考试化学试题2015-2016学年河南省信阳高中高二上学期第一次月考化学试卷2015-2016学年辽宁省实验中学分校高一下学期6月月考化学试卷安徽省合肥市第九中学2018-2019学年高二上学期期中考试化学试题【全国百强校】福建省厦门市双十中学2018-2019学年高二下学期第一次月考化学试题安徽省郎溪中学2018-2019学年高二下学期第一次月考化学试题2020届高三化学知识点强化训练—化学平衡的移动及影响因素广东省广州市第八十九中学2020-2021学年高二上学期期中考试化学试题湖南省临澧县第一中学2020-2021学年高二上学期期中考试化学试题(选考)重庆市渝西中学2020-2021学年高二上学期第一次月考化学试题湖南省临澧县第一中学2020-2021学年高二下学期阶段性考试(二)化学试题上海市上海交通大学附属中学2022-2023学年高二上学期期中考试化学试题上海市延安中学2023-2024学年高二上学期期中考试(等级考)化学试题
名校
解题方法
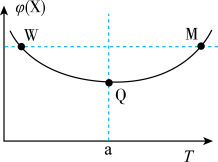
6 . 在某2 L恒容密闭容器中充入2 mol X(g)和1mol Y(g)发生反应:2X(g)+ Y(g) 3Z(g) △H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是
3Z(g) △H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是
 3Z(g) △H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是
3Z(g) △H,反应过程中持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示:下列推断正确的是
| A.Q点时,Y的转化率最大 |
| B.升高温度,平衡常数增大 |
| C.W点Y的正反应速率等于M点Y的正反应速率 |
| D.平衡时充入Y,达到新平衡时Y的体积分数比原平衡时小 |
您最近半年使用:0次
2019-12-18更新
|
84次组卷
|
3卷引用:福建省宁德市高中同心顺联盟校2019-2020学年高二上学期期中考试化学试题
福建省宁德市高中同心顺联盟校2019-2020学年高二上学期期中考试化学试题福建省南安第一中学2019-2020学年高二上学期第二次月考化学(选考)试题(已下线)2019年12月28日 《每日一题》人教版(选修4)——周末培优
7 . T℃时,在1L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的浓度变化如图1所示;若保持其他条件不变,温度分别为T1和T2时,Y的体积百分含量与时间的关系如图2所示。则下列结论正确的是( )


A.容器中发生的反应可表示为:X(g)+Y(g)  Z(g) Z(g) |
| B.保持其他条件不变,升高温度,反应的化学平衡常数K减小 |
| C.反应进行的前3 min内,用X表示的反应速率 v(Z)=0.4mol/(L·min) |
| D.反应达到平衡后,增大压强,Z的体积分数增大 |
您最近半年使用:0次
名校
8 . 对于可逆反应mA(g)+nB(g)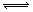 pC(s)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与温度T或压强P的关系如图所示,请判断下列说法正确的是
pC(s)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与温度T或压强P的关系如图所示,请判断下列说法正确的是
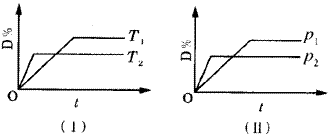
 pC(s)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与温度T或压强P的关系如图所示,请判断下列说法正确的是
pC(s)+qD(g)反应过程中,其他条件不变时,产物D的质量分数D%与温度T或压强P的关系如图所示,请判断下列说法正确的是
| A.降温,化学平衡向正反应方向移动 |
| B.使用催化剂可使D%有所增加 |
| C.化学方程式中气体的化学计量数m+n>q |
| D.B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动 |
您最近半年使用:0次
2019-01-30更新
|
131次组卷
|
4卷引用:2015-2016学年福建省福安市高级中学高二上学期第一次月考化学试卷



