19. 甲醇(CH
3OH)是一种重要的化工原料,也是一种比较理想的燃料。甲醇在各个领域有着广泛的应用。
(1)实验测得:32 g甲醇在氧气中完全燃烧,生成二氧化碳气体和液态水时释放出726.4 kJ的热量,试写出甲醇燃烧的热化学方程式:
_________________________。
(2)燃料电池是一种连续地将燃料和氧化剂的化学能直接转换成电能的化学电池。下图是一个化学过程的示意图。2CH
3OH+3O
2+4KOH

K
2CO
3+6H
2O
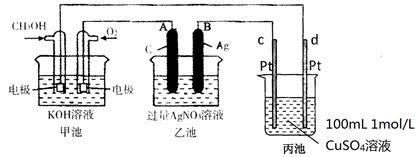
①A(石墨)电极的名称是
______________。
②通入O
2的电极的电极反应式是
________________③写出通入CH
3OH的电极的电极反应式是
________________。
④乙池中反应的化学方程式为
___________________。
⑤当电路中通过0.01mol电子时,丙池溶液的C(H
+) =
_________mol/L(忽略电解过程中溶液体积的变化)。
(3)合成甲醇的主要反应是:2H
2(g)+ CO(g)

CH
3OH(g) △H=—90.8 kJ·mol
—1。
①在恒温恒容条件下,充入一定量的H
2和CO,发生反应2H
2(g)+ CO(g)

CH
3OH(g)。则该反应达到平衡状态的标志有
____a.混合气体的密度保持不变
b.混合气体的总压强保持不变
c.CO的质量分数保持不变
d.甲醇的浓度保持不变
e.v
正(H
2)= v
逆(CH
3OH) f.v(CO)= v(CH
3OH)
②要提高反应2H
2(g)+ CO(g)

CH
3OH(g)中CO的转化率,可以采取的措施是
____:
a.升温
b.加入催化剂
c.增加CO的浓度 d.加入H
2e.加入惰性气体
f.分离出甲醇