1 . 乙烯是合成多种塑料的单体。我国科学家开发的特殊催化剂用 制备
制备 ,有利于实现“双碳”目标。
,有利于实现“双碳”目标。
主反应: 放热反应
放热反应
(1)在容积为2L的恒容密闭容器中充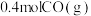 和
和 ,若只发生主反应,反应时间2.0min,
,若只发生主反应,反应时间2.0min, 的转化率为20%,在这段时间内
的转化率为20%,在这段时间内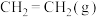 的平均反应速率为
的平均反应速率为___________ 。
(2)在一定温度下,向恒容密闭容器中充入 和
和 ,若只发生主反应,下列情况不能说明反应达到平衡的是
,若只发生主反应,下列情况不能说明反应达到平衡的是___________ (填编号)。
A.混合气体总压强保持不变 B.混合气体密度保持不变
C.乙烯体积分数保持不变 D.平均摩尔质量保持不变
达到平衡后能提高 平衡转化率的措施是
平衡转化率的措施是___________ (任填一条)。
(3)下列事实中,不能用勒夏特列原理解释的是_______。
(4)下图表示反应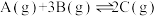 放热反应在某段时间
放热反应在某段时间 里的反应速率与反应过程的关系图,则C的百分含量最高的一段是_______。
里的反应速率与反应过程的关系图,则C的百分含量最高的一段是_______。
 制备
制备 ,有利于实现“双碳”目标。
,有利于实现“双碳”目标。主反应:
 放热反应
放热反应(1)在容积为2L的恒容密闭容器中充
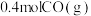 和
和 ,若只发生主反应,反应时间2.0min,
,若只发生主反应,反应时间2.0min, 的转化率为20%,在这段时间内
的转化率为20%,在这段时间内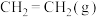 的平均反应速率为
的平均反应速率为(2)在一定温度下,向恒容密闭容器中充入
 和
和 ,若只发生主反应,下列情况不能说明反应达到平衡的是
,若只发生主反应,下列情况不能说明反应达到平衡的是A.混合气体总压强保持不变 B.混合气体密度保持不变
C.乙烯体积分数保持不变 D.平均摩尔质量保持不变
达到平衡后能提高
 平衡转化率的措施是
平衡转化率的措施是(3)下列事实中,不能用勒夏特列原理解释的是_______。
A.反应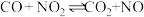 (放热反应),升高温度平衡向逆反应方向移动 (放热反应),升高温度平衡向逆反应方向移动 |
B.采用高压有利于合成氨反应: |
C.使用催化剂有利于合成氨反应: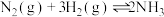 |
D.氯水中有下列平衡: ,当加入 ,当加入 溶液后溶液颜色变浅 溶液后溶液颜色变浅 |
(4)下图表示反应
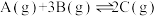 放热反应在某段时间
放热反应在某段时间 里的反应速率与反应过程的关系图,则C的百分含量最高的一段是_______。
里的反应速率与反应过程的关系图,则C的百分含量最高的一段是_______。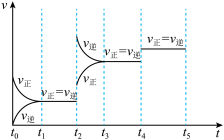
A. | B. | C. | D. |
您最近半年使用:0次
名校
解题方法
2 . 诺贝尔化学奖获得者GeorgeA.Olah 提出了“甲醇经济”的概念,他建议用甲醇来代替目前广泛使用的化石燃料。工业上用天然气为原料,分为两个阶段制备甲醇:
i.制备合成气:CH4(g)+H2O(g) CO(g)+3H2(g) ΔH= + 206.0 kJ·mol-1
CO(g)+3H2(g) ΔH= + 206.0 kJ·mol-1
ii.合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH= - 90.67kJ·mol-1
CH3OH(g) ΔH= - 90.67kJ·mol-1
(焓变 ΔH>0:反应吸热;ΔH<0:反应放热) 回答下列问题:
(1)制备合成气反应中,平衡混合物中 CO 的体积分数与压强的关系如图 1 所示,判断T1和T2的大小关系:T1___________ T2(填“<”或“=”),理由是___________ 。

(2)工业生产中为解决合成气中 H2过量而 CO 不足的问题,原料气中需添加 CO2,发生反应CO2(g)+H2(g) CO(g)+H2O(g) ΔH= + 41.17kJ·mol-1。为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳的体积比为
CO(g)+H2O(g) ΔH= + 41.17kJ·mol-1。为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳的体积比为___________ 。
(3)在体积不变的密闭容器中投入 0.5mol CO 和 1mol H2,不同条件下发生反应:CO(g)+2H2(g) CH3OH(g)。实验测得平衡时H2的转化率随温度、压强的变化如图 2 所示。
CH3OH(g)。实验测得平衡时H2的转化率随温度、压强的变化如图 2 所示。

①图 2 中 X 代表___________ (填“温度”或“压强”)。图 3 中正确表示该反应的平衡常数的负对数pK(pK=-lgK)与X 的关系的曲线___________ (填“AC”或“AB”)。
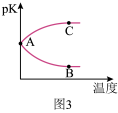
②若图 2 中M 点对应的容器体积为 5L,则N 点的平衡常数K 为___________ 。
(4)通过光催化、光电催化或电水制氢来进行二氧化碳加氢制甲醇(CH3OH),发生的主要反应是:CO2(g)+3H2(g) CH3OH(g)+H2O(g)。若二氧化碳加氢制甲醇的反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到 t1时刻达到平衡状态的是
CH3OH(g)+H2O(g)。若二氧化碳加氢制甲醇的反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到 t1时刻达到平衡状态的是___________ (填标号)。
a.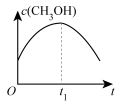 b.
b.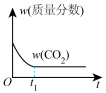
c.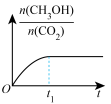 d.
d.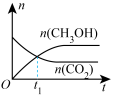
i.制备合成气:CH4(g)+H2O(g)
 CO(g)+3H2(g) ΔH= + 206.0 kJ·mol-1
CO(g)+3H2(g) ΔH= + 206.0 kJ·mol-1ii.合成甲醇:CO(g)+2H2(g)
 CH3OH(g) ΔH= - 90.67kJ·mol-1
CH3OH(g) ΔH= - 90.67kJ·mol-1(焓变 ΔH>0:反应吸热;ΔH<0:反应放热) 回答下列问题:
(1)制备合成气反应中,平衡混合物中 CO 的体积分数与压强的关系如图 1 所示,判断T1和T2的大小关系:T1

(2)工业生产中为解决合成气中 H2过量而 CO 不足的问题,原料气中需添加 CO2,发生反应CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH= + 41.17kJ·mol-1。为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳的体积比为
CO(g)+H2O(g) ΔH= + 41.17kJ·mol-1。为了使合成气配比最佳,理论上原料气中甲烷与二氧化碳的体积比为(3)在体积不变的密闭容器中投入 0.5mol CO 和 1mol H2,不同条件下发生反应:CO(g)+2H2(g)
 CH3OH(g)。实验测得平衡时H2的转化率随温度、压强的变化如图 2 所示。
CH3OH(g)。实验测得平衡时H2的转化率随温度、压强的变化如图 2 所示。
①图 2 中 X 代表

②若图 2 中M 点对应的容器体积为 5L,则N 点的平衡常数K 为
(4)通过光催化、光电催化或电水制氢来进行二氧化碳加氢制甲醇(CH3OH),发生的主要反应是:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)。若二氧化碳加氢制甲醇的反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到 t1时刻达到平衡状态的是
CH3OH(g)+H2O(g)。若二氧化碳加氢制甲醇的反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明该反应进行到 t1时刻达到平衡状态的是a.
 b.
b.
c.
 d.
d.
您最近半年使用:0次
名校
解题方法
3 . 在体积为 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应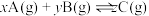 ,图1表示
,图1表示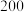 ℃时容器中
℃时容器中 、
、 、
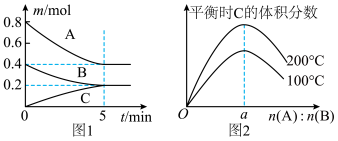
、 物质的量随时间的变化关系,图2表示不同温度下平衡时
物质的量随时间的变化关系,图2表示不同温度下平衡时 的体积分数随起始
的体积分数随起始 的变化关系。则下列结论正确的是
的变化关系。则下列结论正确的是
 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应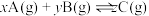 ,图1表示
,图1表示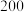 ℃时容器中
℃时容器中 、
、 、
、 物质的量随时间的变化关系,图2表示不同温度下平衡时
物质的量随时间的变化关系,图2表示不同温度下平衡时 的体积分数随起始
的体积分数随起始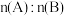 的变化关系。则下列结论正确的是
的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率 |
B.由图2可知反应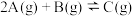 ,正反应吸热且a=2 ,正反应吸热且a=2 |
C.若在图1所示的平衡状态下再向体系中充入 和 和 ,此时 ,此时 |
D.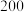 ℃时,向空容器中充入 ℃时,向空容器中充入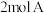 和 和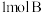 ,达到平衡时 ,达到平衡时 的体积分数小于0.5 的体积分数小于0.5 |
您最近半年使用:0次
2023-04-27更新
|
317次组卷
|
7卷引用:上海市实验学校2021-2022学年高三下学期3月月考化学试题
上海市实验学校2021-2022学年高三下学期3月月考化学试题上海市建平中学2023届高三下学期3月月考化学试题(已下线)卷11 化学反应速率和平衡选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)湖南省常德市澧县一中2021-2022学年高三下学期期中考试化学试题湖南省常德市澧县第一中学2021-2022学年高三下学期期中考试化学试题湖南省衡阳县2023届高三3月教学质量诊断性检测考试化学试题山西省实验中学2023-2024学年高二上学期第一次月考化学试题
名校
解题方法
4 . 脱除烟气中的 、NO有以下几种方法。
、NO有以下几种方法。
I. 催化还原NO,原理如下:
催化还原NO,原理如下:
①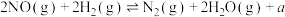 kJ
kJ
②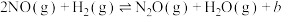 kJ
kJ
(1)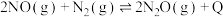 kJ。用含a、b的表达式表示
kJ。用含a、b的表达式表示
___________ 。
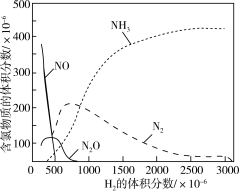
(2)某温度下反应达到平衡, 的初始体积分数对
的初始体积分数对 还原NO反应的影响如图所示。
还原NO反应的影响如图所示。 催化还原NO的主反应是上述反应中的
催化还原NO的主反应是上述反应中的___________ (选填“①”或“②”),当 初始体积分数大于
初始体积分数大于 时,
时, 的体积分数呈下降趋势的原因是
的体积分数呈下降趋势的原因是___________ 。
Ⅱ.碱性溶液吸收
(3)工业上用氨水吸收 ,生成的正盐溶液呈弱碱性的原因是
,生成的正盐溶液呈弱碱性的原因是___________ 。
Ⅲ.尿素 溶液吸收
溶液吸收 、NO。
、NO。
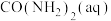 吸收含
吸收含 、NO的烟气时通入少量
、NO的烟气时通入少量 可同时实现脱硫、脱硝。脱硝的总反应为
可同时实现脱硫、脱硝。脱硝的总反应为 (未配平)。
(未配平)。
(4)脱硝反应分为两步。第一步的化学方程式为___________ ;第二步: 和
和 反应生成
反应生成 和
和 。
。
(5)将含 、NO的烟气以一定的流速通过10%的
、NO的烟气以一定的流速通过10%的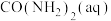 ,其他条件不变,不通
,其他条件不变,不通 和通少量
和通少量 时,
时, 的去除率如下表:
的去除率如下表:
用电离平衡移动原理解释通入少量的 使
使 去除率降低的原因
去除率降低的原因___________ 。
 、NO有以下几种方法。
、NO有以下几种方法。I.
 催化还原NO,原理如下:
催化还原NO,原理如下:①
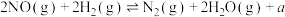 kJ
kJ②
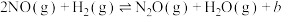 kJ
kJ(1)
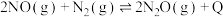 kJ。用含a、b的表达式表示
kJ。用含a、b的表达式表示
(2)某温度下反应达到平衡,
 的初始体积分数对
的初始体积分数对 还原NO反应的影响如图所示。
还原NO反应的影响如图所示。 催化还原NO的主反应是上述反应中的
催化还原NO的主反应是上述反应中的 初始体积分数大于
初始体积分数大于 时,
时, 的体积分数呈下降趋势的原因是
的体积分数呈下降趋势的原因是
Ⅱ.碱性溶液吸收

(3)工业上用氨水吸收
 ,生成的正盐溶液呈弱碱性的原因是
,生成的正盐溶液呈弱碱性的原因是Ⅲ.尿素
 溶液吸收
溶液吸收 、NO。
、NO。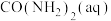 吸收含
吸收含 、NO的烟气时通入少量
、NO的烟气时通入少量 可同时实现脱硫、脱硝。脱硝的总反应为
可同时实现脱硫、脱硝。脱硝的总反应为 (未配平)。
(未配平)。(4)脱硝反应分为两步。第一步的化学方程式为
 和
和 反应生成
反应生成 和
和 。
。(5)将含
 、NO的烟气以一定的流速通过10%的
、NO的烟气以一定的流速通过10%的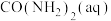 ,其他条件不变,不通
,其他条件不变,不通 和通少量
和通少量 时,
时, 的去除率如下表:
的去除率如下表:不通 | 通少量 | |
 的去除率 的去除率 | >80% | <80% |
 使
使 去除率降低的原因
去除率降低的原因
您最近半年使用:0次
名校
解题方法
5 . (一)2021年度中国科学十大进展之一就是人工淀粉合成途径的研究,其关键步骤之一就是利用CO2合成出有机小分子。这将有利于我国实现碳达峰碳中和,有利于建设友好型社会。如CO2可与H2生成CH4:CO2(g)+4H2(g) CH4(g)+2H2O(g)。
CH4(g)+2H2O(g)。
(1)写出该反应的平衡常数表达式K=_______ 。
(2)在恒温(T>100℃)恒容装置中进行该反应,能判断反应已达平衡状态的是_______。
(3)将1mol CO2和4mol H2置于体积为2L的密闭容器中发生反应,测得H2O(g)的物质的量分数与温度的关系如图所示,该反应的平衡常数K随温度升高而_______ (填“增大”或“减小”)。
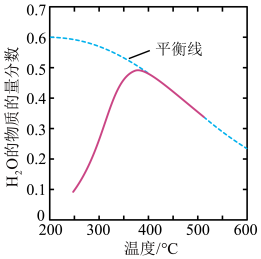
(4)下列措施有利于提高反应中CO2的平衡转化率的是_______。
(二)我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下:
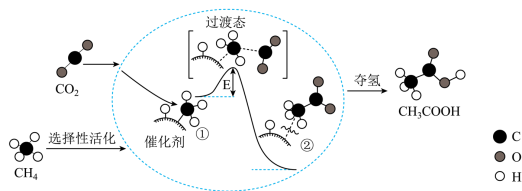
(5)①、②与过滤态三种物质中,最不稳定的是_______ ;①转化为②过程中_______ (选填“吸收”或“放出”)能量。
(6)25℃时,100kPa下,CH4(g)、CH3COOH(l)的燃烧热分别-893kJ·mol-1、-870kJ·mol-1,计算转化反应CO2(g)+CH4(g)=CH3COOH(l)的焓变
_______ kJ·mol-1。该转化反应的熵变
_______ 0(填“>”“<”或“=”),对该转化反应自发性的判断正确的是_______ (单选)。
A. 高温下自发 B. 低温下自发 C. 始终自发 D. 始终不自发
 CH4(g)+2H2O(g)。
CH4(g)+2H2O(g)。(1)写出该反应的平衡常数表达式K=
(2)在恒温(T>100℃)恒容装置中进行该反应,能判断反应已达平衡状态的是_______。
| A.混合气体密度不再改变 | B.混合气体压强不再改变 |
| C.混合气体平均摩尔质量不再改变 | D.n(CO2):n(H2)=1:4 |

(4)下列措施有利于提高反应中CO2的平衡转化率的是_______。
| A.使用催化剂 | B.加压 |
| C.升高温度 | D.增大初始投料比n(CO2)/n(H2) |
(二)我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下:

(5)①、②与过滤态三种物质中,最不稳定的是
(6)25℃时,100kPa下,CH4(g)、CH3COOH(l)的燃烧热分别-893kJ·mol-1、-870kJ·mol-1,计算转化反应CO2(g)+CH4(g)=CH3COOH(l)的焓变


A. 高温下自发 B. 低温下自发 C. 始终自发 D. 始终不自发
您最近半年使用:0次
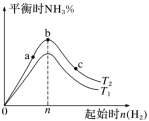
6 . 已知合成氨反应3H2(g)+N2(g) 2NH3(g)+QkJ(Q>0)。某科研小组研究:在其他条件不变的情况下,改变起始时氢气的物质的量对合成NH3反应的影响。实验结果如图所示:(图中T表示温度,n表示起始时H2物质的量)。下列说法错误的是
2NH3(g)+QkJ(Q>0)。某科研小组研究:在其他条件不变的情况下,改变起始时氢气的物质的量对合成NH3反应的影响。实验结果如图所示:(图中T表示温度,n表示起始时H2物质的量)。下列说法错误的是
 2NH3(g)+QkJ(Q>0)。某科研小组研究:在其他条件不变的情况下,改变起始时氢气的物质的量对合成NH3反应的影响。实验结果如图所示:(图中T表示温度,n表示起始时H2物质的量)。下列说法错误的是
2NH3(g)+QkJ(Q>0)。某科研小组研究:在其他条件不变的情况下,改变起始时氢气的物质的量对合成NH3反应的影响。实验结果如图所示:(图中T表示温度,n表示起始时H2物质的量)。下列说法错误的是
| A.由图可知,T1>T2 |
| B.a、b、c三点中,b点时H2的转化率最大 |
| C.a、b、c三点的平衡常数K值相等,c点化学反应速率最快 |
| D.若容器容积为2 L,b点对应的n=0.15 mol,测得平衡时H2、N2的转化率均为60%,则平衡时N2的物质的量浓度为0.01mol·L-1 |
您最近半年使用:0次
2023-03-17更新
|
338次组卷
|
3卷引用:上海市普陀区2022-2023学年高三二模测试化学试题
名校
解题方法
7 . 有关下列图像的分析正确的是


| A.图①表示在合成氨反应达到平衡后,减少NH3浓度时速率的变化 |
| B.图②中a、b曲线分别表示在硫酸工业的接触室中有催化剂和无催化剂存在下建立平衡的过程 |
| C.图③说明酸HA是比酸HB更弱的酸 |
| D.图④表示AgBr在水中的沉淀溶解平衡曲线,在AgBr饱和溶液中加入固体NaBr,可使c点变到b点 |
您最近半年使用:0次
名校
解题方法
8 . 下列叙述与图对应的是
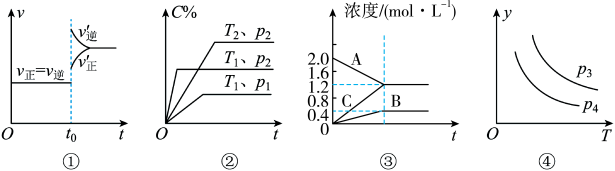

A.对于达到平衡状态的反应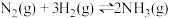 ,图①表示在 ,图①表示在 时刻充入了一定量 时刻充入了一定量 ,平衡逆向移动 ,平衡逆向移动 |
B.由图②可知, 、 、 满足反应: 满足反应: |
C.图③表示的反应方程式为 |
D.对于反应 ,图④y轴可以表示Y的百分含量 ,图④y轴可以表示Y的百分含量 |
您最近半年使用:0次
2023-01-14更新
|
440次组卷
|
9卷引用:上海市嘉定区安亭高级中学2022-2023学年高二上学期期中考试化学试题
上海市嘉定区安亭高级中学2022-2023学年高二上学期期中考试化学试题山东省文登第一中学2022-2023学年高二上学期1月期末考试化学试题 宁夏回族自治区银川一中2023-2024学年高二上学期期中考试化学试题内蒙古第一机械制造(集团)有限公司第一中学2023-2024学年高二上学期9月月考化学试题山东省菏泽市鄄城县第一中学2023-2024学年高二上学期10月月考化学试题(已下线)题型01 化学反应速率与化学平衡的图像分析-【好题汇编】备战2023-2024学年高二化学上学期期末真题分类汇编(人教版2019) 四川省成都市第八中学校2023-2024学年高二上学期第二次月考化学试题新疆乌鲁木齐市第三十一中学2023-2024学年高二上学期期中考试化学试卷 四川省眉山市仁寿第一中学校南校区2023-2024学年高二下学期3月月考化学试题
名校
解题方法
9 . 某温度时,在2L容器中发生A、B两种气态物质间的转化反应,A、B物质的量随时间变化的曲线如图所示。
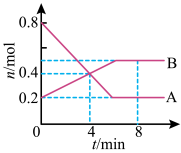
(1)该反应的化学方程式为_______ 。
(2)反应开始至4minA的平均反应速率为_______ 。
(3)4min时,反应是否达到化学平衡?_______ (填“是”或“否”);8min时,正反应速率_______ 逆反应速率(填“>”“<”或“=”)。
(4)如果温度和容积保持不变,下列情况能作为判断该反应达到化学平衡状态的依据有_______。

(1)该反应的化学方程式为
(2)反应开始至4minA的平均反应速率为
(3)4min时,反应是否达到化学平衡?
(4)如果温度和容积保持不变,下列情况能作为判断该反应达到化学平衡状态的依据有_______。
| A.容器中气体的密度不随时间而变化 | B.容器中A的浓度不再发生改变 |
| C.容器中B的质量不再发生改变 | D.容器中n(A):n(B)=2:1 |
您最近半年使用:0次
名校
10 . 某化学研究小组探究外界条件对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响,下列判断正确的是
pC(g)的速率和平衡的影响,下列判断正确的是

 pC(g)的速率和平衡的影响,下列判断正确的是
pC(g)的速率和平衡的影响,下列判断正确的是
| A.由图a可知,T1>T2,该反应的逆反应为吸热反应 |
| B.由图b可知,△H>0 |
| C.图c是绝热条件下速率和时间的图像,由此说明该反应吸热 |
| D.图d中,曲线a一定增加了催化剂 |
您最近半年使用:0次
2022-10-16更新
|
350次组卷
|
2卷引用:上海市奉贤中学2022-2023学年高二上学期10月阶段测试化学试题



