名校
1 . 含氮化合物和含碳化合物对环境、生产和人类生命活动有很大影响。请回答下列有关问题:
I.用CH4将氮氧化合物还原为无毒气体,可改善汽车尾气对环境的影响相关反应历程如图所示。

(1)反应a加入催化剂,可使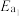
___________ (填“增大”“减小”或“不变”),相同条件下,反应速率b比a___________ (填“快”或“慢”),原因是___________ 。
(2)T℃时,向恒容密闭容器中加入一定量的 和
和 ,下列能表明反应
,下列能表明反应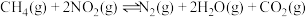 已达到平衡状态的是___________(填字母)。
已达到平衡状态的是___________(填字母)。
Ⅱ.反应 是一种碳资源化处理的途径,在不同温度下,向容积为2L的密闭容器内加入4mol的CO和8mol
是一种碳资源化处理的途径,在不同温度下,向容积为2L的密闭容器内加入4mol的CO和8mol ,
, 的物质的量随时间的变化情况如图:
的物质的量随时间的变化情况如图:

(3)
___________  (填“>”或“<”)。
(填“>”或“<”)。
(4)已知: ,
,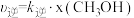 ,
, 和
和 分别为正、逆反应速率常数,x为物质的量分数,c点时
分别为正、逆反应速率常数,x为物质的量分数,c点时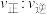 =
=___________ 。
I.用CH4将氮氧化合物还原为无毒气体,可改善汽车尾气对环境的影响相关反应历程如图所示。

(1)反应a加入催化剂,可使
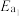
(2)T℃时,向恒容密闭容器中加入一定量的
 和
和 ,下列能表明反应
,下列能表明反应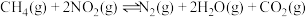 已达到平衡状态的是___________(填字母)。
已达到平衡状态的是___________(填字母)。| A.容器内气体颜色保持不变 |
B.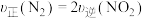 |
| C.容器内压强保持不变 |
| D.容器内混合气体的密度保持不变 |
Ⅱ.反应
 是一种碳资源化处理的途径,在不同温度下,向容积为2L的密闭容器内加入4mol的CO和8mol
是一种碳资源化处理的途径,在不同温度下,向容积为2L的密闭容器内加入4mol的CO和8mol ,
, 的物质的量随时间的变化情况如图:
的物质的量随时间的变化情况如图:
(3)

 (填“>”或“<”)。
(填“>”或“<”)。(4)已知:
 ,
,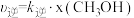 ,
, 和
和 分别为正、逆反应速率常数,x为物质的量分数,c点时
分别为正、逆反应速率常数,x为物质的量分数,c点时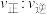 =
=
您最近半年使用:0次
名校
解题方法
2 . 溴代烷的制备,常规工艺分“氧化”和“溴化”两个过程,通常以 在合适温度下催化氧化HBr制备
在合适温度下催化氧化HBr制备 (溴易液化,注意控制温度和压强),再利用
(溴易液化,注意控制温度和压强),再利用 完成溴代过程来制备;新工艺是将烷烃、HBr和
完成溴代过程来制备;新工艺是将烷烃、HBr和 混合,直接催化“氧化溴化”得到溴代烷。回答下列问题:
混合,直接催化“氧化溴化”得到溴代烷。回答下列问题:
(1)已知: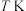 时,部分物质的相对能量如下表:
时,部分物质的相对能量如下表:
此温度下,在恒容密闭容器中充入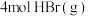 和
和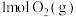 发生“氧化”,测得反应物的平衡转化率为60%。若保持其他条件不变,改为绝热状态,平衡时测得放出热量为
发生“氧化”,测得反应物的平衡转化率为60%。若保持其他条件不变,改为绝热状态,平衡时测得放出热量为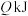 ,则下列关系正确的是___________(填标号)。
,则下列关系正确的是___________(填标号)。
(2)“溴化”时容器体积可变。在温度为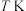 时,向
时,向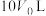 容器中投入初始浓度均为
容器中投入初始浓度均为 的
的 和
和 ,发生反应:
,发生反应: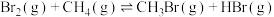 ,保持温度不变,压缩容器体积,测得不同容积下
,保持温度不变,压缩容器体积,测得不同容积下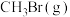 的平衡浓度如下表:
的平衡浓度如下表:
当容器体积从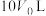 缩小到
缩小到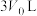 时,测得此时容器内只有气态组分,平衡
时,测得此时容器内只有气态组分,平衡______ 移动(填“正向”“逆向”或“不”),
_______ ;容器体积缩小到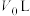 时,平衡
时,平衡_______ 移动(填“正向”“逆向”或“不”)。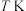 时,此反应在容积为
时,此反应在容积为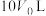 和
和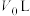 时化学平衡常数分别为
时化学平衡常数分别为 、
、 ,则
,则
____  (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
(3)新工艺中,“氧化溴化”反应: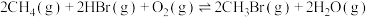
 。反应起始物料
。反应起始物料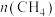 、
、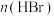 、
、 分别为2mol、2mol、1mol时,在不同条件下达到平衡,设体系中
分别为2mol、2mol、1mol时,在不同条件下达到平衡,设体系中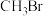 的物质的量分数为
的物质的量分数为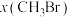 ,
,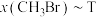 如图所示。
如图所示。

曲线Ⅰ:T为500K下的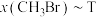 ,曲线Ⅱ:p为
,曲线Ⅱ:p为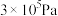 下的
下的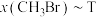
a点对应的温度为_______ ;b点时 的转化率为
的转化率为_______ (保留三位有效数字);c点时,平衡常数
_______ 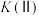 (填写“大于”“小于”或“无法确定”)。
(填写“大于”“小于”或“无法确定”)。
 在合适温度下催化氧化HBr制备
在合适温度下催化氧化HBr制备 (溴易液化,注意控制温度和压强),再利用
(溴易液化,注意控制温度和压强),再利用 完成溴代过程来制备;新工艺是将烷烃、HBr和
完成溴代过程来制备;新工艺是将烷烃、HBr和 混合,直接催化“氧化溴化”得到溴代烷。回答下列问题:
混合,直接催化“氧化溴化”得到溴代烷。回答下列问题:(1)已知:
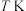 时,部分物质的相对能量如下表:
时,部分物质的相对能量如下表:| 物质 | 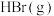 |  |  |  |
| 相对能量(kJ/mol) | x | y | z | w |
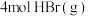 和
和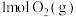 发生“氧化”,测得反应物的平衡转化率为60%。若保持其他条件不变,改为绝热状态,平衡时测得放出热量为
发生“氧化”,测得反应物的平衡转化率为60%。若保持其他条件不变,改为绝热状态,平衡时测得放出热量为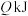 ,则下列关系正确的是___________(填标号)。
,则下列关系正确的是___________(填标号)。A.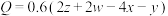 | B.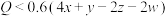 |
C. | D.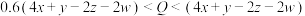 |
(2)“溴化”时容器体积可变。在温度为
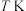 时,向
时,向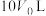 容器中投入初始浓度均为
容器中投入初始浓度均为 的
的 和
和 ,发生反应:
,发生反应: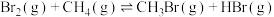 ,保持温度不变,压缩容器体积,测得不同容积下
,保持温度不变,压缩容器体积,测得不同容积下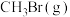 的平衡浓度如下表:
的平衡浓度如下表:| 容器体积V/L |  |  |  |
 | m | 0.09 | 0.25 |
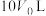 缩小到
缩小到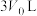 时,测得此时容器内只有气态组分,平衡
时,测得此时容器内只有气态组分,平衡
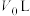 时,平衡
时,平衡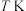 时,此反应在容积为
时,此反应在容积为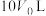 和
和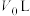 时化学平衡常数分别为
时化学平衡常数分别为 、
、 ,则
,则
 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。(3)新工艺中,“氧化溴化”反应:
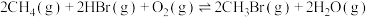
 。反应起始物料
。反应起始物料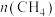 、
、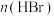 、
、 分别为2mol、2mol、1mol时,在不同条件下达到平衡,设体系中
分别为2mol、2mol、1mol时,在不同条件下达到平衡,设体系中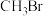 的物质的量分数为
的物质的量分数为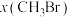 ,
,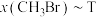 如图所示。
如图所示。
曲线Ⅰ:T为500K下的
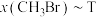 ,曲线Ⅱ:p为
,曲线Ⅱ:p为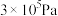 下的
下的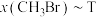
a点对应的温度为
 的转化率为
的转化率为
 (填写“大于”“小于”或“无法确定”)。
(填写“大于”“小于”或“无法确定”)。
您最近半年使用:0次
名校
解题方法
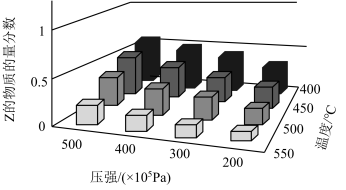
3 . 为探究外界条件对反应:mA(g)+nB(g) cZ(g) ΔH 的影响,以A和B 的物质的量之比为 m:n 开始反应,通过实验得到不同条件下反应达到平衡时Z的物质的量分数与压强及温度的关系,实验结果如图所示。下列判断正确的是
cZ(g) ΔH 的影响,以A和B 的物质的量之比为 m:n 开始反应,通过实验得到不同条件下反应达到平衡时Z的物质的量分数与压强及温度的关系,实验结果如图所示。下列判断正确的是
 cZ(g) ΔH 的影响,以A和B 的物质的量之比为 m:n 开始反应,通过实验得到不同条件下反应达到平衡时Z的物质的量分数与压强及温度的关系,实验结果如图所示。下列判断正确的是
cZ(g) ΔH 的影响,以A和B 的物质的量之比为 m:n 开始反应,通过实验得到不同条件下反应达到平衡时Z的物质的量分数与压强及温度的关系,实验结果如图所示。下列判断正确的是
| A.ΔН>0 |
| B.m+n<c |
| C.升高温度,ν正 ν逆都增大,平衡常数增大 |
| D.恒温恒压时,向已达到平衡的体系中加入少量 Z(g),再次达到平衡后Z的物质的量分数不变 |
您最近半年使用:0次
解题方法
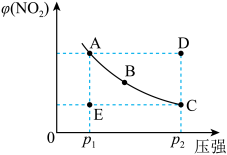
4 . 对于反应N2O4(g) 2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示。下列说法错误的是
2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示。下列说法错误的是
 2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示。下列说法错误的是
2NO2(g),在温度一定时,平衡体系中NO2的体积分数φ(NO2)随压强的变化情况如图所示。下列说法错误的是
| A.A、D两点对应状态的正反应速率大小关系:v(A)>v(D) |
| B.A、B、C、D、E各点对应的状态中,v正<v逆的是D |
| C.C. 维持p1不变,E→A所需时间为t1,维持p2不变,D→C所需时间为t2,则t1>t2 |
| D.欲使C状态到达A状态,从理论上,可将p2降压至p1 |
您最近半年使用:0次
解题方法
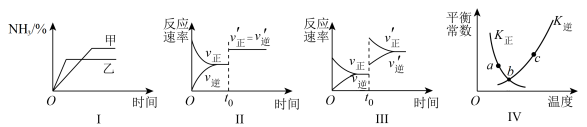
5 . 在容积不变的密闭容器中进行反应:
 。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是

 。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
。下列各图表示当其他条件不变时,改变某一条件对上述反应的影响,其中分析正确的是
| A.图Ⅰ表示温度对化学平衡的影响,且甲的温度较高 |
B.图Ⅱ表示 时刻使用催化剂对反应速率的影响 时刻使用催化剂对反应速率的影响 |
C.图Ⅲ表示 时刻增大 时刻增大 的浓度对反应速率的影响 的浓度对反应速率的影响 |
| D.图Ⅳa、b、c三点,只有b点达到平衡状态 |
您最近半年使用:0次
6 . 对于可逆反应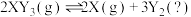
 ,有关图像[
,有关图像[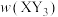 表示平衡时
表示平衡时 所占的体积分数]如图所示,下列说法正确的是
所占的体积分数]如图所示,下列说法正确的是

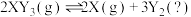
 ,有关图像[
,有关图像[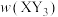 表示平衡时
表示平衡时 所占的体积分数]如图所示,下列说法正确的是
所占的体积分数]如图所示,下列说法正确的是
A.依据图1可知 , , 为液体 为液体 |
B.图2中 时改变的条件可能为压缩容器体积 时改变的条件可能为压缩容器体积 |
| C.图3中曲线b表示的是该反应的逆反应速率 |
D.已知 时,平衡常数 时,平衡常数 。若在此温度下,测得某密闭容器中某时刻 。若在此温度下,测得某密闭容器中某时刻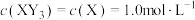 , ,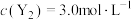 ,则此时 ,则此时 |
您最近半年使用:0次
名校
7 . 一定条件下,治理汽车尾气的反应是2NO(g)+2CO(g) 2CO2(g)+N2(g) △H<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=2:1的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时一定达到平衡状态的是
2CO2(g)+N2(g) △H<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=2:1的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时一定达到平衡状态的是
 2CO2(g)+N2(g) △H<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=2:1的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时一定达到平衡状态的是
2CO2(g)+N2(g) △H<0。在恒温恒容的密闭容器中通入n(NO):n(CO)=2:1的混合气体,发生上述反应。下列图像正确且能说明反应在进行到t1时一定达到平衡状态的是A. | B.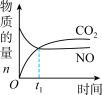 |
C.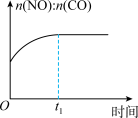 | D. |
您最近半年使用:0次
2023-08-28更新
|
262次组卷
|
4卷引用:辽宁省沈阳市第二中学2022-2023学年高二上学期10月阶段验收 化学试题
8 . 某化学研究小组探究外界条件对化学反应mA(g)+nB(g)⇌pC(g)(m+n≠p)的速率和平衡的影响,图象如图,下列判断正确的是


| A.图d中,曲线a一定增加了催化剂 |
| B.由图b可知,该反应m+n<p |
| C.图c是绝热条件下速率和时间的图象,由此说明该反应吸热 |
| D.由图a可知,T1>T2,该反应的逆反应为放热反应 |
您最近半年使用:0次
2023-08-26更新
|
902次组卷
|
5卷引用:辽宁省大连市第八中学2022-2023学年高二上学期10月月考化学试题
9 . 反应
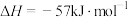 ,在温度为
,在温度为 、
、 时,平衡体系中
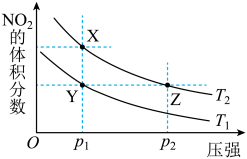
时,平衡体系中 的体积分数随压强变化曲线如图所示。下列说法错误的是
的体积分数随压强变化曲线如图所示。下列说法错误的是

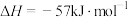 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化曲线如图所示。下列说法错误的是
的体积分数随压强变化曲线如图所示。下列说法错误的是
A.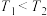 |
B.X、Y两点的反应速率: |
| C.X、Z两点气体的颜色:X浅,Z深 |
D.X、Z两点气体的平均相对分子质量: |
您最近半年使用:0次
2023-06-27更新
|
685次组卷
|
4卷引用:辽宁省辽东南协作校2023-2024学年高三上学期12月月考化学(A卷)试题
名校
10 . 向一恒容密闭容器中充入A、B、C三种气体,在一定条件下发生反应,各物质的物质的量浓度随时间的变化如图a所示。若从 时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b,下列说法不正确的是
时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b,下列说法不正确的是

 时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b,下列说法不正确的是
时刻开始,每个时刻只改变一个且不重复的条件,物质C的正、逆反应速率随时间变化如图b,下列说法不正确的是
A.O至 内,A与B的平均反应速率之比为3∶2 内,A与B的平均反应速率之比为3∶2 |
B.该反应的化学方程式为 |
C. 时,改变的条件可能是加入催化剂 时,改变的条件可能是加入催化剂 |
| D.该反应的正反应为放热反应 |
您最近半年使用:0次



