1 . 在一定温度下,向一容积为5 L的恒容密闭容器中充入0.4 mol SO2和0.2 mol O2,发生反应:2SO2(g)+O2(g) 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
(1)判断该反应达到平衡状态的标志是___________ (填字母);
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为___________ ,用SO2的浓度变化表示的平均反应速率v(SO2)=___________ 。
(3)若反应温度降低,SO2的转化率___________ (填“增大”“减小”或“不变”);如图表示平衡时SO2的体积分数随压强和温度变化的曲线。则温度关系:T1___________ T2(填“>”“<”或“=”)。
 2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:
2SO3(g) ∆H = -196 kJ/mol。经2 min后达到平衡,当反应达到平衡时,容器内压强变为起始时的0.8倍。请回答下列问题:(1)判断该反应达到平衡状态的标志是
a.SO2、O2、SO3三者的浓度之比为2∶1∶2
b.容器内气体的压强不变
c.容器内混合气体的密度保持不变
d.SO3的物质的量不再变化
e.SO2的生成速率和SO3的生成速率相等
(2)从反应开始到平衡的这段时间O2的转化率为
(3)若反应温度降低,SO2的转化率

您最近半年使用:0次
解题方法
2 . 燃油汽车尾气中含有NO和CO等有毒气体,某研究小组用新型催化剂对NO、CO在不同条件下的催化转化进行研究,反应原理为:
 。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是
。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是

 。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是
。在密闭容器中充入2 mol NO和2 mol CO,平衡时NO的体积分数随温度、压强的变化关系如图。下列说法正确的是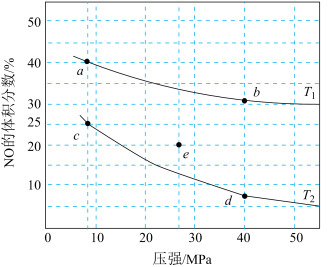
| A.a点CO的平衡转化率为25% |
| B.c点和b点的反应速率可能相同 |
| C.若在e点扩大容器体积并加热,可能达到c点状态 |
| D.恒温恒压条件下,向d点平衡体系中再充入2 mol NO和2 mol CO,重新达到平衡后,与d点状态相比,NO的体积分数将增大 |
您最近半年使用:0次
2024-04-17更新
|
293次组卷
|
3卷引用:广西壮族自治区柳州市2024届高三第三次模拟考试化学试题
广西壮族自治区柳州市2024届高三第三次模拟考试化学试题广西柳州市2024届高三下学期第三次模拟考试(三模)化学试题(已下线)题型7 化学反应速率与化学平衡 水溶液中的离子反应与平衡(25题)-2024年高考化学常考点必杀300题(新高考通用)
3 . 已知反应: 。在一定压强下,按
。在一定压强下,按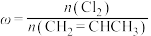 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
 。在一定压强下,按
。在一定压强下,按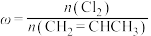 向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数(
向密闭容器中充入氯气与丙烯。图甲表示平衡时,丙烯的体积分数( )与温度(T)、
)与温度(T)、 的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
的关系,图乙表示反应的平衡常数(K)与温度(T)的关系。则下列说法正确的是
A.此反应 H>0 H>0 | B.图甲中 |
| C.图乙中,曲线A表示正反应的平衡常数 | D.温度T1、 , , 的转化率约为33.3% 的转化率约为33.3% |
您最近半年使用:0次
4 . 可逆反应mA(g)+nB(g)⇌pC(g)+qD(g)的相关物质体积分数的变化图像如下,请回答下列问题:

(1)温度T1_______ T2(填“>”、“<”或“=”,下同)。
(2)压强p1_______ p2。
(3)m+n_______ p+q。
(4)正反应为_______ (填“放热”或“吸热”)反应。

(1)温度T1
(2)压强p1
(3)m+n
(4)正反应为
您最近半年使用:0次
5 . 恒容条件下,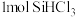 发生如下反应:
发生如下反应: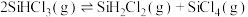 。已知:
。已知: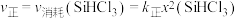 ,
,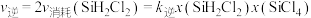 ,
,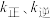 分别为正、逆向反应速率常数(仅与温度有关),
分别为正、逆向反应速率常数(仅与温度有关), 为物质的量分数。如图是不同温度下
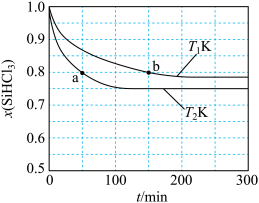
为物质的量分数。如图是不同温度下 随时间的变化。下列说法不正确的是
随时间的变化。下列说法不正确的是
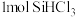 发生如下反应:
发生如下反应: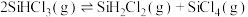 。已知:
。已知: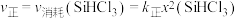 ,
,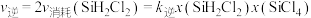 ,
,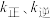 分别为正、逆向反应速率常数(仅与温度有关),
分别为正、逆向反应速率常数(仅与温度有关), 为物质的量分数。如图是不同温度下
为物质的量分数。如图是不同温度下 随时间的变化。下列说法不正确的是
随时间的变化。下列说法不正确的是
A.已知电负性: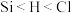 ,则 ,则 与水反应的方程式为: 与水反应的方程式为: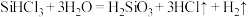 |
B.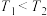 ,该反应 ,该反应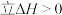 |
C. 时平衡体系中再充入 时平衡体系中再充入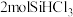 ,平衡正向移动, ,平衡正向移动,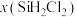 增大 增大 |
D.当反应进行到 处时, 处时, |
您最近半年使用:0次
23-24高三上·北京·阶段练习
名校
解题方法
6 . 工业上利用碳热还原 制得
制得 ,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原
,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原 过程中可能发生下列反应
过程中可能发生下列反应
ⅰ.
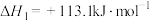
ⅱ.
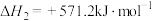
ⅲ.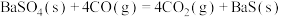
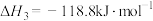

关于碳热还原 的过程,下列说法正确的是
的过程,下列说法正确的是
 制得
制得 ,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原
,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原 过程中可能发生下列反应
过程中可能发生下列反应ⅰ.

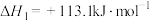
ⅱ.

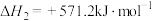
ⅲ.
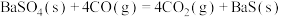
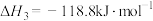

关于碳热还原
 的过程,下列说法正确的是
的过程,下列说法正确的是A.制 的最佳温度应控制在1000℃ 的最佳温度应控制在1000℃ |
| B.400℃之前一定不会发生反应ⅱ |
C.400℃后,反应后组分的变化可能与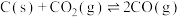 有关 有关 |
D.反应过程中,生成的 和CO的物质的量之和始终等于投入C的物质的量 和CO的物质的量之和始终等于投入C的物质的量 |
您最近半年使用:0次
7 . 温室气体让地球“发烧”,倡导低碳生活,是一种可持续发展的环保责任,通过化学、生物等方法将其转化为更具附加值的能源、化工原料和精细化学品成为目前研究热点。回答下列问题:
(1)通过使用不同的新型催化剂,实现二氧化碳加氢合成转化为二甲醚(CH3OCH3)也有广泛的应用。
反应Ⅰ: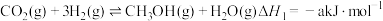
反应Ⅱ: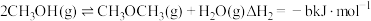
反应Ⅲ: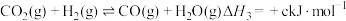
则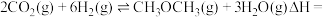
___________  。
。
(2)一定条件下, 的反应历程如图所示。该反应的反应速率由第
的反应历程如图所示。该反应的反应速率由第___________ (填“1”或“2”)步决定。

(3)向2L恒容密闭容器中充入amolCO2和3amolH2,在一定条件下,仅发生上述反应Ⅰ;在甲、乙两种不同催化剂的作用下,反应时间均为tmin时,测得甲醇的物质的量分数随温度的变化如图所示。
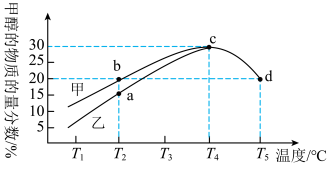
①相同温度下,催化剂效果更好的是___________ (填“甲”或“乙”)。
②T2℃和T5℃下,平衡常数:K2___________ (填“>”“<”或“=”)K5。
③T5℃下,甲醇的平均反应速率为___________  ,反应开始时容器中的总压为p0MPa,该温度下反应的平衡常数Kp=
,反应开始时容器中的总压为p0MPa,该温度下反应的平衡常数Kp=___________ (列出计算式即可,气体分压=气体总压 气体的物质的量分数)。
气体的物质的量分数)。
(4)甲醇(CH3OH)是重要的化工原料及能源物质,如图是甲醇燃料电池工作原理示意图。
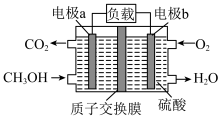
①a电极是电池的___________ (填“正”或“负”)极。
②b电极的电极反应式为___________ 。
(1)通过使用不同的新型催化剂,实现二氧化碳加氢合成转化为二甲醚(CH3OCH3)也有广泛的应用。
反应Ⅰ:
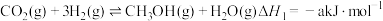
反应Ⅱ:
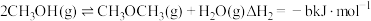
反应Ⅲ:
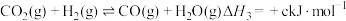
则
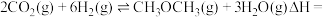
 。
。(2)一定条件下,
 的反应历程如图所示。该反应的反应速率由第
的反应历程如图所示。该反应的反应速率由第
(3)向2L恒容密闭容器中充入amolCO2和3amolH2,在一定条件下,仅发生上述反应Ⅰ;在甲、乙两种不同催化剂的作用下,反应时间均为tmin时,测得甲醇的物质的量分数随温度的变化如图所示。

①相同温度下,催化剂效果更好的是
②T2℃和T5℃下,平衡常数:K2
③T5℃下,甲醇的平均反应速率为
 ,反应开始时容器中的总压为p0MPa,该温度下反应的平衡常数Kp=
,反应开始时容器中的总压为p0MPa,该温度下反应的平衡常数Kp= 气体的物质的量分数)。
气体的物质的量分数)。(4)甲醇(CH3OH)是重要的化工原料及能源物质,如图是甲醇燃料电池工作原理示意图。

①a电极是电池的
②b电极的电极反应式为
您最近半年使用:0次
名校
解题方法
8 . 反应mA(g)+nB(g) eC(g)+fD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述中正确的是
eC(g)+fD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述中正确的是
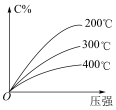
 eC(g)+fD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述中正确的是
eC(g)+fD(g),反应过程中,当其他条件不变时,C的百分含量(C%)与温度(T)和压强(p)的关系如图所示。下列叙述中正确的是
| A.达到平衡后,加入催化剂则C%增大 |
| B.化学方程式中n<e+f |
| C.达到平衡后,若升温,平衡左移 |
D.达到平衡后,增加 的量有利于平衡向右移动 的量有利于平衡向右移动 |
您最近半年使用:0次
9 . 绿色能源是未来能源发展的方向,积极发展氢能,是实现“碳达峰、碳中和”的重要举措,可以用以下方法制备氢气。
I.甲烷和水蒸气催化制氢气。主要反应如下:
i.CH4(g)+H2O(g) CO(g)+3H2(g) △H=+206.2kJ•mol-1
CO(g)+3H2(g) △H=+206.2kJ•mol-1
ii.CO(g)+H2O(g) CO2(g)+H2(g) △H=-41.2kJ•mol-1
CO2(g)+H2(g) △H=-41.2kJ•mol-1
(1)反应CH4(g)+CO2(g) 2CO(g)+2H2(g)的△H=
2CO(g)+2H2(g)的△H=______ kJ•mol-1。
(2)在容积不变的绝热密闭容器中发生反应i,下列能说明反应达到平衡状态的是______ (填标号)。
A.气体混合物的密度不再变化
B.CH4消耗速率和H2的生成速率相等
C.CO的浓度保持不变
D.气体平均相对分子质量不再变化
E.体系的温度不再发生变化
(3)恒定压强为P0MPa时,将n(CH4):n(H2O)=1:3的混合气体投入反应器中发生反应i和ii,平衡时,各组分的物质的量分数与温度的关系如图所示。
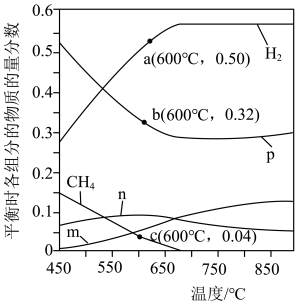
①图中表示CO2的物质的量分数与温度的变化曲线是______ (填字母)。
②结合图中数据,其他条件不变,若要H2的产量最大,最适宜的反应温度是______ (填标号)。
A.550~600℃ B.650~700℃ C.750~800℃
在其他条件不变的情况下,向体系中加入CaO可明显提高平衡体系中H2的含量,原因是______ 。
③600℃时,反应ii的平衡常数的计算式为Kp=______ (Kp是以分压表示的平衡常数,分压=总压×物质的量分数)。
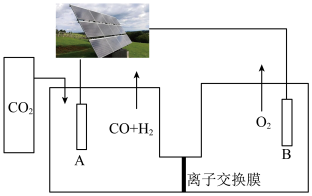
Ⅱ.电解法制氢气。某科研小组设计如图所示电解池,利用CO2和H2O在碱性电解液中制备水煤气(H2、CO),产物中H2和CO的物质的量之比为1∶1。
(4)电极B是______ 极,生成水煤气的电极反应式为______ 。
I.甲烷和水蒸气催化制氢气。主要反应如下:
i.CH4(g)+H2O(g)
 CO(g)+3H2(g) △H=+206.2kJ•mol-1
CO(g)+3H2(g) △H=+206.2kJ•mol-1ii.CO(g)+H2O(g)
 CO2(g)+H2(g) △H=-41.2kJ•mol-1
CO2(g)+H2(g) △H=-41.2kJ•mol-1(1)反应CH4(g)+CO2(g)
 2CO(g)+2H2(g)的△H=
2CO(g)+2H2(g)的△H=(2)在容积不变的绝热密闭容器中发生反应i,下列能说明反应达到平衡状态的是
A.气体混合物的密度不再变化
B.CH4消耗速率和H2的生成速率相等
C.CO的浓度保持不变
D.气体平均相对分子质量不再变化
E.体系的温度不再发生变化
(3)恒定压强为P0MPa时,将n(CH4):n(H2O)=1:3的混合气体投入反应器中发生反应i和ii,平衡时,各组分的物质的量分数与温度的关系如图所示。

①图中表示CO2的物质的量分数与温度的变化曲线是
②结合图中数据,其他条件不变,若要H2的产量最大,最适宜的反应温度是
A.550~600℃ B.650~700℃ C.750~800℃
在其他条件不变的情况下,向体系中加入CaO可明显提高平衡体系中H2的含量,原因是
③600℃时,反应ii的平衡常数的计算式为Kp=
Ⅱ.电解法制氢气。某科研小组设计如图所示电解池,利用CO2和H2O在碱性电解液中制备水煤气(H2、CO),产物中H2和CO的物质的量之比为1∶1。
(4)电极B是

您最近半年使用:0次
2023-10-27更新
|
907次组卷
|
3卷引用:广西部分高中2024届高三第一次摸底测试化学试题
23-24高三上·重庆·阶段练习
名校
解题方法
10 . 草酸二甲酯(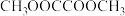 )和
)和 在催化剂条件下发生如下反应:
在催化剂条件下发生如下反应:
反应Ⅰ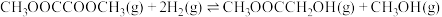

反应Ⅱ

将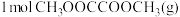 和
和 通入含催化剂的1 L恒容容器中,相同时间内测得草酸二甲酯的转化率及
通入含催化剂的1 L恒容容器中,相同时间内测得草酸二甲酯的转化率及 、
、 的选择性与温度的关系如图所示。已知,b线表示
的选择性与温度的关系如图所示。已知,b线表示 的选择性[
的选择性[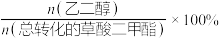 ]。下列说法正确的是
]。下列说法正确的是

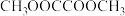 )和
)和 在催化剂条件下发生如下反应:
在催化剂条件下发生如下反应:反应Ⅰ
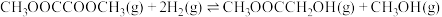

反应Ⅱ


将
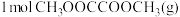 和
和 通入含催化剂的1 L恒容容器中,相同时间内测得草酸二甲酯的转化率及
通入含催化剂的1 L恒容容器中,相同时间内测得草酸二甲酯的转化率及 、
、 的选择性与温度的关系如图所示。已知,b线表示
的选择性与温度的关系如图所示。已知,b线表示 的选择性[
的选择性[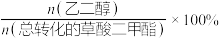 ]。下列说法正确的是
]。下列说法正确的是
| A.反应Ⅰ在高温条件下才能自发 |
| B.190~198℃范围内,升高温度,草酸二甲酯的平衡转化率减小 |
| C.c线表示草酸二甲酯的转化率与温度的关系 |
| D.可用M点对应的转化率和选择性的数据求194℃时反应Ⅱ的平衡常数K |
您最近半年使用:0次
2023-10-13更新
|
255次组卷
|
3卷引用:选择题11-14



