名校
1 . T℃时在2L密闭容器中使X(g)与Y(g)发生反应生成Z(g)。反应过程中X、Y、Z的物质的量变化如图-1所示;若保持其他条件不变,温度分别为T1和T2,Y的体积百分含量与时间的关系如图-2所示。下列分析正确的是
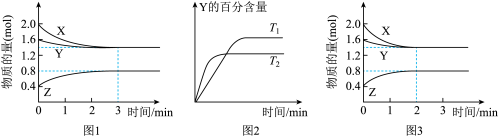

A.容器中发生的反应可表示为:2X(g)+Y(g) 2Z(g) 2Z(g) |
B.0~3 min内, (X)=0.2 mol•L-1•min-1 (X)=0.2 mol•L-1•min-1 |
C.其他条件不变升高温度, 正、 正、 逆都增大,且重新平衡前 逆都增大,且重新平衡前 正> 正> 逆 逆 |
| D.若改变条件,使反应进程如图-3所示,则改变的条件可能是增大压强 |
您最近半年使用:0次
名校
2 . 羰基硫(COS)作为一种粮食熏蒸剂广泛应用于农药工业。利用工厂废气中的H2S和CO反应可以合成COS,回答下列问题:
(1)已知:①CO的燃烧热为283kJ•mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH1=-484kJ•mol-1
③COS(g)+H2O(g) H2S(g)+CO2(g) ΔH2=-18kJ•mol-1
H2S(g)+CO2(g) ΔH2=-18kJ•mol-1
④CO(g)+H2S(g) COS(g)+H2(g) ΔH3
COS(g)+H2(g) ΔH3
则ΔH3=_______ kJ•mol-1。
(2)以FeOOH作催化剂,由H2S和CO合成COS的反应分两步进行。下列示意图能正确体现上述反应能量变化的是_______ (填“甲”或“乙”)。
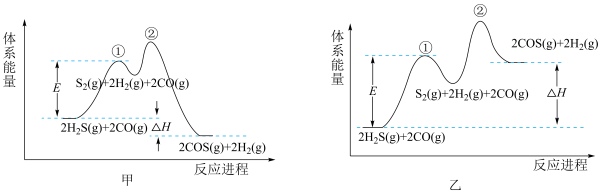
关于该反应的下列叙述正确的是_______ (填标号)。
A.步骤①是慢反应,活化能较大 B.总反应的速率由步骤②决定
C.反应进程中S2属于中间产物 D.更换催化剂可改变E和ΔH
(3)在240℃,将等物质的量H2S和CO充入恒压(100kPa)的密闭容器中发生反应:CO(g)+H2S(g) COS(g)+H2(g)。已知正反应速率v正=k正×p(CO)×p(H2S),v逆=k逆×p(COS)×p(H2),其中p为分压,该温度下k正=5.0×10-4kPa-1•s-1,反应达平衡时v逆=
COS(g)+H2(g)。已知正反应速率v正=k正×p(CO)×p(H2S),v逆=k逆×p(COS)×p(H2),其中p为分压,该温度下k正=5.0×10-4kPa-1•s-1,反应达平衡时v逆= kPa-1•s-1测得,则H2S的转化率为
kPa-1•s-1测得,则H2S的转化率为______ ,COS的体积分数为______ 。在240℃下,要同时提高CO和H2S的转化率,可采取的措施是______ 。
(4)在两个密闭容器中都加入CO、H2S、COS、H2四种气体,起始时气体体积分数φ(CO)=φ(H2S),φ(COS)=p(H2),分别在300℃和320℃时反应,容器中H2S(g)和COS(g)的体积分数(φ)随时间(t)的变化关系如图所示。

320℃时,φ(COS)随时间变化关系的曲线是______ ,判断的理由是_______ 。
(1)已知:①CO的燃烧热为283kJ•mol-1
②2H2(g)+O2(g)=2H2O(g) ΔH1=-484kJ•mol-1
③COS(g)+H2O(g)
 H2S(g)+CO2(g) ΔH2=-18kJ•mol-1
H2S(g)+CO2(g) ΔH2=-18kJ•mol-1④CO(g)+H2S(g)
 COS(g)+H2(g) ΔH3
COS(g)+H2(g) ΔH3则ΔH3=
(2)以FeOOH作催化剂,由H2S和CO合成COS的反应分两步进行。下列示意图能正确体现上述反应能量变化的是

关于该反应的下列叙述正确的是
A.步骤①是慢反应,活化能较大 B.总反应的速率由步骤②决定
C.反应进程中S2属于中间产物 D.更换催化剂可改变E和ΔH
(3)在240℃,将等物质的量H2S和CO充入恒压(100kPa)的密闭容器中发生反应:CO(g)+H2S(g)
 COS(g)+H2(g)。已知正反应速率v正=k正×p(CO)×p(H2S),v逆=k逆×p(COS)×p(H2),其中p为分压,该温度下k正=5.0×10-4kPa-1•s-1,反应达平衡时v逆=
COS(g)+H2(g)。已知正反应速率v正=k正×p(CO)×p(H2S),v逆=k逆×p(COS)×p(H2),其中p为分压,该温度下k正=5.0×10-4kPa-1•s-1,反应达平衡时v逆= kPa-1•s-1测得,则H2S的转化率为
kPa-1•s-1测得,则H2S的转化率为(4)在两个密闭容器中都加入CO、H2S、COS、H2四种气体,起始时气体体积分数φ(CO)=φ(H2S),φ(COS)=p(H2),分别在300℃和320℃时反应,容器中H2S(g)和COS(g)的体积分数(φ)随时间(t)的变化关系如图所示。

320℃时,φ(COS)随时间变化关系的曲线是
您最近半年使用:0次
2024-03-20更新
|
210次组卷
|
2卷引用:四川省南充高级中学2023-2024学年高三下学期第二次模拟考试化学
名校
解题方法
3 . 回答下列问题
(1)某温度下, 的平衡常数为9,反应开始时
的平衡常数为9,反应开始时 和
和 的浓度都是
的浓度都是 ,达平衡时
,达平衡时 的转化率为
的转化率为_______ ;该温度下,若起始时c(CO)=0.01 mol∙L-1,c(H2O)=0.02 mol∙L-1,反应一段时间后,测得c(H2)=0.005mol∙L-1,则此时该反应
_______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)关于反应 △H<0,在一定条件下,反应过程中的速率变化曲线如图:其它条件不变,只改变一种条件,则t1时刻改变的外界条件可能是
△H<0,在一定条件下,反应过程中的速率变化曲线如图:其它条件不变,只改变一种条件,则t1时刻改变的外界条件可能是_______ (填选项,下同),t2时刻改变的外界条件又可能是_______ 。
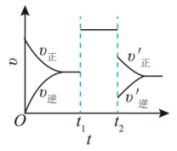
A.加入催化剂 B.压缩容器体积 C.升温 D.降温 E.扩大容器体积 F.恒容下,减少CO的用量 G.恒容下,移走部分CO2
(3)甲酸甲酯( )是一种重要的有机合成中间体,可通过甲醇催化脱氢法制备,其工艺过程包含以下反应:
)是一种重要的有机合成中间体,可通过甲醇催化脱氢法制备,其工艺过程包含以下反应:
反应Ⅰ: K1
K1 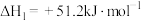
反应Ⅱ: K2
K2 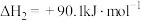
回答下列问题:
①反应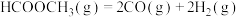 的△H3=
的△H3=_______ kJ∙mol-1,K3=_______ (用K1、K2表示)。
②在400kPa、铜基催化剂存在下,向密闭容器中通入CH3OH进行Ⅰ、Ⅱ两个反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。
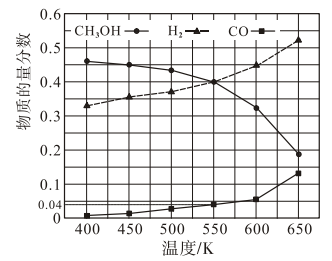
a.随温度升高,CH3OH的平衡组成比例呈现如图所示趋势的原因是_______ 。
b.550K时,反应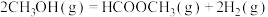 的平衡常数Kp=
的平衡常数Kp=_______  ,CH3OH的平衡转化率为
,CH3OH的平衡转化率为_______ 。(物质 的摩尔分数
的摩尔分数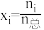 ,气体分压
,气体分压 )
)
c.研究表明,在700K以后升高体系温度,HCOOCH3的产率下降,可能的原因是_______ 。
(1)某温度下,
 的平衡常数为9,反应开始时
的平衡常数为9,反应开始时 和
和 的浓度都是
的浓度都是 ,达平衡时
,达平衡时 的转化率为
的转化率为
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)关于反应
 △H<0,在一定条件下,反应过程中的速率变化曲线如图:其它条件不变,只改变一种条件,则t1时刻改变的外界条件可能是
△H<0,在一定条件下,反应过程中的速率变化曲线如图:其它条件不变,只改变一种条件,则t1时刻改变的外界条件可能是
A.加入催化剂 B.压缩容器体积 C.升温 D.降温 E.扩大容器体积 F.恒容下,减少CO的用量 G.恒容下,移走部分CO2
(3)甲酸甲酯(
 )是一种重要的有机合成中间体,可通过甲醇催化脱氢法制备,其工艺过程包含以下反应:
)是一种重要的有机合成中间体,可通过甲醇催化脱氢法制备,其工艺过程包含以下反应:反应Ⅰ:
 K1
K1 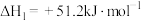
反应Ⅱ:
 K2
K2 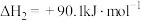
回答下列问题:
①反应
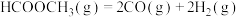 的△H3=
的△H3=②在400kPa、铜基催化剂存在下,向密闭容器中通入CH3OH进行Ⅰ、Ⅱ两个反应。体系中气体平衡组成比例(物质的量分数)随温度变化的理论计算结果如图所示。

a.随温度升高,CH3OH的平衡组成比例呈现如图所示趋势的原因是
b.550K时,反应
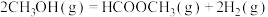 的平衡常数Kp=
的平衡常数Kp= ,CH3OH的平衡转化率为
,CH3OH的平衡转化率为 的摩尔分数
的摩尔分数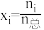 ,气体分压
,气体分压 )
)c.研究表明,在700K以后升高体系温度,HCOOCH3的产率下降,可能的原因是
您最近半年使用:0次
名校
解题方法
4 . 二氧化碳资源化利用是科研的热点, 甲烷化技术是重要途径之一,其相关反应如下:
甲烷化技术是重要途径之一,其相关反应如下:
ⅰ.
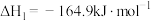
ⅱ.
 ;
;
ⅲ.积炭反应: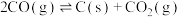
 ;
;
ⅳ.
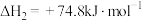 。
。
(1)CO歧化积炭反应在低温下能自发进行,则
______ 0(填“>”或“<”)。
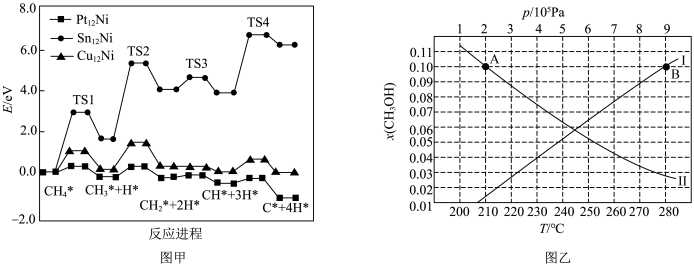
(2)研究表明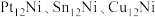 三种双金属合金团簇均可用于催化反应ⅰ,在催化剂表面涉及多个基元反应,其中
三种双金属合金团簇均可用于催化反应ⅰ,在催化剂表面涉及多个基元反应,其中 在不同催化剂作用下裂解的反应历程如图甲所示。
在不同催化剂作用下裂解的反应历程如图甲所示。
①该历程分______ 步进行,甲烷逐步脱氢过程中活化能最大的反应步骤是:______ (用化学方程式表示)。
②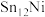 双金属合金团簇具有良好的抗积碳作用,有效抑制碳积沉对催化剂造成的不良影响,请结合图甲解释原因:
双金属合金团簇具有良好的抗积碳作用,有效抑制碳积沉对催化剂造成的不良影响,请结合图甲解释原因:______ 。
(3) 加氢制甲醇也是
加氢制甲醇也是 资源化利用的重要途径之一,其反应原理为
资源化利用的重要途径之一,其反应原理为
 。投料比
。投料比 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为 ,在
,在 时
时 随压强
随压强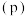 变化关系及在
变化关系及在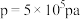 时
时 随温度(
随温度( )的曲线变化如图乙所示:
)的曲线变化如图乙所示:
①图中对应等温过程的曲线为______ 。
②图中 两点的速率
两点的速率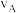
______  (填“>”、“<”或“=”)
(填“>”、“<”或“=”)
③当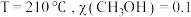 时,
时, 的平衡转化率为
的平衡转化率为______ ; 为210℃时,各物质的平衡分压表示反应的平衡常数
为210℃时,各物质的平衡分压表示反应的平衡常数
______ (列出计算式)。
 甲烷化技术是重要途径之一,其相关反应如下:
甲烷化技术是重要途径之一,其相关反应如下:ⅰ.

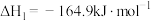
ⅱ.

 ;
;ⅲ.积炭反应:
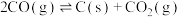
 ;
;ⅳ.

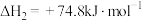 。
。
(1)CO歧化积炭反应在低温下能自发进行,则

(2)研究表明
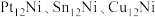 三种双金属合金团簇均可用于催化反应ⅰ,在催化剂表面涉及多个基元反应,其中
三种双金属合金团簇均可用于催化反应ⅰ,在催化剂表面涉及多个基元反应,其中 在不同催化剂作用下裂解的反应历程如图甲所示。
在不同催化剂作用下裂解的反应历程如图甲所示。①该历程分
②
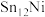 双金属合金团簇具有良好的抗积碳作用,有效抑制碳积沉对催化剂造成的不良影响,请结合图甲解释原因:
双金属合金团簇具有良好的抗积碳作用,有效抑制碳积沉对催化剂造成的不良影响,请结合图甲解释原因:(3)
 加氢制甲醇也是
加氢制甲醇也是 资源化利用的重要途径之一,其反应原理为
资源化利用的重要途径之一,其反应原理为
 。投料比
。投料比 时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为
时,在不同条件下达到平衡,设体系中甲醇的物质的量分数为 ,在
,在 时
时 随压强
随压强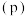 变化关系及在
变化关系及在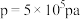 时
时 随温度(
随温度( )的曲线变化如图乙所示:
)的曲线变化如图乙所示:①图中对应等温过程的曲线为
②图中
 两点的速率
两点的速率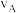
 (填“>”、“<”或“=”)
(填“>”、“<”或“=”)③当
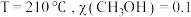 时,
时, 的平衡转化率为
的平衡转化率为 为210℃时,各物质的平衡分压表示反应的平衡常数
为210℃时,各物质的平衡分压表示反应的平衡常数
您最近半年使用:0次
名校
解题方法
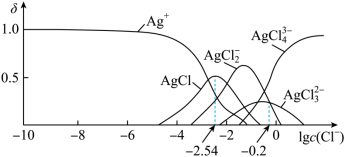
5 . 湿法提银工艺中,浸出的Ag+需加入Cl-进行沉淀。25℃时,平衡体系中含Ag微粒的分布系数δ[如δ(AgCl )=
)=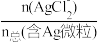 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
 )=
)=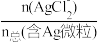 ]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
]随lgc(Cl-)的变化曲线如图所示。已知:lg[Ksp(AgCl)]=-9.75。下列叙述错误的是
| A.AgCl溶解度随c(Cl-)增大而不断减小 |
| B.沉淀最彻底时,溶液中c(Ag+)=10-7.21mol•L-1 |
C.当c(Cl-)=10-2mol•L-1时,溶液中c(AgCl )>c(Ag+)>c(AgCl )>c(Ag+)>c(AgCl ) ) |
D.25℃时,AgCl +Cl- +Cl- AgCl AgCl 的平衡常数K=100.2 的平衡常数K=100.2 |
您最近半年使用:0次
名校
6 . 已知某可逆反应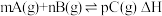 在密闭容器中进行,下图表示在不同反应时间t时温度T和压强P与反应物B在混合气体中的质量百分含量B%的关系曲线。由曲线分析,下列判断正确的是
在密闭容器中进行,下图表示在不同反应时间t时温度T和压强P与反应物B在混合气体中的质量百分含量B%的关系曲线。由曲线分析,下列判断正确的是
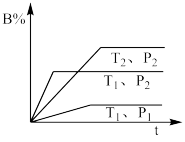
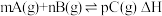 在密闭容器中进行,下图表示在不同反应时间t时温度T和压强P与反应物B在混合气体中的质量百分含量B%的关系曲线。由曲线分析,下列判断正确的是
在密闭容器中进行,下图表示在不同反应时间t时温度T和压强P与反应物B在混合气体中的质量百分含量B%的关系曲线。由曲线分析,下列判断正确的是
A.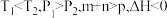 | B.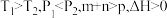 |
C. | D.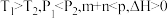 |
您最近半年使用:0次
名校
7 . 下列图示与对应的叙述相符的是


A.图一表示反应: ,在一定温度下,平衡时B的体积分数 ,在一定温度下,平衡时B的体积分数 与压强变化的关系如图所示,反应速率x点比y点时的快 与压强变化的关系如图所示,反应速率x点比y点时的快 |
B.图二是可逆反应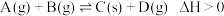 的速率时间图像,在 的速率时间图像,在 时刻改变条件是加入催化剂或缩小容器的体积加压 时刻改变条件是加入催化剂或缩小容器的体积加压 |
C.图三表示对于化学反应 ,反应物A的质量百分含量与温度 ,反应物A的质量百分含量与温度 的变化情况,则该反应的 的变化情况,则该反应的 |
D.图四所示图中的阴影部分面积的含义是 |
您最近半年使用:0次
名校
解题方法
8 . 丙烯是重要的化工原料,可用于生产丙醇、卤代烃和塑料。回答下列问题:
(1)工业上用丙烯加成法制备1,2-二氯丙烷,主要副产物为3-氯丙烯,反应原理为:
①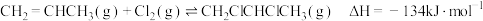
②
已知: 的活化能
的活化能 为
为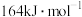 ,则该反应的活化能
,则该反应的活化能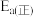 为
为___________  。
。
(2)某研究小组向密闭容器中充入一定量的 和
和 ,分别在
,分别在 、
、 两种不同催化剂作用下发生反应①,一段时间后测得
两种不同催化剂作用下发生反应①,一段时间后测得 的产率与温度的关系如下图所示。
的产率与温度的关系如下图所示。___________ (填代号)。
A.使用催化剂 的最佳温度约为
的最佳温度约为
B.相同条件下,改变压强不影响 的产率
的产率
C.两种催化剂均能降低反应的活化能,但 不变
不变
D.P点是对应温度下 的平衡产率
的平衡产率
②在催化剂 作用下,温度低于
作用下,温度低于 时,
时, 的产率随温度升高变化不大,主要原因是
的产率随温度升高变化不大,主要原因是___________ 。
(3) 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图所示。
时,测得丙烷及丙烯的物质的量分数如图所示。___________ (填“丙烷”或“丙烯”),
___________  (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。
②起始时充入一定量丙烷,在恒压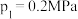 条件下发生反应,
条件下发生反应, 点对应温度下丙烷的转化率为
点对应温度下丙烷的转化率为___________ (保留1位小数),该反应的平衡常数
___________ 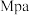 (用平衡分压代替平衡浓度计算,分压
(用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数)。
物质的量分数)。
(1)工业上用丙烯加成法制备1,2-二氯丙烷,主要副产物为3-氯丙烯,反应原理为:
①
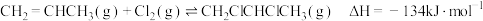
②

已知:
 的活化能
的活化能 为
为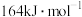 ,则该反应的活化能
,则该反应的活化能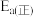 为
为 。
。(2)某研究小组向密闭容器中充入一定量的
 和
和 ,分别在
,分别在 、
、 两种不同催化剂作用下发生反应①,一段时间后测得
两种不同催化剂作用下发生反应①,一段时间后测得 的产率与温度的关系如下图所示。
的产率与温度的关系如下图所示。
A.使用催化剂
 的最佳温度约为
的最佳温度约为
B.相同条件下,改变压强不影响
 的产率
的产率C.两种催化剂均能降低反应的活化能,但
 不变
不变D.P点是对应温度下
 的平衡产率
的平衡产率②在催化剂
 作用下,温度低于
作用下,温度低于 时,
时, 的产率随温度升高变化不大,主要原因是
的产率随温度升高变化不大,主要原因是(3)
 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图所示。
时,测得丙烷及丙烯的物质的量分数如图所示。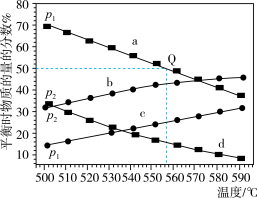

 (填“大于”、“小于”或“等于”)。
(填“大于”、“小于”或“等于”)。②起始时充入一定量丙烷,在恒压
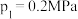 条件下发生反应,
条件下发生反应, 点对应温度下丙烷的转化率为
点对应温度下丙烷的转化率为
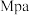 (用平衡分压代替平衡浓度计算,分压
(用平衡分压代替平衡浓度计算,分压 总压
总压 物质的量分数)。
物质的量分数)。
您最近半年使用:0次
2023-12-19更新
|
416次组卷
|
4卷引用:2024届四川省自贡市普高高三上学期第一次诊断性考试理综试题
2024届四川省自贡市普高高三上学期第一次诊断性考试理综试题河南省焦作市博爱县第一中学2023-2024学年高三下学期开学化学试题(已下线)专题10 化学反应原理综合题-【好题汇编】2024年高考化学一模试题分类汇编(全国通用)(已下线)大题04 化学反应原理综合题(逐空突破)-【大题精做】冲刺2024年高考化学大题突破+限时集训(新高考专用)
名校
9 . 在一定条件下,对于反应 ,C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的
,C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的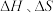 判断正确的是
判断正确的是
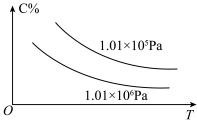
 ,C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的
,C的百分含量(C%)与温度、压强的关系如图所示,下列该反应的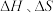 判断正确的是
判断正确的是
A.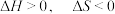 | B.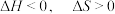 | C.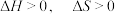 | D.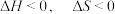 |
您最近半年使用:0次
名校
10 . 对化学反应mA(g)+nB(g) pC(g)的速率和平衡的影响,下列判断正确的是
pC(g)的速率和平衡的影响,下列判断正确的是

 pC(g)的速率和平衡的影响,下列判断正确的是
pC(g)的速率和平衡的影响,下列判断正确的是
| A.由图a可知,该反应的正反应为吸热反应 |
| B.由图b可知,该反应m+n>p |
| C.若图c是绝热条件下速率和时间的图像,说明该反应的正反应为吸热反应 |
| D.图d中的a曲线一定是加入了催化剂 |
您最近半年使用:0次
2023-10-17更新
|
653次组卷
|
4卷引用:四川省成都市第七中学2023-2024学年高一上学期12月月考化学试题



