1 . 已知反应
 ,将
,将 和
和 按一定比例通入恒温恒压的密闭容器中,反应相同时间后,
按一定比例通入恒温恒压的密闭容器中,反应相同时间后, 的体积分数随温度的变化关系如图所示,下列相关描述正确的是
的体积分数随温度的变化关系如图所示,下列相关描述正确的是

 ,将
,将 和
和 按一定比例通入恒温恒压的密闭容器中,反应相同时间后,
按一定比例通入恒温恒压的密闭容器中,反应相同时间后, 的体积分数随温度的变化关系如图所示,下列相关描述正确的是
的体积分数随温度的变化关系如图所示,下列相关描述正确的是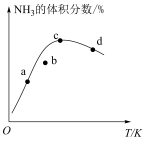
A.平衡常数值: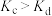 | B.逆反应速率: |
C.b点时 | D.曲线上的点均代表平衡时刻的点 |
您最近半年使用:0次
2 . 在 ℃,
℃, 下,向1L的密闭容器中充入1mol
下,向1L的密闭容器中充入1mol 和一定物质的量的
和一定物质的量的 发生反应:
发生反应: ,平衡时
,平衡时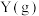 的物质的量分数与初始投料比
的物质的量分数与初始投料比 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是

 ℃,
℃, 下,向1L的密闭容器中充入1mol
下,向1L的密闭容器中充入1mol 和一定物质的量的
和一定物质的量的 发生反应:
发生反应: ,平衡时
,平衡时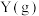 的物质的量分数与初始投料比
的物质的量分数与初始投料比 的关系如图所示。下列说法错误的是
的关系如图所示。下列说法错误的是
A.随着 的增大, 的增大, 的转化率逐渐增大 的转化率逐渐增大 |
B.e点: |
C.a点时,该反应的平衡常数为 |
D.a点,平衡后再投入1mol 和1mol 和1mol ,达到新平衡时, ,达到新平衡时,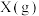 的产率增大 的产率增大 |
您最近半年使用:0次
名校
解题方法
3 . 图像对应的叙述正确的是
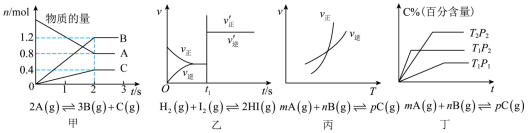

A.图甲:A的平衡转化率为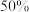 |
| B.图丙:对图中反应升高温度,该反应平衡常数减小 |
C.图乙: 时刻改变的条件只能是加入催化剂 时刻改变的条件只能是加入催化剂 |
| D.图丁:该正向反应在任何温度下都能自发进行 |
您最近半年使用:0次
解题方法
4 . 氨是重要的化工原料,我国目前氨的生产能力位居世界首位。回答下列问题:
(1)二十世纪初,工业以 和
和 为原料在一定温度和压强下合成尿素。反应分两步:a.
为原料在一定温度和压强下合成尿素。反应分两步:a. 和
和 生成
生成 ;b.
;b. 分解生成尿素,结合反应过程中能量变化示意图(如图),回答问题:
分解生成尿素,结合反应过程中能量变化示意图(如图),回答问题:
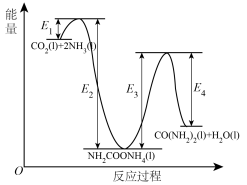
①反应a为反应_____ (填“放热”或“吸热”)。
②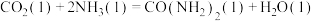

_____ kJ/mol(用含“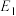 、
、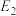 、
、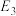 、
、 ”的代数式表示)。
”的代数式表示)。
(2)研究表明,合成氨反应在Fe催化剂上可能通过下图机理进行(*表示催化剂表面吸附位, 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 ),其中
),其中 的吸附分解反应活化能高,速率慢,是合成氨反应的决速步。
的吸附分解反应活化能高,速率慢,是合成氨反应的决速步。
(i)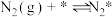
(ii)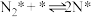
(iii)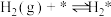
(iv)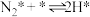
(v)
……
(…)
实际生产中, 和
和 的物质的量之比并非
的物质的量之比并非 ,而是
,而是 ,分析说明原料气中
,分析说明原料气中 适度过量的2个理由:
适度过量的2个理由:
①_____ ;②_____ 。
(3)若在不同压强下,以投料比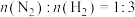 的方式进料,反应达平衡时氨的物质的量分数与温度的计算结果如图所示:(物质i的物质的量分数:
的方式进料,反应达平衡时氨的物质的量分数与温度的计算结果如图所示:(物质i的物质的量分数: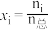 )
)
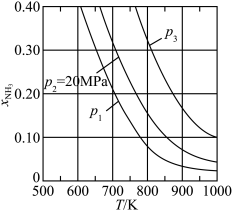
①图中压强由小到大的顺序为_____ 。
②当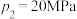 、
、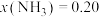 时,氮气的转化率ɑ=
时,氮气的转化率ɑ=_____ (保留到小数点后一位)。
③某温度下,在1L的密闭容器中充入 和
和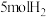 ,反应达到平衡后,测得
,反应达到平衡后,测得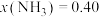 ,计算该温度下合成氨反应的平衡常数为
,计算该温度下合成氨反应的平衡常数为_____ 。
(1)二十世纪初,工业以
 和
和 为原料在一定温度和压强下合成尿素。反应分两步:a.
为原料在一定温度和压强下合成尿素。反应分两步:a. 和
和 生成
生成 ;b.
;b. 分解生成尿素,结合反应过程中能量变化示意图(如图),回答问题:
分解生成尿素,结合反应过程中能量变化示意图(如图),回答问题:
①反应a为反应
②
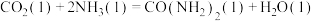

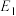 、
、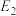 、
、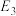 、
、 ”的代数式表示)。
”的代数式表示)。(2)研究表明,合成氨反应在Fe催化剂上可能通过下图机理进行(*表示催化剂表面吸附位,
 表示被吸附于催化剂表面的
表示被吸附于催化剂表面的 ),其中
),其中 的吸附分解反应活化能高,速率慢,是合成氨反应的决速步。
的吸附分解反应活化能高,速率慢,是合成氨反应的决速步。(i)
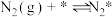
(ii)
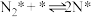
(iii)
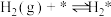
(iv)
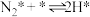
(v)

……
(…)
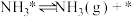
实际生产中,
 和
和 的物质的量之比并非
的物质的量之比并非 ,而是
,而是 ,分析说明原料气中
,分析说明原料气中 适度过量的2个理由:
适度过量的2个理由:①
(3)若在不同压强下,以投料比
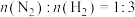 的方式进料,反应达平衡时氨的物质的量分数与温度的计算结果如图所示:(物质i的物质的量分数:
的方式进料,反应达平衡时氨的物质的量分数与温度的计算结果如图所示:(物质i的物质的量分数: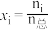 )
)
①图中压强由小到大的顺序为
②当
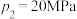 、
、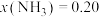 时,氮气的转化率ɑ=
时,氮气的转化率ɑ=③某温度下,在1L的密闭容器中充入
 和
和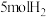 ,反应达到平衡后,测得
,反应达到平衡后,测得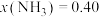 ,计算该温度下合成氨反应的平衡常数为
,计算该温度下合成氨反应的平衡常数为
您最近半年使用:0次
名校
5 . 反应
 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是


 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化的曲线如图所示。下列说法正确的是
的体积分数随压强变化的曲线如图所示。下列说法正确的是
| A.X、Z两点气体的颜色:X比Z浅 |
| B.X、Y两点的反应速率:X<Y |
C. |
| D.X、Z两点气体的平均相对分子质量:X>Z |
您最近半年使用:0次
名校
6 . 在2L恒容密闭容器中充入2molX和1molY,发生反应: ,反应过程中持续升高温度,测得X的体积分数与温度的关系如图所示。下列推断正确的是
,反应过程中持续升高温度,测得X的体积分数与温度的关系如图所示。下列推断正确的是
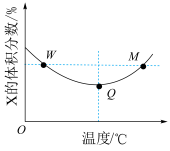
 ,反应过程中持续升高温度,测得X的体积分数与温度的关系如图所示。下列推断正确的是
,反应过程中持续升高温度,测得X的体积分数与温度的关系如图所示。下列推断正确的是
| A.Q点时,Y的转化率最大 |
| B.升高温度,平衡常数增大 |
| C.W点X的正反应速率等于M点X的正反应速率 |
| D.平衡时,再充入Y,达到平衡时Z的体积分数一定增大 |
您最近半年使用:0次
名校
解题方法
7 . 下列图示与对应的叙述相符的是
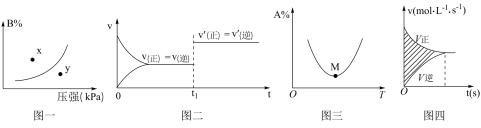

A.图一表示反应:  ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 ,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,反应速率x点比y点时的快 |
B.图二是可逆反应  的速率时间图像,在 的速率时间图像,在 时刻改变条件一定是加入催化剂 时刻改变条件一定是加入催化剂 |
C.图三表示对于化学反应 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 ,A的百分含量与温度(T)的变化情况,则升高温度,该反应平衡常数增大 |
D.图四所示图中的阴影部分面积的含义是( ) ) |
您最近半年使用:0次
2023-10-10更新
|
446次组卷
|
4卷引用:湖南省永州市第一中学2023-2024学年高二上学期10月月考化学试题
解题方法
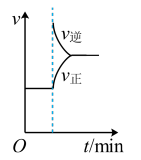
8 . 图中是某化学研究小组探究外界条件对化学反应速率和化学平衡影响的图像,其中,图像和实验结论表达均正确的是
 |  |
① | ② |
 |  |
③ | ④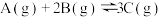 |
A.①是其他条件一定时,反应速率随温度变化的图像,正反应的 |
| B.②是在平衡体系的溶液中溶入少量KCl晶体后,化学反应速率随时间变化的图像 |
| C.③是在有催化剂和无催化剂存在下建立的平衡过程图像,a是使用催化剂时的曲线 |
| D.④表明该反应的正反应为吸热反应 |
您最近半年使用:0次
名校
解题方法
9 . 据报道,我国在南海北部神狐海域进行的可燃冰(甲烷的水合物)试采获得成功。甲烷是一种重要的化工原料。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:
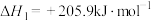 ①
①

 ②
②
二氧化碳重整:
 ③
③
则反应①自发进行的条件是_______ ,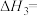
_______  。
。
氮的化合物以及氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为 。
。
(2)在不同温度、压强和相同催化剂条件下,初始 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。

①该反应
_______ 0(填“>”或“<”),图中 、
、 和
和 由大到小的顺序是
由大到小的顺序是_______ 。
②若分别用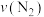 和
和 表示从反应开始至达平衡状态A、B时的化学反应速率,则
表示从反应开始至达平衡状态A、B时的化学反应速率,则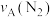
_______  (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是_______ 。
③下列描述中不能表明A点已达到平衡状态的是_______ 。(填字母)
a.氢气的消耗速率等于氢气的生成速率
b.容器内氮气、氢气、氨三种气体的物质的量浓度之比为
c.混合气体中氮气的体积分数保持不变
d.混合气体的相对分子质量保持不变
④若在250℃、 为
为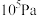 条件下,反应达到平衡时容器的体积为1L,则该条件下B点
条件下,反应达到平衡时容器的体积为1L,则该条件下B点 的分压
的分压 为
为_______ Pa(分压=总压×物质的量分数,保留一位小数)。
(1)甲烷重整是提高甲烷利用率的重要方式,除部分氧化外还有以下两种:
水蒸气重整:

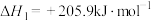 ①
①
 ②
②二氧化碳重整:

 ③
③则反应①自发进行的条件是
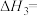
 。
。氮的化合物以及氮的固定一直是科学家研究的重要课题,合成氨则是人工固氮比较成熟的技术,其原理为
 。
。(2)在不同温度、压强和相同催化剂条件下,初始
 、
、 分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数(
分别为0.1mol、0.3mol时,平衡后混合物中氨的体积分数( )如图所示。
)如图所示。
①该反应

 、
、 和
和 由大到小的顺序是
由大到小的顺序是②若分别用
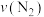 和
和 表示从反应开始至达平衡状态A、B时的化学反应速率,则
表示从反应开始至达平衡状态A、B时的化学反应速率,则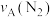
 (填“>”“<”或“=”),理由是
(填“>”“<”或“=”),理由是③下列描述中不能表明A点已达到平衡状态的是
a.氢气的消耗速率等于氢气的生成速率
b.容器内氮气、氢气、氨三种气体的物质的量浓度之比为

c.混合气体中氮气的体积分数保持不变
d.混合气体的相对分子质量保持不变
④若在250℃、
 为
为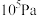 条件下,反应达到平衡时容器的体积为1L,则该条件下B点
条件下,反应达到平衡时容器的体积为1L,则该条件下B点 的分压
的分压 为
为
您最近半年使用:0次
名校
解题方法
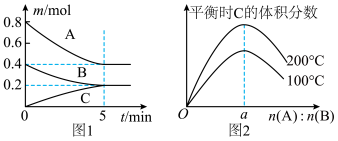
10 . 在体积为 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应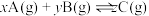 ,图1表示
,图1表示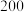 ℃时容器中
℃时容器中 、
、 、
、 物质的量随时间的变化关系,图2表示不同温度下平衡时
物质的量随时间的变化关系,图2表示不同温度下平衡时 的体积分数随起始
的体积分数随起始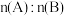 的变化关系。则下列结论正确的是
的变化关系。则下列结论正确的是
 的恒容密闭容器中发生反应
的恒容密闭容器中发生反应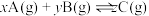 ,图1表示
,图1表示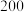 ℃时容器中
℃时容器中 、
、 、
、 物质的量随时间的变化关系,图2表示不同温度下平衡时
物质的量随时间的变化关系,图2表示不同温度下平衡时 的体积分数随起始
的体积分数随起始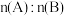 的变化关系。则下列结论正确的是
的变化关系。则下列结论正确的是
A.200℃时,反应从开始到平衡的平均速率 |
B.由图2可知反应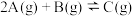 ,正反应吸热且a=2 ,正反应吸热且a=2 |
C.若在图1所示的平衡状态下再向体系中充入 和 和 ,此时 ,此时 |
D.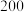 ℃时,向空容器中充入 ℃时,向空容器中充入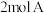 和 和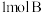 ,达到平衡时 ,达到平衡时 的体积分数小于0.5 的体积分数小于0.5 |
您最近半年使用:0次
2023-04-27更新
|
317次组卷
|
7卷引用:湖南省常德市澧县一中2021-2022学年高三下学期期中考试化学试题
湖南省常德市澧县一中2021-2022学年高三下学期期中考试化学试题湖南省常德市澧县第一中学2021-2022学年高三下学期期中考试化学试题湖南省衡阳县2023届高三3月教学质量诊断性检测考试化学试题上海市实验学校2021-2022学年高三下学期3月月考化学试题(已下线)卷11 化学反应速率和平衡选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)上海市建平中学2023届高三下学期3月月考化学试题山西省实验中学2023-2024学年高二上学期第一次月考化学试题



