名校
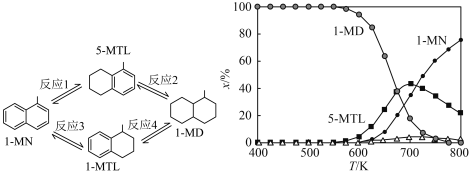
1 . 下图(左)表示1-甲基萘(1-MN)加氢饱和反应网络,四个加氢反应均为放热反应(用反应1、2、3、4表示)。下图(右)表示反应温度(T)对平衡时反应体系中有机化合物物质的量分数(x/%)的影响(6MPa,1-MN和 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法不正确 的是
 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法
| A.800K反应2和反应4生成1-MD的程度很小 |
| B.600K到800K,反应1的平衡常数逐渐减小 |
| C.700K反应1的平衡常数小于反应3的平衡常数 |
| D.600K到650K,反应2中5-MTL增加的量大于反应1中5-MTL减少的量 |
您最近半年使用:0次
名校
解题方法
2 . 在2L恒容密闭容器中充入2molX(g)和1molY(g),发生反应:2X(g)+Y(g) 3Z(g)。反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断不正确的是
3Z(g)。反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断不正确的是

 3Z(g)。反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断不正确的是
3Z(g)。反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示。下列推断不正确的是
| A.该反应为放热反应 | B.升高温度,平衡右移,正反应速率增大,逆反应速率减小 |
| C.Q点时Z的体积分数最大 | D.W、M两点Y的正反应速率W点小于M点 |
您最近半年使用:0次
名校
解题方法
3 . 工业上利用碳热还原 制得
制得 ,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原
,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原 过程中可能发生下列反应
过程中可能发生下列反应
ⅰ.
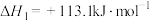
ⅱ.
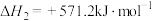
ⅲ.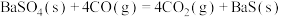
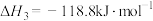

关于碳热还原 的过程,下列说法正确的是
的过程,下列说法正确的是
 制得
制得 ,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原
,进而生产各种含钡化合物。温度对反应后组分的影响如下图。已知:碳热还原 过程中可能发生下列反应
过程中可能发生下列反应ⅰ.

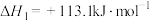
ⅱ.

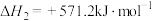
ⅲ.
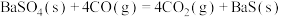
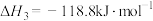

关于碳热还原
 的过程,下列说法正确的是
的过程,下列说法正确的是A.制 的最佳温度应控制在1000℃ 的最佳温度应控制在1000℃ |
| B.400℃之前一定不会发生反应ⅱ |
C.400℃后,反应后组分的变化可能与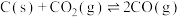 有关 有关 |
D.反应过程中,生成的 和CO的物质的量之和始终等于投入C的物质的量 和CO的物质的量之和始终等于投入C的物质的量 |
您最近半年使用:0次
4 .  的资源化利用是实现我国“双碳”目标的有效途径之一
的资源化利用是实现我国“双碳”目标的有效途径之一
(1)杭州第19届亚洲运动会开幕式主火炬创新使用“零碳”甲醇燃料,综合利用焦炉气中的 与工业尾气中
与工业尾气中 合成绿色甲醇,实现了循环内零碳排放。
合成绿色甲醇,实现了循环内零碳排放。
①制备甲醇的主反应: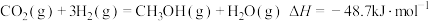 该过程中还存在一个生成
该过程中还存在一个生成 的副反应,结合反应:
的副反应,结合反应:
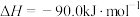 写出该副反应的热化学方程式:
写出该副反应的热化学方程式:___________ 。
②将 和
和 按物质的量比
按物质的量比 混合,以固定流速通过盛放
混合,以固定流速通过盛放 催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。
催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。
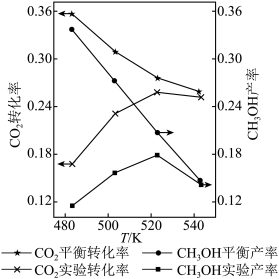
已知:CH3OH产率=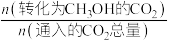
i.催化剂活性最好的温度为___________ 。(填字母序号)
a. 483 K b. 503 K c. 523 K d. 543 K
ii.温度升高时 的平衡转化率降低,解释原因:
的平衡转化率降低,解释原因:___________ 。
iii.温度由 升到543K,CH3OH的实验产率降低,解释原因:
升到543K,CH3OH的实验产率降低,解释原因:___________ 。
(2)近年研究发现,电催化 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含食废水污染问题。向一定浓度的
等)在常温常压下合成尿素,有助于实现碳中和及解决含食废水污染问题。向一定浓度的 溶液通
溶液通 至饱和,在电极上反应生成
至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。

①电极b是电解池的___________ 极。
②电解过程中生成尿素的电极反应式是___________ 。
 的资源化利用是实现我国“双碳”目标的有效途径之一
的资源化利用是实现我国“双碳”目标的有效途径之一(1)杭州第19届亚洲运动会开幕式主火炬创新使用“零碳”甲醇燃料,综合利用焦炉气中的
 与工业尾气中
与工业尾气中 合成绿色甲醇,实现了循环内零碳排放。
合成绿色甲醇,实现了循环内零碳排放。①制备甲醇的主反应:
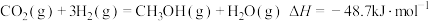 该过程中还存在一个生成
该过程中还存在一个生成 的副反应,结合反应:
的副反应,结合反应:
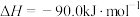 写出该副反应的热化学方程式:
写出该副反应的热化学方程式:②将
 和
和 按物质的量比
按物质的量比 混合,以固定流速通过盛放
混合,以固定流速通过盛放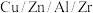 催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。
催化剂的反应器,在相同时间内,不同温度下的实验数据如图所示。
已知:CH3OH产率=
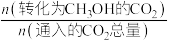
i.催化剂活性最好的温度为
a. 483 K b. 503 K c. 523 K d. 543 K
ii.温度升高时
 的平衡转化率降低,解释原因:
的平衡转化率降低,解释原因:iii.温度由
 升到543K,CH3OH的实验产率降低,解释原因:
升到543K,CH3OH的实验产率降低,解释原因:(2)近年研究发现,电催化
 和含氮物质(
和含氮物质( 等)在常温常压下合成尿素,有助于实现碳中和及解决含食废水污染问题。向一定浓度的
等)在常温常压下合成尿素,有助于实现碳中和及解决含食废水污染问题。向一定浓度的 溶液通
溶液通 至饱和,在电极上反应生成
至饱和,在电极上反应生成 ,电解原理如图所示。
,电解原理如图所示。
①电极b是电解池的
②电解过程中生成尿素的电极反应式是
您最近半年使用:0次
名校
解题方法
5 . 在2L恒容密闭容器中充入2mol X和1mol Y发生反应
 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
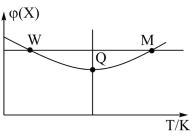

 ,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
,反应过程持续升高温度,测得混合体系中X的体积分数与温度的关系如图所示,下列推断正确的是
| A.Q点时,Y的转化率最大 |
| B.W点X的正反应速率等于M点X的正反应速率 |
| C.升高温度,平衡常数增大 |
| D.平衡时充入Z,达到新平衡时Z的体积分数比原平衡时大 |
您最近半年使用:0次
2023-10-22更新
|
385次组卷
|
3卷引用:北京市顺义区第一中学2023-2024学年高二上学期10月月考化学试题
解题方法
6 . 合成氨是人类科技发展史上的一项重大突破。
(1)在一定条件下, 和
和 反应生成
反应生成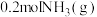 ,放出
,放出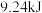 的热量,写出该可逆反应的热化学方程式:
的热量,写出该可逆反应的热化学方程式:_____ 。
(2)将 和
和 通入体积为
通入体积为 的恒温恒容密闭容器中,
的恒温恒容密闭容器中, 后达到化学平衡,测得
后达到化学平衡,测得 的浓度为
的浓度为 ,这段时间内用
,这段时间内用 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为_____ 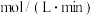 。
。
(3)理论上,为了增大平衡时 的转化率,可采取的措施是
的转化率,可采取的措施是_____ (写出一条)。
(4)下图是某压强下 和
和 按物质的量之比
按物质的量之比 投料进行反应,反应混合物中
投料进行反应,反应混合物中 的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是
的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是_____ 。

A.图中a点,容器内
B.图中 点,
点,
C.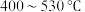 ,Ⅱ中
,Ⅱ中 的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
(1)在一定条件下,
 和
和 反应生成
反应生成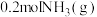 ,放出
,放出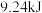 的热量,写出该可逆反应的热化学方程式:
的热量,写出该可逆反应的热化学方程式:(2)将
 和
和 通入体积为
通入体积为 的恒温恒容密闭容器中,
的恒温恒容密闭容器中, 后达到化学平衡,测得
后达到化学平衡,测得 的浓度为
的浓度为 ,这段时间内用
,这段时间内用 的浓度变化表示的化学反应速率为
的浓度变化表示的化学反应速率为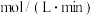 。
。(3)理论上,为了增大平衡时
 的转化率,可采取的措施是
的转化率,可采取的措施是(4)下图是某压强下
 和
和 按物质的量之比
按物质的量之比 投料进行反应,反应混合物中
投料进行反应,反应混合物中 的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是
的物质的量分数随温度的变化曲线。Ⅰ是平衡时的曲线,Ⅱ是不同温度下反应经过相同时间测得的曲线,下列说法正确的是
A.图中a点,容器内

B.图中
 点,
点,
C.
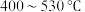 ,Ⅱ中
,Ⅱ中 的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
的物质的量分数随温度升高而增大,原因是升高温度化学反应速率增大
您最近半年使用:0次
名校
解题方法
7 . 烟气中的NOx是大气的主要污染物之一,NOx的吸收处理是当前研究的热点。
(1)还原吸收法
方法1:直接使用尿素[CO(NH2)2]溶液吸收烟气中的NOx。
方法2:先用合适的氧化剂将NOx中的NO氧化为NO2,再用CO(NH2)2溶液去还原吸收。
还原吸收等量的NOx,消耗尿素较多的是___________ (填“方法1”或“方法2”)。工业上选择方法2处理NOx的原因是___________ 。
(2)水吸收法
NO2和N2O4均能被水吸收,不同初始压强下,NO2和N2O4的混合气体被水吸收前和吸收达平衡后,气体中NO2和N2O4的体积分数如图所示。混合气体中与水反应的主要成分是___________ 。达平衡后,气体中的NO2和N2O4的体积分数之和远小于100%,原因是___________ 。

(3)配合物吸收法
钴氨配合物吸收NO的主要原理如下。 对NO的配合能力很强,而
对NO的配合能力很强,而 对NO的配合能力极低。
对NO的配合能力极低。

①与NO反应的 和与
和与 反应的
反应的 物质的量之比为
物质的量之比为___________ 。
②钴氨溶液经过多次循环吸收NO后,其吸收NO的能力会降低,为了恢复钴氨溶液吸收NO的能力,需采取的方法是___________ 。
(4)NO与 在某催化剂表面反应生成
在某催化剂表面反应生成 的过程中,
的过程中, 在催化剂表面能形成被吸附的O(用O-Site表示),接下来的机理可能有两种:
在催化剂表面能形成被吸附的O(用O-Site表示),接下来的机理可能有两种:
机理1: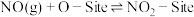
机理2: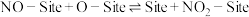
上述两个反应均为基元反应。保持温度和NO的浓度不变,测得NO与 在该催化剂作用下反应的初始速率与
在该催化剂作用下反应的初始速率与 浓度的关系如图所示。能合理解释图中曲线变化的机理为
浓度的关系如图所示。能合理解释图中曲线变化的机理为___________ (填“机理1”或“机理2”);判断的依据是___________ 。

(1)还原吸收法
方法1:直接使用尿素[CO(NH2)2]溶液吸收烟气中的NOx。
方法2:先用合适的氧化剂将NOx中的NO氧化为NO2,再用CO(NH2)2溶液去还原吸收。
还原吸收等量的NOx,消耗尿素较多的是
(2)水吸收法
NO2和N2O4均能被水吸收,不同初始压强下,NO2和N2O4的混合气体被水吸收前和吸收达平衡后,气体中NO2和N2O4的体积分数如图所示。混合气体中与水反应的主要成分是

(3)配合物吸收法
钴氨配合物吸收NO的主要原理如下。
 对NO的配合能力很强,而
对NO的配合能力很强,而 对NO的配合能力极低。
对NO的配合能力极低。
①与NO反应的
 和与
和与 反应的
反应的 物质的量之比为
物质的量之比为②钴氨溶液经过多次循环吸收NO后,其吸收NO的能力会降低,为了恢复钴氨溶液吸收NO的能力,需采取的方法是
(4)NO与
 在某催化剂表面反应生成
在某催化剂表面反应生成 的过程中,
的过程中, 在催化剂表面能形成被吸附的O(用O-Site表示),接下来的机理可能有两种:
在催化剂表面能形成被吸附的O(用O-Site表示),接下来的机理可能有两种:机理1:
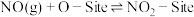
机理2:
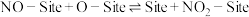
上述两个反应均为基元反应。保持温度和NO的浓度不变,测得NO与
 在该催化剂作用下反应的初始速率与
在该催化剂作用下反应的初始速率与 浓度的关系如图所示。能合理解释图中曲线变化的机理为
浓度的关系如图所示。能合理解释图中曲线变化的机理为
您最近半年使用:0次
2023-06-02更新
|
554次组卷
|
3卷引用:北京交通大学附属中学2023-2024学年高三上学期10月月考化学试题
解题方法
8 . 合成氨在农业和国防中有很重要的意义。
(1)人工固氮有如下两种途径,工业上选用途径二固氮的原因是:_____ 。
途径一:N2(g)+O2(g) 2NO(g) K=5×10-31
2NO(g) K=5×10-31
途径二:N2(g)+3H2(g) 2NH3(g) K=4.1×106
2NH3(g) K=4.1×106
(2)工业合成氨的平衡常数表达式为_____ 。
(3)某探究小组同学在实验室模拟工业合成氨:
①在298K、容积为0.5L的密闭容器内充入一定量的N2和H2,经过10分钟后生成1mol氨气,则v(NH3)=_____ mol/(L·min)。
②在恒容不同温度下,达到平衡时NH3的体积百分数与投料比 的关系图如图所示。
的关系图如图所示。

KA、KB、KC间的大小关系是_____ ,C点H2的平衡转化率为______ 。
(4)在实际工业生产中,常采用下列流程:

①可以用勒夏特列原理解释的措施是_____ 。
a.②④ b.②⑤ c.④⑥ d.③⑤
②原料气是含N2、H2及少量CO、H2O的混合气,净化干燥的原因是_____ 。
A.防止催化剂中毒 B.有利于平衡正向移动 C.提高正反应速率
③研究发现Fe-LiH复合催化剂催化效果明显高于未复合LiH的铁基催化剂,LiH在复合催化剂中是合成氨反应的另一个活性中心,经过以下三步基元反应完成(“*”代表活性中心):
第ⅰ步:N2+2*→2N*
第ⅱ步:N*+LiH→*+[LiNH]
第ⅲ步:……
催化过程中第Ⅲ步的基元反应方程式是______ 。
(5)结合以上所学知识,欲提高工业合成氨产率除了调控压强、温度外,还可采取的合理措施是_____ (至少答出两条)。
(1)人工固氮有如下两种途径,工业上选用途径二固氮的原因是:
途径一:N2(g)+O2(g)
 2NO(g) K=5×10-31
2NO(g) K=5×10-31途径二:N2(g)+3H2(g)
 2NH3(g) K=4.1×106
2NH3(g) K=4.1×106(2)工业合成氨的平衡常数表达式为
(3)某探究小组同学在实验室模拟工业合成氨:
①在298K、容积为0.5L的密闭容器内充入一定量的N2和H2,经过10分钟后生成1mol氨气,则v(NH3)=
②在恒容不同温度下,达到平衡时NH3的体积百分数与投料比
 的关系图如图所示。
的关系图如图所示。
KA、KB、KC间的大小关系是
(4)在实际工业生产中,常采用下列流程:

①可以用勒夏特列原理解释的措施是
a.②④ b.②⑤ c.④⑥ d.③⑤
②原料气是含N2、H2及少量CO、H2O的混合气,净化干燥的原因是
A.防止催化剂中毒 B.有利于平衡正向移动 C.提高正反应速率
③研究发现Fe-LiH复合催化剂催化效果明显高于未复合LiH的铁基催化剂,LiH在复合催化剂中是合成氨反应的另一个活性中心,经过以下三步基元反应完成(“*”代表活性中心):
第ⅰ步:N2+2*→2N*
第ⅱ步:N*+LiH→*+[LiNH]
第ⅲ步:……
催化过程中第Ⅲ步的基元反应方程式是
(5)结合以上所学知识,欲提高工业合成氨产率除了调控压强、温度外,还可采取的合理措施是
您最近半年使用:0次
名校
解题方法
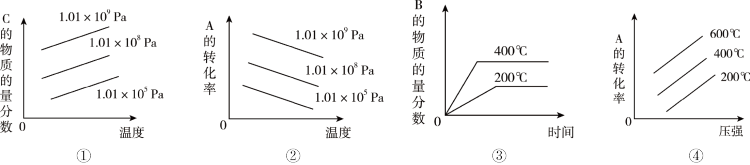
9 . 对于反应: ,下列图像正确的是
,下列图像正确的是
 ,下列图像正确的是
,下列图像正确的是
| A.①④ | B.②③ | C.①③ | D.②④ |
您最近半年使用:0次
2022-11-12更新
|
218次组卷
|
2卷引用:北京市顺义区顺义第一中学2022-2023学年高二上学期期中考试化学试题
名校
解题方法
10 . 二甲醚催化制备乙醇主要涉及以下两个反应:
反应I:CO(g)+CH3OCH3(g)=CH3COOCH3(g)
反应II:CH3COOCH3(g)+2H2(g)=CH3CH2OH(g)+CH3OH(g)
固定CO、CH3OCH3、H2的起始原料比为1∶1∶2、体系压强不变的条件下发生反应I、II,平衡时部分物质的物质的量分数随温度变化如图所示。下列说法不正确 的是

反应I:CO(g)+CH3OCH3(g)=CH3COOCH3(g)
反应II:CH3COOCH3(g)+2H2(g)=CH3CH2OH(g)+CH3OH(g)
固定CO、CH3OCH3、H2的起始原料比为1∶1∶2、体系压强不变的条件下发生反应I、II,平衡时部分物质的物质的量分数随温度变化如图所示。下列说法

| A.反应II为放热反应 |
| B.由图可知,600K以后随温度的升高,氢气物质的量减少 |
| C.曲线C也可以表示CH3OH的物质的量分数 |
| D.由500K上升至600K,温度对反应I的影响大于对反应II的影响 |
您最近半年使用:0次
2022-11-07更新
|
1235次组卷
|
4卷引用:北京师范大学附属中学2022-2023学年高三上学期统练(VII)化学试题



