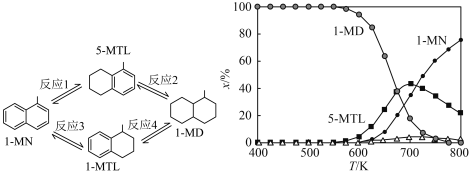
下图(左)表示1-甲基萘(1-MN)加氢饱和反应网络,四个加氢反应均为放热反应(用反应1、2、3、4表示)。下图(右)表示反应温度(T)对平衡时反应体系中有机化合物物质的量分数(x/%)的影响(6MPa,1-MN和 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法不正确 的是
 体积比为1∶5条件下)。下列说法
体积比为1∶5条件下)。下列说法
| A.800K反应2和反应4生成1-MD的程度很小 |
| B.600K到800K,反应1的平衡常数逐渐减小 |
| C.700K反应1的平衡常数小于反应3的平衡常数 |
| D.600K到650K,反应2中5-MTL增加的量大于反应1中5-MTL减少的量 |
更新时间:2024-03-28 21:20:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
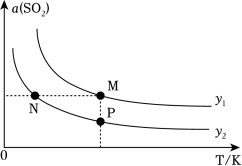
【推荐1】一定压强下,对于反应2CO(g)+SO2(g)⇌S(l)+2CO2(g)ΔH,SO2的平衡转化率[α(SO2)]与投料比的比值[ ]、温度(T)的关系如图所示。下列说法正确的是
]、温度(T)的关系如图所示。下列说法正确的是
 ]、温度(T)的关系如图所示。下列说法正确的是
]、温度(T)的关系如图所示。下列说法正确的是
| A.ΔH>0 | B.温度相同时,y1>y2 |
| C.CO的平衡转化率:N<M | D.逆反应速率:N>P |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知合成氨的热化学方程式为:N2(g)+ 3H2(g) 2NH3(g)△H=-92kJ/mol,下列说法中正确的是
2NH3(g)△H=-92kJ/mol,下列说法中正确的是
 2NH3(g)△H=-92kJ/mol,下列说法中正确的是
2NH3(g)△H=-92kJ/mol,下列说法中正确的是| A.当1molN2与3molH2充分反应,可放出92kJ热量 |
| B.恒容恒温发生该反应时,向容器中充入少量He,反应速率加快且平衡正向移动 |
| C.恒压恒温发生该反应时,向容器中充入少量He,反应速率不变且平衡不移动 |
| D.升高温度时,正、逆反应速率都加快,而逆反应速率增加更多 |
您最近半年使用:0次
【推荐3】在3种不同条件下,分别向容积为2 L的恒容密闭容器中充入2 mol A和1 mol B,发生反应2A(g) +B(g) 2D(g) ΔH=-QkJ· mol-1。实验的相关条件和数据如下表所示:
2D(g) ΔH=-QkJ· mol-1。实验的相关条件和数据如下表所示:
下列说法正确的是
 2D(g) ΔH=-QkJ· mol-1。实验的相关条件和数据如下表所示:
2D(g) ΔH=-QkJ· mol-1。实验的相关条件和数据如下表所示: | 实验编号 | 实验I | 实验II | 实验III |
| 反应温度/°C | 800 | 800 | 850 |
| 达到平衡时间/min | 40 | 10 | 30 |
| 平衡时c(D)/(mol·L-1) | 0.5 | 0.5 | 0.15 |
| 反应的能量变化 | Q1 | Q2 | Q3 |
| A.可用压强或密度是否发生变化判断上述反应是否达到平衡状态 |
| B.实验I达到平衡后,恒温条件下再向容器中通入1 mol A和1 mol D, 达到平衡时,c(D) = 1.0mol·L-1 |
| C.实验II可能隐含的条件是使用催化剂,实验III达到平衡时,v(D) = 0.05mol ·L-1 ·min-1 |
| D.由表中信息可知:Q>0,并且有Q1=Q2<Q3<Q |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】K、Ka、KW分别表示化学平衡常数、电离平衡常数和水的离子积常数,下列判断正确的是
| A.温度升高,三者都增大 |
| B.化学平衡常数的大小与温度、浓度、催化剂等有关 |
| C.室温下Ka(HCN)<Ka(HF),说明HF的电离度比HCN大 |
D.2SO2(g)+O2(g) 2SO3(g)平衡后,仅增大压强,平衡向右移动,K值不变 2SO3(g)平衡后,仅增大压强,平衡向右移动,K值不变 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】化学平衡常数(K)、电离常数(Ka、Kb)、水的离子积常数(Kw)、溶度积常数(Ksp)等常数是表示判断物质性质的重要常数,下列关于这些常数的说法中,正确的是

| A.化学平衡常数的大小与温度、浓度、压强有关,与催化剂无关 |
| B.Ka(HCN)<Ka(CH3COOH)说明相同物质的量浓度时,氢氰酸的酸性比醋酸的强 |
| C.当温度升高时,弱酸、弱碱的电离常数(Ka、Kb)和水的离子积常数(Kw)均变大 |
D.向氯化钡溶液中加入等体积同浓度的碳酸钠和硫酸钠溶液,先产生 沉淀,则Ksp(BaSO4)>Ksp(BaCO3) 沉淀,则Ksp(BaSO4)>Ksp(BaCO3) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下图所示与对应叙述相符的是
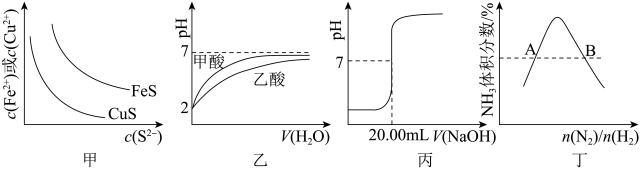

| A.图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,Ksp(FeS)>Ksp(CuS) |
| B.图乙表示pH=2的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸<乙酸 |
| C.图丙表示用0.1000 mol·L-lNaOH溶液滴定20.00 mL硫酸的滴定曲线,则c(H2SO4)=0.1000 mol·L-1 |
| D.图丁表示反应N2(g)+3H2(g)⇌2NH3(g)平衡时NH3体积分数随起始n(N2)/n(H2)变化的曲线,则转化率:αA(H2)=αB(H2) |
您最近半年使用:0次
单选题
|
适中
(0.65)
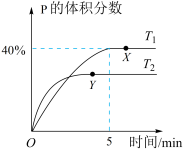
【推荐2】将1molM和2 molN置于体积为2L的恒容密闭容器中,发生反应:M(s)+2N(g) P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
 P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
P(g)+Q(g) △H。反应过程中测得P的体积分数在不同温度下随时间的变化如图所示。下列说法正确的是( )
| A.若X、Y两点的平衡常数分别为K1、K2,则K1<K2 |
| B.温度为T1时,N的平衡转化率为80%,平衡常数K=4.0 |
| C.无论T1还是T2,当容器中混合气体平均摩尔质量和压强不变时,反应达平衡状态 |
| D.降低温度、增大压强、及时分离出产物均有利于提高反应物的平衡转化率 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
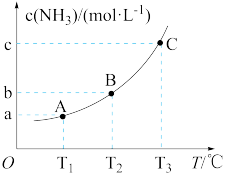
【推荐3】向体积为V1L的密闭容器中充入x mol NH3、x mol NO和y mol O2,x :y=4: 1,模拟SNCR- SCR脱硝技术,主要反应为4NH3(g) +4NO(g) + O2(g)  4N2(g)+ 6H2O(g) △H= -1 632.4 kJ·mol-1,达到平衡时c(NH3)与温度T的关系如下图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3。下列说法正确的是
4N2(g)+ 6H2O(g) △H= -1 632.4 kJ·mol-1,达到平衡时c(NH3)与温度T的关系如下图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3。下列说法正确的是
 4N2(g)+ 6H2O(g) △H= -1 632.4 kJ·mol-1,达到平衡时c(NH3)与温度T的关系如下图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3。下列说法正确的是
4N2(g)+ 6H2O(g) △H= -1 632.4 kJ·mol-1,达到平衡时c(NH3)与温度T的关系如下图所示。若T1、T2、T3时的平衡常数分别为K1、K2、K3。下列说法正确的是
| A.K1<K3 |
B.T2时,若保持温度不变,容器体积由V1 L缩小到V2 L,则平衡后c(N2)小于(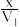 -b)mol·L-1 -b)mol·L-1 |
| C.若保持体系绝热,容积不变,T3时发生反应,平衡后c(NH3)对应的点在C点右下方 |
| D.反应开始后的一段时间内,适当升高温度可提高单位时间内NH3的转化率 |
您最近半年使用:0次

 在密闭容器中达到平衡,下列说法正确的是
在密闭容器中达到平衡,下列说法正确的是 ,平衡常数增大
,平衡常数增大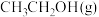 的浓度增大
的浓度增大 ,平衡向正反应方向移动
,平衡向正反应方向移动 ,
,

