碳酸钠作固硫剂并用氢还原辉钼矿的原理为MoS2(s)+4H2(g)+2Na2CO3(s) Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。

(1)该反应的平衡常数表达式为K=___ 。
(2)由图1可知,该反应ΔH__ 0(填“>”或“<”),p1、p2、p3由大到小的顺序为___ 。
(3)由图2可知,A点时H2的平衡转化率为___ 。
 Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。
Mo(s)+2CO(g)+4H2O(g)+2Na2S(s) ΔH,实验测得平衡时的有关变化曲线如图所示。
(1)该反应的平衡常数表达式为K=
(2)由图1可知,该反应ΔH
(3)由图2可知,A点时H2的平衡转化率为
更新时间:2020-05-16 13:29:05
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐1】某可逆反应在某体积为2 L的密闭容器中进行,从0~3分钟各物质的量的变化情况如图所示(A为固体、B、C为气体):

(1)反应开始至2分钟时,B的平均反应速率为_______ 。
(2)此反应的化学平衡常数表达式为_______ 。
(3)在密闭容器里,加入一定量的A、B、C,发生上述反应,当改变条件时,反应速率会加快的是_______ (填序号)。
①增大容器体积②加入催化剂③降低温度④增加A的浓度

(1)反应开始至2分钟时,B的平均反应速率为
(2)此反应的化学平衡常数表达式为
(3)在密闭容器里,加入一定量的A、B、C,发生上述反应,当改变条件时,反应速率会加快的是
①增大容器体积②加入催化剂③降低温度④增加A的浓度
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】工业合成氨的反应为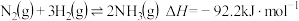 ,其部分工艺流程如图所示。
,其部分工艺流程如图所示。

反应体系中各组分的部分性质如表所示。
回答下列问题:
(1)该反应的化学平衡常数表达式K=_________ 。随着温度升高,K值________ (填“增大”“减小”或“不变”)。
(2)合成氨反应的平衡常数很小,所以在工业上将气体循环利用,即反应后通过把混合气体的温度降低到_________ ,将________ 分离出来;继续循环利用的气体是_________ 。
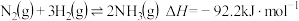 ,其部分工艺流程如图所示。
,其部分工艺流程如图所示。
反应体系中各组分的部分性质如表所示。
| 气体 |  |  |  |
| 熔点/℃ | 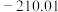 |  | 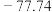 |
| 沸点/℃ | 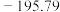 | 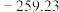 | 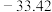 |
(1)该反应的化学平衡常数表达式K=
(2)合成氨反应的平衡常数很小,所以在工业上将气体循环利用,即反应后通过把混合气体的温度降低到
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】水煤气(CO和H2)是合成甲醇的重要原料,它可用水蒸气通过炽热的炭层制得:C(s)+H2O(g) CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
(1)该反应的平衡常数的表达式为_________________ ;升高温度,K值将________ ;容器中气体的平均相对分子质量将________ 。(填“增大”、“减小”或“不变”)。
(2)上述反应达到平衡后,将体系中的C(s)部分移走,平衡将________ (填字母)。
A.向左移 B.向右移 C.不移动
(3)下列事实能说明该反应在一定条件下已达到平衡状态的有________ (填字母)。
A.单位体积内每消耗1 mol CO的同时生成1 mol H2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
(4)某温度下,将4.0 mol H2O(g)和足量的炭充入2 L的密闭容器中,发生如下反应,C(s)+H2O(g) CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为________ 。
 CO(g)+H2(g) ΔH=+131.3 kJ·mol-1
CO(g)+H2(g) ΔH=+131.3 kJ·mol-1(1)该反应的平衡常数的表达式为
(2)上述反应达到平衡后,将体系中的C(s)部分移走,平衡将
A.向左移 B.向右移 C.不移动
(3)下列事实能说明该反应在一定条件下已达到平衡状态的有
A.单位体积内每消耗1 mol CO的同时生成1 mol H2
B.混合气体总物质的量保持不变
C.生成H2O(g)的速率与消耗CO的速率相等
D.H2O(g)、CO、H2的浓度相等
(4)某温度下,将4.0 mol H2O(g)和足量的炭充入2 L的密闭容器中,发生如下反应,C(s)+H2O(g)
 CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为
CO(g)+H2(g),达到平衡时测得K=1,则此温度下H2O(g)的转化率为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】I.把6molA气体和5molB气体混合放入4L密闭容器中,在一定条件下发生反应: ,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:
,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:
(1)B的转化率___________ 。
(2)恒温达平衡时容器内的压强与开始时压强比___________ 。
Ⅱ.化学电池在通讯,交通及日常生活中有着广泛的应用。
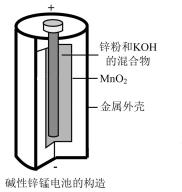
(3)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是___________ (填名称),负极上发生的电极反应为___________ 。若反应消耗13g负极材料,则电池中转移电子的物质的量为___________ mol。
(4)铅蓄电池是典型的可充电电池,它的正、负极格板都是惰性材料,电池总反应式为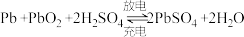 。下列说法正确的是___________(填标号)。
。下列说法正确的是___________(填标号)。
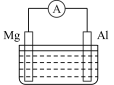
(5)镁铝电池的构造如图所示,当电解质溶液为NaOH溶液时,可知电池的负极材料为_______ (填“Mg”或“Al”),正极上的电极反应式为___________ 。
 ,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:
,经5min达到平衡,此时生成C为2mol,测定D的平均反应速率为0.1mol/(L·min),计算:(1)B的转化率
(2)恒温达平衡时容器内的压强与开始时压强比
Ⅱ.化学电池在通讯,交通及日常生活中有着广泛的应用。
(3)碱性锌锰干电池(如图所示)是应用最普遍的电池之一,电池总反应为
 ,碱性锌锰干电池的负极材料是
,碱性锌锰干电池的负极材料是
(4)铅蓄电池是典型的可充电电池,它的正、负极格板都是惰性材料,电池总反应式为
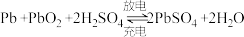 。下列说法正确的是___________(填标号)。
。下列说法正确的是___________(填标号)。| A.电解液中H2SO4的浓度始终保持不变 |
B.放电时正极上的电极反应式为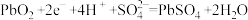 |
| C.放电时,当外电路通过1mol电子时,理论上负极质量增加48g |
D.放电时,溶液中的 向正极移动 向正极移动 |

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】某温度时,在一个2L的密闭容器中,X、Y、Z三种气体物质的物质的量随时间的变化曲线如图所示。根据图中数据,试填写下列空白:

(1)该反应的化学方程式为_______ 。
(2)反应开始~2min,气体X的平均反应速率为_______ 。
(3)反应开始~2min,气体Y的转化率为_______
(4)此反应在四种不同情况下的反应速率分别为:①v(X)=5mol/(L·min)②v(Y)=0.05mol/(L·s)③v(Z)=4.5mol/(L·min),其中反应速率最快的是_______ (填编号)。

(1)该反应的化学方程式为
(2)反应开始~2min,气体X的平均反应速率为
(3)反应开始~2min,气体Y的转化率为
(4)此反应在四种不同情况下的反应速率分别为:①v(X)=5mol/(L·min)②v(Y)=0.05mol/(L·s)③v(Z)=4.5mol/(L·min),其中反应速率最快的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+ 6CO(g)。
Si3N4(s)+ 6CO(g)。
(1)该反应的氧化剂是________ ,该反应的平衡常数表达式为K=________ 。
(2)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率 与时间t的关系如图。
与时间t的关系如图。
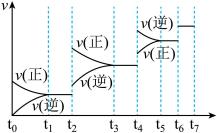
若t2时改变的条件为加热,则此反应的反应热ΔH______ 0(填“>”、“<”或“=”);降低温度,其平衡常数值_______ (填“增大”、“减小”或“不变”);
(3)t4时引起平衡移动的条件可能是_______ ;图中表示平衡混合物中CO的含量最高的时间段是______ 。
(4)若该反应的平衡常数为 K=729,则在同温度下1L固定密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是_______ (提示:272 = 729);若平衡后再向此容器中加入3molN2,N2的转化率将______ (填“增大”、“减小”或“不变”)。
 Si3N4(s)+ 6CO(g)。
Si3N4(s)+ 6CO(g)。(1)该反应的氧化剂是
(2)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率
 与时间t的关系如图。
与时间t的关系如图。
若t2时改变的条件为加热,则此反应的反应热ΔH
(3)t4时引起平衡移动的条件可能是
(4)若该反应的平衡常数为 K=729,则在同温度下1L固定密闭容器中,足量的SiO2和C与2mol N2充分反应,则N2的转化率是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度):

(1)图像中 和
和 的关系是:
的关系是:
_______  (填“>、<或=”)。
(填“>、<或=”)。
(2)a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是_______ (填字母)。

(1)图像中
 和
和 的关系是:
的关系是:
 (填“>、<或=”)。
(填“>、<或=”)。(2)a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】甲醇是一种重要的化工原料又是一种可再生能源,具有开发和应用的广阔前景。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g) CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
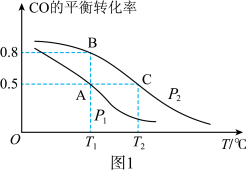
由图可判断△H____ 0,A、B两点对应的平衡常数关系是KA____ KB(填“>、<、=”)。
(2)某温度下,充分反应后,达到平衡时测得c(CO)=0.02mol/L,则此温度下的平衡常数K=____ 。
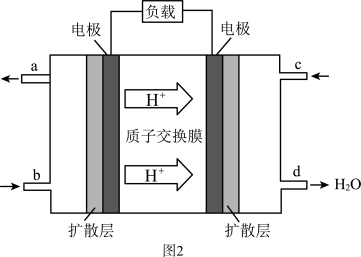
(3)我国在甲醇燃料电池技术方面获得新突破,组装出自呼吸电池及主动式电池。其工作原理如图2所示。该电池工作时,c口通入的物质为___  (填化学式)
(填化学式) ;电池负极的电极反应式为
;电池负极的电极反应式为____ 。
(1)在一容积为2L的密闭容器内,充入0.2molCO与0.4molH2发生反应,CO(g)+2H2(g)
 CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
CH3OH(g),CO的平衡转化率与温度,压强的关系如图1所示。
由图可判断△H
(2)某温度下,充分反应后,达到平衡时测得c(CO)=0.02mol/L,则此温度下的平衡常数K=
(3)我国在甲醇燃料电池技术方面获得新突破,组装出自呼吸电池及主动式电池。其工作原理如图2所示。该电池工作时,c口通入的物质为
 (填化学式)
(填化学式) ;电池负极的电极反应式为
;电池负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】科学家正致力于研究一种“碳中和”技术—(CH4CO2)重整,该技术具有一定的经济效益和深远的社会意义。其工艺过程中涉及如下反应:
I:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1=+234kJ·mol-1
II:H2(g)+CO2(g)⇌H2O(g)+CO(g) ΔH2=+41kJ·mol-1
将1molCH4与1molCO2在2L密闭容器中反应制取CO和H2时,CH4和CO2的平衡转化率随温度变化关系如图所示。

(1)923K时CO2的平衡转化率大于CH4的原因是______________________ 。
(2)1200K以上CO2和CH4的平衡转化率趋于相等的原因可能是______________________ 。
I:CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH1=+234kJ·mol-1
II:H2(g)+CO2(g)⇌H2O(g)+CO(g) ΔH2=+41kJ·mol-1
将1molCH4与1molCO2在2L密闭容器中反应制取CO和H2时,CH4和CO2的平衡转化率随温度变化关系如图所示。

(1)923K时CO2的平衡转化率大于CH4的原因是
(2)1200K以上CO2和CH4的平衡转化率趋于相等的原因可能是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】密闭容器中mA(g)+nB(g)  pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如下图。则:
pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如下图。则:

(1)增大压强,A的转化率___________ 平衡向___________ 移动,达到平衡后,混合物中C的浓度___________ 。
(2)上述化学方程式中的系数m、n、p的正确关系是___________ ,
(3)当降低温度时,C的浓度减小,正反应是___________ 热反应。
 pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如下图。则:
pC(g),反应达到平衡,经测定增大压强P时,A的转化率随P而变化的曲线如下图。则:
(1)增大压强,A的转化率
(2)上述化学方程式中的系数m、n、p的正确关系是
(3)当降低温度时,C的浓度减小,正反应是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】二氧化碳的转化和利用成为实现“碳达峰”、“碳中和”的重要研究课题。回答下列问题:
(1)利用CO2和H2可生产乙烯。相关热化学方程式为:
反应I:2CO2(g)+6H2(g) CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1
CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1
反应II:CO2(g)+4H2(g) CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1
CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1
某催化剂作用下,在容积为2.0L的恒容密闭容器中充入lmolCO2和3molH2,体系中主要发生上述反应I和反应II两个竞争反应。反应进行tmin时测得两种烃的物质的量随温度的变化如图所示,该催化剂在840℃时主要选择反应________ (填“I”或“II”);840℃之后,C2H4产量下降的原因是_______ 。

520℃时,0~tmin内用氢气表示反应II的平均反应速率:υ(H2)=_______ mol/(L·min)(用含t的代数式表示)。
(2)利用工业废气CO2制甲醇,发生反应III:CO2(g)+3H2(g) CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。
CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。
①上述反应自发的条件是________ 。
②在aL密闭容器中,充入不同氢碳比的原料气体,控制温度600K,发生反应III,请在图中画出CH3OH在混合气体中的平衡体积分数随氢碳比递增的变化趋势_________ 。

③一定条件下,将1molCO2和1molH2置于恒容密闭容器中,发生反应III。下列能说明反应达到平衡状态的是_________ 。
A.混合气体的密度保持不变
B.CO2的消耗速率与H2O的消耗速率相等
C.CO2的体积分数保持不变
D.混合气体的平均相对分子质量保持不变
(1)利用CO2和H2可生产乙烯。相关热化学方程式为:
反应I:2CO2(g)+6H2(g)
 CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1
CH2=CH2(g)+4H2O(g) △H1=−246.4 kJ∙mol−1反应II:CO2(g)+4H2(g)
 CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1
CH4(g)+2H2O(g) △H2=−166.8 kJ∙mol−1某催化剂作用下,在容积为2.0L的恒容密闭容器中充入lmolCO2和3molH2,体系中主要发生上述反应I和反应II两个竞争反应。反应进行tmin时测得两种烃的物质的量随温度的变化如图所示,该催化剂在840℃时主要选择反应

520℃时,0~tmin内用氢气表示反应II的平均反应速率:υ(H2)=
(2)利用工业废气CO2制甲醇,发生反应III:CO2(g)+3H2(g)
 CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。
CH3OH(g)+H2O(g) △H3<0,可一定程度摆脱当下对化石燃料的依赖。①上述反应自发的条件是
②在aL密闭容器中,充入不同氢碳比的原料气体,控制温度600K,发生反应III,请在图中画出CH3OH在混合气体中的平衡体积分数随氢碳比递增的变化趋势

③一定条件下,将1molCO2和1molH2置于恒容密闭容器中,发生反应III。下列能说明反应达到平衡状态的是
A.混合气体的密度保持不变
B.CO2的消耗速率与H2O的消耗速率相等
C.CO2的体积分数保持不变
D.混合气体的平均相对分子质量保持不变
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】向1L恒容密闭容器中充入3molCO2、7molH2的混合气体,控制适当条件发生反应: 。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
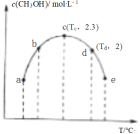
回答下列问题:
(1)第10min时,正反应速率υ(c)_______ (填“>”“<”或“=”,下同)υ(d),c点处对应反应体系中c(H2)=_______  。
。
(2)该反应的
_______ (填“>”或“<”)0,a、b、c、d、e五点对应温度下,反应肯定处于非平衡状态的是_______ (填字母)。
(3)实际生产中,通常会采用下列方法以提高单位时间内CH3OH的产率_______(填字母)。
(4)若d点时容器总压为12kPa,则Kp=_______ (用平衡分压代替平衡浓度,分压=总压 物质的量分数)。
物质的量分数)。
 。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
。如图为不同温度下,反应经过10min时容器中c(CH3OH)变化情况。
回答下列问题:
(1)第10min时,正反应速率υ(c)
 。
。(2)该反应的

(3)实际生产中,通常会采用下列方法以提高单位时间内CH3OH的产率_______(填字母)。
| A.使用催化剂 | B.不断分离出产物 |
| C.低温下进行反应 | D.不断补充原料 |
 物质的量分数)。
物质的量分数)。
您最近一年使用:0次



