名校
解题方法
1 . 对于可逆反应 ,下列研究目的和图示相符的是
,下列研究目的和图示相符的是
 ,下列研究目的和图示相符的是
,下列研究目的和图示相符的是 |  |  |  | |
| 研究 目的 | 压强对反应的影响 | 温度对反应的影响 | 平衡体系增加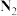 对反应的影响 对反应的影响 | 催化剂对反应的影响 |
| 图示 |
|
|
|
|
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2023-11-16更新
|
359次组卷
|
155卷引用:甘肃省庆阳市第六中学2020-2021学年高二上学期期末考试化学试题
甘肃省庆阳市第六中学2020-2021学年高二上学期期末考试化学试题甘肃省兰州新舟中学2017-2018学年高二上学期第二次月考化学试题甘肃省武威市第六中学2019-2020学年高二上学期第一次学段考试化学试题甘肃省庆阳市宁县第二中学2019-2020学年高二下学期期中考试化学试题(萃英班)辽宁省丹东市2020-2021学年高二上学期期末考试化学试题湖北省沙市中学2020-2021学年高二上学期期末考试化学试题吉林省延边朝鲜族自治州汪清县第四中学2020-2021学年高二上学期期末考试化学试题内蒙古自治区土默特左旗第三中学2020-2021学年高二上学期期末考试化学试题广东省广州市荔湾区广州市西关外国语学校2020—2021学年高二培优选拔测试化学试题江苏省吴江汾湖高级中学2020-2021学年高二下学期阶段性教学质量检测化学试题云南省曲靖市马龙二中2020-2021学年高二5月月考化学试题(已下线)专题2.4 化学反应的调控(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)安徽省合肥新城高升学校2021-2022学年高二上学期第一次月考化学试题山东省潍坊市临朐县实验中学2021-2022学年高二上学期9月月考化学试题黑龙江省大庆中学2021-2022学年高二上学期第一次月考化学试题重庆市育才中学校2021-2022学年高二上学期第一次月考化学试题四川省广安市武胜烈面中学校2021-2022学年高二10月月考化学试题重庆市永川景圣中学校2021-2022学年高二上学期第一次月考化学试题河南省平顶山九校联盟2021-2022学年高二上学期期中考试化学试题山东省泰安肥城市2021-2022学年高二上学期期中考试化学试题吉林省白城市第一中学2021-2022学年高二上学期期中考试化学试题天津市第二十一中学2021-2022学年高二上学期期中检测化学试题(已下线)2.4 化学反应的调控(素养提优B练)-2021-2022学年高二化学课时过关提优AB练(人教版2019选择性必修1)(已下线)2.3.3 化学平衡中的图像问题(备作业)-【上好课】2021-2022学年高二化学同步备课系列(苏教版2019选择性必修1)福建省福州铜盘中学2021-2022学年高二上学期12月月考化学试题陕西省渭南市咸林中学2021-2022学年高二上学期第三阶段检测化学试题河北省张家口市第一中学2021-2022学年高二上学期10月月考化学试题吉林省松原市长岭县第三中学2021-2022学年高二上学期第三次考试化学试题湖北省南漳县第二中学2021-2022学年高二上学期期中考试化学试题陕西省西安市雁塔区第二中学2021-2022学年高二上学期第一次月考化学试题四川省成都市东部新区养马高级中学2021-2022学年高二上学期期中考试化学试题湖北省黄石市有色第一中学2021-2022学年高二上学期期中考试化学试题(已下线)2010年广西柳州二中高三第三次模拟考试(理科综合)化学部分(已下线)2010-2011学年浙江省台州市高二下学期六校期中联考化学试卷(已下线)2011届浙江省学军中学高三上学期期中考试化学试题(已下线)2011-2012学年辽宁省沈阳二中高二上学期期中考试化学试卷(已下线)2011-2012学年江西省南昌市四校高二第二次联考化学试卷(已下线)2012届江西省上饶县中学高三上学期第三次月考化学试卷(普)(已下线)2012届江苏省如皋中学高三下学期质量检测化学试卷(已下线)2011-2012学年浙江省蓬街私立中学高二下学期第一次月考化学试卷(已下线)2011-2012年安徽红星中安工大附中高二下学期期中联考理科化学试卷(已下线)2011-2012年江苏无锡市洛社高级中学高二下学期期中考试化学试卷(已下线)2011-2012学年浙江省杭州地区七校高二下学期期中联考化学试卷(已下线)2014届浙江省温州市十校联合体高三上学期期中联考化学试卷(已下线)2013-2014学年贵州省重点高中高二上学期期中考试理科化学试卷(已下线)2014届高考化学三轮复习排查 专题6化学反应速率和化学平衡练习卷2015届山东省潍坊市重点中学高三12月月考化学试卷2015届吉林省吉林市一中高三3月教与学质量检测一化学试卷2015-2016学年四川省雅安中学高二上期中考试化学试卷2016届吉林省吉林一中高三上质量检测(六)化学试卷2015-2016学年安徽省合肥中科大附中高二下期中理科化学试卷2015-2016学年广西南宁市八中高二下学期期中段考化学试卷2015-2016学年湖北省天门、仙桃、潜江市高一下学期期末化学试卷2016-2017学年陕西省西安一中高二上10月月考化学卷2016-2017学年安徽省合肥一中高二上月考一化学试卷2016-2017学年四川省成都外国语学校高二上10月月考化学试卷2016-2017学年河南省漯河中学高二上第一次月考化学卷2016-2017学年湖北省蕲春县高二上学期期中化学试卷河北省大名县第一中学2017-2018学年高二上学期第一次月考化学试题辽宁省六校协作体2017-2018学年高二上学期期中考试化学试题黑龙江省哈尔滨市第三中学2018届高三上学期(10月)第二次验收考试化学试题2017.11辽宁省六校协作体高二期中化学试卷高中化学人教版 选修四 第二章 化学反应速率和化学平衡 第三节 化学平衡 化学平衡第二课时(化学平衡状态)内蒙古杭锦后旗奋斗中学2017-2018学年高二下学期第一次月考化学试题【全国百强校】黑龙江省哈尔滨师范大学附属中学2017-2018学年高一下学期期末考试(理)化学试题陕西省黄陵中学2017-2018学年高一(重点班)下学期期末考试化学试题【全国百强校】黑龙江省双鸭山市第一中学2018-2019学年高二上学期第一次月考化学试题山西省长治二中2018-2019学年高二上学期第一次月考化学试题吉林省长春市田家炳实验中学2018-2019学年高二上学期第一学程检测化学试题【全国百强校】陕西省西安市第一中学2018-2019学年高二上学期10月月考化学试题【全国百强校】内蒙古集宁一中(西校区)2018-2019学年高二上学期期中考试化学试题山西省吕梁市高级中学2018-2019学年高二上学期期中考试化学试题高二人教版选修4 第二章 章末基础排查(二)【全国百强校】宁夏回族自治区银川市第一中学2018-2019学年高二上学期期末考试化学试题宁夏回族自治区长庆高级中学2018-2019学年高二上学期期末考试化学试题【市级联考】四川省达州市2018-2019学年高二上学期期末检测化学试题四川省德阳市第五中学2018-2019学年高二下学期第一次月考化学试题【全国百强校】辽宁省鞍山市第一中学2018-2019学年高二下学期开学考试化学试题黑龙江省双鸭山市第一中学2019-2020学年高二上学期第一次月考化学试题天津市静海区独流中学等四校2019-2020学年高二10月联考化学试题新疆乌鲁木齐市第四中学2019-2020学年高二上学期期中考试化学试题安徽省合肥市一六八中学2019-2020学年高二上学期期中考试化学试题新疆生产建设兵团第七师高级中学2019-2020学年高二上学期第二次月考化学试题福建省漳平市第一中学2019-2020学年高二上学期期中考试化学试题广东省揭阳市惠来县第一中学2019-2020学年高二上学期第二次阶段考试化学试题河北省鸡泽县第一中学2019-2020学年高二12月月考化学试题湖南省长沙市长郡中学2018-2019学年高二上学期期末考试化学试题陕西省黄陵中学2019-2020学年高二上学期期末考试(普通班)化学试题宁夏育才中学2019-2020学年高二上学期期末考试化学试题2020届高三化学二轮冲刺新题专练——影响化学反应速率的因素青海省西宁市第十四中学2019-2020学年高二上学期期末考试化学试题安徽省合肥市一六八中学2019-2020学年高二上学期期末考试化学试题陕西省渭南市大荔县2019-2020学年高二上学期期末教学质量检测化学试题黑龙江省安达市第七中学2019-2020学年高二3月月考化学试题陕西省榆林市绥德县绥德中学2019-2020高二下学期第一次阶段性测试化学试题辽宁省营口市第二高级中学2019-2020学年高二上学期第一次月考化学试题浙江省桐庐分水高级中学2018-2019学年高二下学期期中考试化学试题(已下线)第02章 化学反应速率与化学平衡(B卷能力提高篇)-2020-2021学年高二化学选择性必修1同步单元AB卷(新教材人教版)鲁科版(2019)选择性必修1 第2章 化学反应的方向、限度与速率 章末综合检测卷湖北省部分重点中学(郧阳中学、恩施高中、随州二中、沙市中学)2020-2021学年高二上学期联考化学试题重庆市缙云教育联盟2020-2021学年高一上学期10月月考化学试题内蒙古包头市第一中学2020-2021学年高二上学期第一次月考化学试题安徽省滁州市明光县明光中学2020-2021学年高二上学期第一次月考化学试题重庆市合川实验中学2020-2021学年高二上学期期中考试化学试题贵州省思南中学2020-2021学年高二上学期期中考试化学试题人教版(2019)高二化学选择性必修1第二章 化学反应速率与化学平衡 第四节 化学反应的调控福建省南平市高级中学2020-2021学年高二上学期期中考试化学(选考)试题内蒙古自治区乌兰察布市四子王旗第一中学2020-2021学年高二上学期期中考试化学试题河南省郑州市郑州中学2020-2021学年高二上学期期中考试化学试题江西省九江市浔阳区九江市第七中学2020-2021学年高二上学期期中考试化学试题广西玉林师院附中、玉林十一中等五校2020-2021学年高二上学期教学质量评价理综化学试题辽宁省大连市普兰店区第三十八中学2020-2021学年高二上学期第三次月考化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP415(1)】【化学】安徽省合肥市第七中学2020-2021学年高二上学期第一次段考化学试卷(已下线)【浙江新东方】98山东省泰安市新泰第一中学(东校)2020-2021学年高二上学期期中考试化学试题辽宁省辽河油田第二高级中学2020-2021学年高二上学期期中考试化学试题(已下线)练习7 化学平衡(二)-2020-2021学年【补习教材·寒假作业】高二化学(人教版)黑龙江省哈尔滨市宾县第一中学2021届高三上学期第三次月考化学试题广东省东莞市光明中学2020-2021学年高二上学期期中考试化学试题云南省玉溪第二中学2020-2021学年高二上学期期中质量检测化学试题陕西省眉县槐芽中学2020-2021学年高二上学期期中考试化学试题辽宁省滨海实验中学2019-2020学年高二上学期期末化学试题江西省新余市2021-2022学年高二上学期期末检测化学试题河南省中原名校联盟2021-2022学年高二上学期第三次适应性联考化学试题广东省珠海市2021-2022学年高二上学期期末考试化学试题广西民族高中2021-2022学年高二下学期3月月考化学试题山东省泰安一中新校2022-2023学年高二上学期10月质量检测化学试题黑龙江省牡丹江市海林市朝鲜族中学2022-2023学年高二上学期第一次月考化学试题河北省石家庄市第十八中学2022-2023学年高二上学期10月月考化学试题山东省枣庄市第三中学(实验班)2022-2023学年高二11月线上测试化学试题江西省宜春市丰城市东煌学校2022-2023学年高二上学期期中考试化学试卷广西百色民族高级中学2022-2023学年高二上学期10月阶段检测化学试题湖北省孝感市云梦县黄香高级中学2021-2022学年高二上学期期末考试化学试题四川省资阳中学2022-2023学年高二上学期期末考试化学试题广西河池八校同盟体2022-2023学年高二下学期5月月考化学试题章末检测卷(二)化学反应的方向、限度与速率安徽省芜湖市无为襄安中学2022-2023学年高二上学期11月期中考试化学试题山东省泰安新泰市第一中学(实验部)2023-2024学年高二上学期第一次质量检测化学试题浙江省舟山中学2023-2024学年高二上学期10月月考化学试题贵州省贵阳市清华中学2022-2023学年高二上学期11月月考化学试题浙江省杭州市“六县九校”联盟2023-2024学年高二上学期11月期中考试化学试题河北省唐山市丰润区2023-2024学年高二上学期期中考试化学试题 福建省龙岩市连城县第一中学2023-2024学年高二上学期10月月考化学试题湖南省长沙市周南中学2024届高三上学期第三次阶段性测试化学试题广东省广州市三校2023—2024学年高二上学期期中联考化学考试四川省仁寿第一中学校南校区2023-2024学年高二上学期10月月考化学试题陕西省汉中市乡县第一中学2023-2024学年高二上学期10月月考化学试题辽宁省辽西联合校2023-2024学年高二上学期期中考试化学试题山东省济宁市泗水县2023-2024学年高二上学期期中考试化学试题四川省南充市嘉陵第一中学2023-2024学年高二上学期10月月考化学试题四川省眉山市彭山区第一中学2023-2024学年高二上学期10月月考化学试题广西柳州铁一中学2023-2024学年高二上学期10月校际交流联考化学试卷广西桂林市第十一中学2023-2024学年高二上学期11月期中化学试题(已下线)提升练04 化学平衡图像分析-【查漏补缺】2024年高考化学复习冲刺过关(新高考专用)
名校
2 . 根据相应的图象(图象编号与选项一一对应),判断下列相关说法正确的是
 | 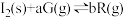 | 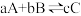 |  |
A.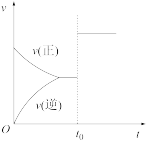 | B.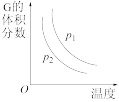 | C.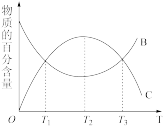 | D.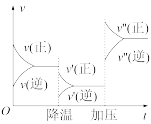 |
A. 时改变某一条件后如图所示,则改变的条件一定是加入催化剂 时改变某一条件后如图所示,则改变的条件一定是加入催化剂 |
| B.反应达到平衡时,外界条件对平衡的影响如图所示,则正反应为放热反应 |
| C.从加入反应物开始,物质的百分含量与温度的关系如图所示,则正反应为吸热反应 |
| D.该反应的正反应为放热反应,A、B、C一定均为气体,D为固体或液体 |
您最近一年使用:0次
名校
解题方法
3 . 在一密闭容器中进行以下可逆反应: 。在不同的条件下P的体积分数
。在不同的条件下P的体积分数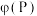 的变化情况如图,则该反应
的变化情况如图,则该反应
 。在不同的条件下P的体积分数
。在不同的条件下P的体积分数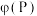 的变化情况如图,则该反应
的变化情况如图,则该反应
| A.正反应放热,L是固体 | B.正反应放热,L是气体 |
| C.正反应吸热,L是气体 | D.正反应吸热,L是固体或气体 |
您最近一年使用:0次
2021-10-22更新
|
241次组卷
|
2卷引用:甘肃省徽县第一中学2021-2022学年高二上学期11月月考化学试题
解题方法
4 . 已知反应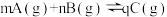 ,由图象得到的对应结论正确的是
,由图象得到的对应结论正确的是
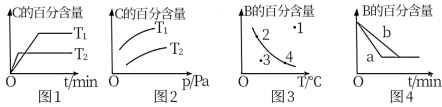
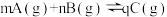 ,由图象得到的对应结论正确的是
,由图象得到的对应结论正确的是
| A.仅由图1判断,T1、T2对应平衡常数的大小关系为K1>K2 |
| B.仅由图2判断,m+n>q且T1<T2 |
| C.仅由图3判断,反应处于点1时,v正<v逆 |
| D.仅由图4判断,曲线a一定是使用了催化剂 |
您最近一年使用:0次
2021-01-10更新
|
117次组卷
|
4卷引用:甘肃省白银市靖远县2020-2021学年高二上学期期末考试化学试题
名校
解题方法
5 . 一定条件下,反应2NH3(g) N2(g) + 3H2(g) △H>0,达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是
N2(g) + 3H2(g) △H>0,达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是
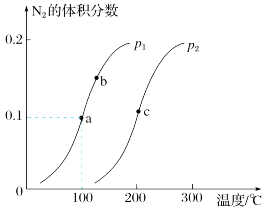
 N2(g) + 3H2(g) △H>0,达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是
N2(g) + 3H2(g) △H>0,达到平衡时N2的体积分数与温度、压强的关系如图所示。下列说法正确的是
| A.压强:p1>p2 | B.a点:2v正(NH3)= 3v逆(H2) |
C.a点:NH3的转化率为 | D.b、c两点对应的平衡常数:Kc>Kb |
您最近一年使用:0次
2020-12-29更新
|
727次组卷
|
14卷引用:甘肃省永昌县第一高级中学2021-2022学年高二上学期期中考试化学(理)试题
甘肃省永昌县第一高级中学2021-2022学年高二上学期期中考试化学(理)试题(已下线)天津市和平区2021届高三上学期期末考试化学试题(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点19 化学平衡常数 化学反应进行的方向-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时38 化学平衡常规图像-2022年高考化学一轮复习小题多维练(全国通用)2017届湖南长沙市长郡中学高三上第一次周测化学卷(已下线)2019年4月13日《每日一题》三轮复习—— 周末培优(已下线)2019年9月27日 《每日一题》2020年高考一轮复习-化学平衡常数和转化率河北省秦皇岛市第一中学2018-2019学年高二第一学期第一次月考化学试题辽宁师范大学附中2019-2020学年高二10月月考化学试题广东省广州市执信中学(广雅,执信,二中联考)2019-2020学年高二上学期期末考试化学试题(已下线)考点25 化学反应速率与平衡图象-备战2023年高考化学一轮复习考点帮(全国通用)广东省佛山市第一中学2022-2023学年高二上学期10月月考化学试题(已下线)考点25 化学反应速率与平衡图象(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)
名校
解题方法
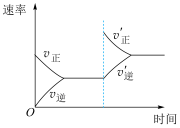
6 . T ℃ 时,A气体与B气体反应生成C气体。反应过程中A、B、C的浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
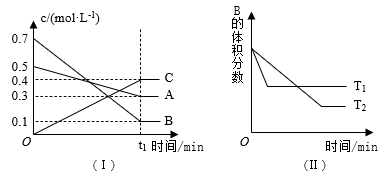

| A.t1 min后,其他条件不变,增大压强,平衡向逆反应方向移动 |
| B.t1 min后,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动 |
| C.T ℃ 时,在相同容器中,若通入0.3 mol·L-1 A、0.1 mol·L-1 B和0.4 mol·L-1 C进行反应,达到平衡后,C的浓度仍为0.4 mol·L-1 |
| D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
您最近一年使用:0次
2020-12-26更新
|
179次组卷
|
10卷引用:甘肃省民乐县第一中学2021--2022学年高二上学期期中考试化学试题
甘肃省民乐县第一中学2021--2022学年高二上学期期中考试化学试题甘肃省天水市第六中学2019-2020学年高二上学期期末考试化学试题(普通班)(已下线)2010年黑龙江省双鸭山一中高三上学期期中考试(化学)(已下线)2012-2013学年河北省沧县中学高二10月月考化学试卷2016-2017学年江西省宜春市奉新一中高二上月考一化学试卷夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 化学反应速率及影响图像分析山西省长治市第二中学校2020-2021学年高二上学期期中考试化学试题河北省沧州市黄骅中学2020-2021学年高二上学期第三次月考化学试题安徽省安庆市怀宁县第二中学2022-2023学年高二上学期期末考试化学试题吉林省BEST合作体八校2023-2024学年高二上学期1月期末化学试题
解题方法
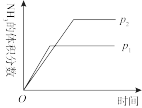
7 . 可逆反应 aA(s) + bB(g)⇌cC(g) + dD(g)进行过程中,当其他条件不变时,C 的体积分数 C%与温度(T)、压强(P)的关系如图所示。下列叙述正确的是( )


| A.化学方程式中,b > c + d |
| B.达到平衡后,加入催化剂,C 的体积分数增大 |
| C.达到平衡后,升高温度,平衡向左移动 |
| D.在P1时化学平衡常数大于P2时化学平衡常数 |
您最近一年使用:0次
2020-10-16更新
|
192次组卷
|
4卷引用:甘肃省镇原县第二中学2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
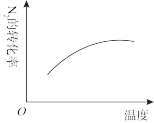
8 . 反应 mY(g)+nZ(g)⇌qX(g) ΔH,在不同温度下的平衡体系中,物质 Y 的体积分数随压强变化的曲线如图所示。下列说法正确的是
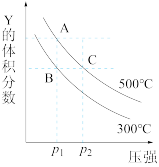

| A.m+n<q |
| B.该反应的ΔH>0 |
| C.A、C 两点化学平衡常数:KA>KC |
| D.B、C 两点的反应速率:v(B)<v(C) |
您最近一年使用:0次
2020-07-04更新
|
268次组卷
|
5卷引用:甘肃省甘南藏族自治州舟曲县第一中学2021-2022学年高二上学期期中考试化学试题
甘肃省甘南藏族自治州舟曲县第一中学2021-2022学年高二上学期期中考试化学试题北京101学校2019-2020学年高二下学期期末考试化学试题(已下线)第二章检测-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)广东省深圳市新安中学(集团)高中部2020-2021学年高二上学期期中考试化学试题辽宁省沈阳市第十五中学2023-2024学年高二上学期10月月考化学试题
名校
解题方法
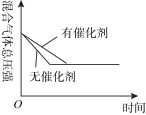
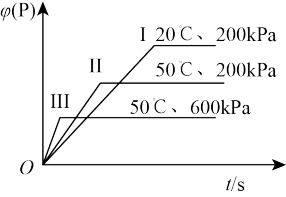
9 . 某化学科研小组研究在其他条件不变时,改变某一条件对化学平衡的影响,得到如下变化规律(图中p表示压强,T表示温度,n表示物质的量)。
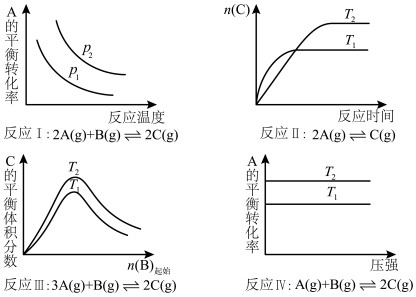
根据以上规律判断,下列结论正确的是( )

根据以上规律判断,下列结论正确的是( )
| A.反应Ⅰ:ΔH>0,p2>p1 | B.反应Ⅱ:ΔH<0,T1<T2 |
| C.反应Ⅲ:ΔH>0,T2>T1或ΔH<0,T2<T1 | D.反应Ⅳ:ΔH<0,T2>T1 |
您最近一年使用:0次
2020-05-09更新
|
177次组卷
|
9卷引用:甘肃省张掖市第二中学2021-2022学年高二上学期11月月考化学试题
甘肃省张掖市第二中学2021-2022学年高二上学期11月月考化学试题陕西省西安市第一中学2021-2022学年高二上学期期中考试化学试题广西南宁市第三中学2017-2018学年高二上学期期末考试化学试题【全国百强校】黑龙江省哈尔滨市第三中学校2018-2019学年高二上学期第一次阶段性测试化学试题【全国百强校】山东省师范大学附属中学2018-2019学年高二上学期第五次学分认定(期中)考试化学试题【全国百强校】山东省师范大学附属中学2018-2019学年高二上学期期中学分认定考试分化学试题安徽省合肥市2019-2020学年高二下学期开学考试化学试题河南省洛阳市2020-2021学年高二上学期期中考试化学试题内蒙古呼伦贝尔市阿荣旗第一中学2020-2021学年高二上学期月考化学试题
名校
10 . 密闭容器中进行的可逆反应aA(g)+bB(g)⇌cC(g)在不同温度(T1和T2)及压强(p1和p2)下,混合气体中B的质量分数w(B)与反应时间(t)的关系如图所示。下列判断正确的是( )
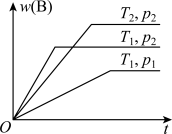

| A.T1<T2,p1<p2,a+b>c,正反应为吸热反应 |
| B.T1>T2,p1<p2,a+b<c,正反应为吸热反应 |
| C.T1<T2,p1>p2,a+b<c,正反应为吸热反应 |
| D.T1>T2,p1>p2,a+b>c,正反应为放热反应 |
您最近一年使用:0次
2020-05-08更新
|
393次组卷
|
25卷引用:甘肃省永昌县第一高级中学2020-2021学年高二上学期期末考试化学试题
甘肃省永昌县第一高级中学2020-2021学年高二上学期期末考试化学试题甘肃省天水市甘谷第一中学2019-2020学年高二下学期开学考试化学试题江苏省南京市雨花台中学2020-2021学年高二年级上学期期末调研测试化学试题2016-2017学年新疆生产建设兵团二中高二上期中化学卷新疆呼图壁县第一中学2017-2018学年高二上学期期中考试化学试题新疆维吾尔自治区昌吉市第四中学2018-2019学年第一学期高二第一次月考化学试题内蒙古自治区翁牛特旗乌丹第一中学2018-2019学年高二上学期期中考试化学试题新疆自治区昌吉市第九中学2018-2019学年高二上学期第二次月考化学试题四川省宁南中学2018-2019学年高二下学期第一次月考化学试题山东省实验中学2020届高三第一次诊断性考试化学试题云南省玉溪市玉溪一中2019-2020学年高二上学期第一次月考化学试题(已下线)专题7.2 化学平衡状态 化学平衡移动(讲)-《2020年高考一轮复习讲练测》步步为赢 高二化学寒假作业:作业五 化学平衡的图像分析黑龙江省哈尔滨市第六中学2019-2020学年高二上学期期末考试化学试题湖北省新高考联考协作体2020-2021学年高二上学期期中考试化学试题贵州省毕节市七星关区毕节市实验高级中学2020-2021学年高二上学期期中考试化学试题重庆市朝阳中学高2020-2021学年高二上学期期中考试化学试题广东省大埔县虎山中学2022-2023学年高三上学期1月期末考试化学试题河北省承德县第一中学2022-2023学年高一下学期期末考试化学试题北京市东直门中学2022-2023学年高二上学期期中考试化学试题北京工业大学附属中学2023-2024学年高二上学期期中考试化学试题四川省达州市宣汉县第二中学2023-2024学年高二上学期中期考试化学试题四川省内江市2025届第三中学高二上学期化学试卷四川省自贡市第二十二中学校2023-2024学年高二上学期期中考试化学试题上海市建平世纪中学2023-2024学年高二上学期阶段练习二 化学(等级)试题