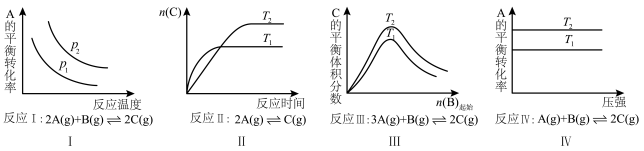
T ℃ 时,A气体与B气体反应生成C气体。反应过程中A、B、C的浓度变化如图(Ⅰ)所示,若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如图(Ⅱ)所示,则下列结论正确的是
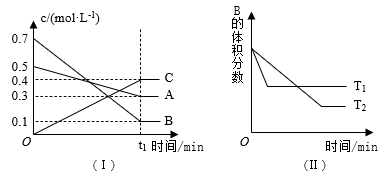

| A.t1 min后,其他条件不变,增大压强,平衡向逆反应方向移动 |
| B.t1 min后,保持容器总压强不变,通入稀有气体,平衡向正反应方向移动 |
| C.T ℃ 时,在相同容器中,若通入0.3 mol·L-1 A、0.1 mol·L-1 B和0.4 mol·L-1 C进行反应,达到平衡后,C的浓度仍为0.4 mol·L-1 |
| D.其他条件不变,升高温度,正、逆反应速率均增大,且A的转化率增大 |
10-11高三上·黑龙江双鸭山·阶段练习 查看更多[10]
吉林省BEST合作体八校2023-2024学年高二上学期1月期末化学试题安徽省安庆市怀宁县第二中学2022-2023学年高二上学期期末考试化学试题甘肃省民乐县第一中学2021--2022学年高二上学期期中考试化学试题河北省沧州市黄骅中学2020-2021学年高二上学期第三次月考化学试题甘肃省天水市第六中学2019-2020学年高二上学期期末考试化学试题(普通班)山西省长治市第二中学校2020-2021学年高二上学期期中考试化学试题夯基提能2020届高三化学选择题对题专练——选修4化学反应原理—— 化学反应速率及影响图像分析2016-2017学年江西省宜春市奉新一中高二上月考一化学试卷(已下线)2010年黑龙江省双鸭山一中高三上学期期中考试(化学)(已下线)2012-2013学年河北省沧县中学高二10月月考化学试卷
更新时间:2020-12-26 22:49:54
|
相似题推荐
单选题
|
适中
(0.65)
解题方法
【推荐1】新制氯水显淡黄绿色,可使蓝色石蕊试纸先变红后褪色,久置氯水不能实现该变化。为探究氯水失效的原因,某同学用强光照射盛有新制氯水的密闭广口瓶,并用传感器测定广口瓶中数据,得到氯离子浓度曲线(图1)、氧气体积分数曲线(图2)。

下列有关实验表述不正确 的是

下列有关实验表述
A.新制氯水存在:Cl2+H2O HCl+HClO HCl+HClO |
B.新制氯水存在: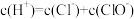 |
| C.光照实验过程中新制氯水颜色逐渐变浅 |
| D.若实验过程测定溶液的pH值,pH值减小 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.ΔH<0、ΔS>0的反应在温度低时不能自发进行 |
| B.因为焓变和熵变都与反应自发性有关,因此焓变或熵变均可单独作为反应自发性的判据 |
| C.NH4HCO3(s)═NH3(g)+H2O(g)+CO2(g) △H=+185.57kJ/mol能自发进行,原因是体系有自发地向混乱度增大的方向转变的倾向 |
| D.化学反应的限度不可以通过改变条件而改变 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】对于可逆反应:A(g)+2B(g) 2C(g)△H>0,下列图像中正确的是()
2C(g)△H>0,下列图像中正确的是()
 2C(g)△H>0,下列图像中正确的是()
2C(g)△H>0,下列图像中正确的是()A.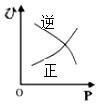 | B. |
C.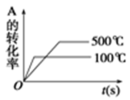 | D. |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
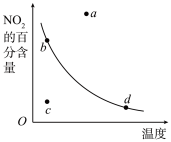
【推荐2】如图曲线表示其他条件一定时,2NO(g)+O2(g) 2NO2(g) △H<0反应中NO2的百分含量与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且
2NO2(g) △H<0反应中NO2的百分含量与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且 (正)>
(正)> (逆)的点是
(逆)的点是
 2NO2(g) △H<0反应中NO2的百分含量与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且
2NO2(g) △H<0反应中NO2的百分含量与温度的关系曲线,图中标有a、b、c、d四点,其中表示未达到平衡状态,且 (正)>
(正)> (逆)的点是
(逆)的点是
| A.a点 | B.b点 | C.c点 | D.d点 |
您最近半年使用:0次

 pC,化学平衡常数为K,若升高温度,K值增大。下列说法正确的是
pC,化学平衡常数为K,若升高温度,K值增大。下列说法正确的是