20. CO可用于合成甲醇,化学方程式为:CO(g)+2H
2(g)

CH
3OH(g)。
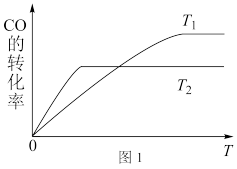
(1)图1是反应CO(g)+2H
2(g)

CH
3OH(g)在不同温度下CO的转化率随时间变化的曲线。
①该反应的焓变Δ
H___(填“>”“<”或“=”)0。
②T
1和T
2温度下的平衡常数大小关系是
K1__(填“>”“<”或“=”)
K2。在T
1温度下,往体积为1L的密闭容器中,充入1molCO和2molH
2,经测得CO和CH
3OH(g)的浓度随时间变化如图2所示。则该反应的平衡常数为
___。
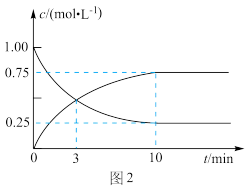
③若容器容积不变,下列措施可增加CO转化率的是
___(填字母)。
a.升高温度
b.将CH
3OH(g)从体系中分离
c.使用合适的催化剂
d.充入He,使体系总压强增大
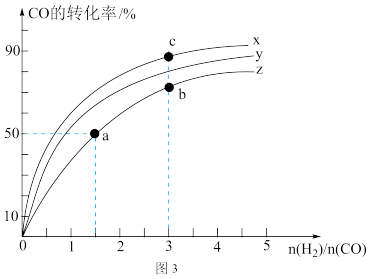
(2)在容积为1L的恒容容器中,分别研究在230℃、250℃和270℃三种温度下合成甲醇的规律。如图3是上述三种温度下H
2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系,则曲线z对应的温度是
___℃;该温度下上述反应的化学平衡常数为
___。曲线上a、b、c点对应的化学平衡常数分别为
K1、
K2、
K3,则
K1、
K2、
K3的大小关系为
___。