名校
解题方法
1 . Ⅰ.从氯二氟甲烷(CHClF2)中获得四氟乙烯(C2F4):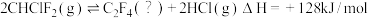 。
。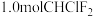 样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有
样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有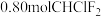 。
。
(1)写出四氟乙烯形成的高分子化合物聚四氟乙烯的结构简式_______ 。
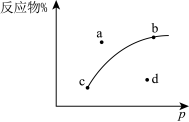
(2)如图是一定条件下,反应物平衡时物质的量分数与压强的关系曲线。据此判断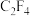 的状态是
的状态是 _______ (填“气体”、“液体”或“固体”)。
(3)该反应在_______ (填“高温”、“低温”或“任意温度”)的自发性更大;
(4)如图的a~d四点中,表示Q>K的点有_______ ;
(5)以平衡时气态物质的量分数表示平衡常数 ,其计算表达式为
,其计算表达式为 _______ 。
Ⅱ. 研究 氧化
氧化 制
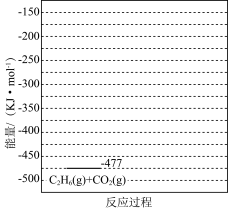
制 对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):
对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):
Ⅰ.C2H6(g) C2H4(g)+H2(g) △H1=136kJ·mol-1
C2H4(g)+H2(g) △H1=136kJ·mol-1
Ⅱ.C2H6(g)+CO2(g) C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1
C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1
Ⅲ.C2H6(g)+2CO2(g) 4CO(g)+3H2(g) △H3
4CO(g)+3H2(g) △H3
Ⅳ.CO2(g)+H2(g) CO(g)+H2O(g) △H4=41kJ·mol-1
CO(g)+H2O(g) △H4=41kJ·mol-1

(6)有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:[C2H6(g)+CO2(g)]→[C2H4(g)+H2(g)+CO2(g)]→[C2H4(g)+CO(g)+H2O(g)],且第二步速率较慢(反应活化能为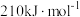 )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量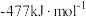 开始(如图)。
开始(如图)。_______
(7)① 和
和 按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“
按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“ 氧化
氧化 制
制 ”的影响,所得实验数据如下表:
”的影响,所得实验数据如下表:
结合具体反应分析,在催化剂X作用下, 氧化
氧化 的主要产物是
的主要产物是_______ ,判断依据是_______ 。
②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高 的选择性(生成
的选择性(生成 的物质的量与消耗
的物质的量与消耗 的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是
的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是_______ 。
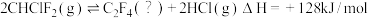 。
。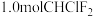 样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有
样品在18.5L容器内加热。反应达到平衡后,平衡混合物中含有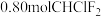 。
。(1)写出四氟乙烯形成的高分子化合物聚四氟乙烯的结构简式
(2)如图是一定条件下,反应物平衡时物质的量分数与压强的关系曲线。据此判断
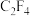 的状态是
的状态是 
(3)该反应在
(4)如图的a~d四点中,表示Q>K的点有
(5)以平衡时气态物质的量分数表示平衡常数
 ,其计算表达式为
,其计算表达式为 Ⅱ. 研究
 氧化
氧化 制
制 对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):
对资源综合利用有重要意义。相关的主要化学反应有(298K时,相关物质的相对能量如图):Ⅰ.C2H6(g)
 C2H4(g)+H2(g) △H1=136kJ·mol-1
C2H4(g)+H2(g) △H1=136kJ·mol-1Ⅱ.C2H6(g)+CO2(g)
 C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1
C2H4(g)+H2O(g)+CO(g) △H2=177kJ·mol-1Ⅲ.C2H6(g)+2CO2(g)
 4CO(g)+3H2(g) △H3
4CO(g)+3H2(g) △H3Ⅳ.CO2(g)+H2(g)
 CO(g)+H2O(g) △H4=41kJ·mol-1
CO(g)+H2O(g) △H4=41kJ·mol-1
(6)有研究表明,在催化剂存在下,反应Ⅱ分两步进行,过程如下:[C2H6(g)+CO2(g)]→[C2H4(g)+H2(g)+CO2(g)]→[C2H4(g)+CO(g)+H2O(g)],且第二步速率较慢(反应活化能为
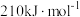 )。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量
)。根据相关物质的相对能量,画出反应Ⅱ分两步进行的“能量−反应过程图”,起点从[C2H6(g)+CO2(g)]的能量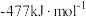 开始(如图)。
开始(如图)。
(7)①
 和
和 按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“
按物质的量1:1投料,在923K和保持总压恒定的条件下,研究催化剂X对“ 氧化
氧化 制
制 ”的影响,所得实验数据如下表:
”的影响,所得实验数据如下表:| 催化剂 | 转化率C2H6/% | 转化率CO2/% | 产率C2H4/% |
| 催化剂X | 19.0 | 37.6 | 3.3 |
 氧化
氧化 的主要产物是
的主要产物是②采用选择性膜技术(可选择性地让某气体通过而离开体系)可提高
 的选择性(生成
的选择性(生成 的物质的量与消耗
的物质的量与消耗 的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是
的物质的量之比)。在773K,乙烷平衡转化率为9.1%,保持温度和其他实验条件不变,采用选择性膜技术,乙烷转化率可提高到11.0%。结合具体反应说明乙烷转化率增大的原因是
您最近一年使用:0次



