名校
解题方法
1 . 回答下列问题。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是___________ ,用平衡原理解释原因___________ 。
(2)常温下,0.1 mol/L 的NaOH溶液的pH=___________ ,0.05mol/L的硫酸的pH=___________ ,取一定体积的两溶液混合,所得混合液的pH=2,则所取硫酸溶液的体积与NaOH溶液的体积比为___________ 。
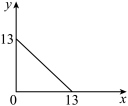
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为___________ ,则该温度t___________ 25℃(填“>”“<”或“=”)。
(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为___________ 。
(1)向滴有酚酞的氨水中加入少量的氯化铵固体,观察到的现象是
(2)常温下,0.1 mol/L 的NaOH溶液的pH=
(3)某温度(t℃)下的溶液中,c(H+)=10-xmol/L,c(OH-)=10-ymol/L,x与y的关系如图所示,此温度时,水的离子积常数Kw为

(4)25℃时,pH=3的酸酸溶液和pH=11的NaOH溶液中由水电离出的c(H+)之比为
您最近一年使用:0次
解题方法
2 . 研究电解质在水溶液中的离子反应与平衡有重要的意义。常温下,用0.1 mol/L NaOH溶液滴定10 mL 0.1 mol/L CH3COOH溶液的滴定曲线如图所示。
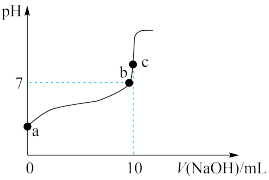
(1)a点溶液的pH________ 1(填“>”、“<”或“=”)。醋酸的电离平衡常数 表达式为___________________________ 。
(2)现有0.1 mol/L NaOH溶液,该溶液中c(OH-)≈_______________ ,其中水电离产生的c(H+)=_______________ ,水电离产生的c(OH-)=____________ ,该溶液的pH为__________ 。
(3)b点溶液中,存在的电荷守恒关系式为______________ ,因此时混合液pH=7,则溶液中c(H+)为______________ ,其中c(Na+) ________ c(CH3COO−)(填“>”、“<”或“=”)。
(4)c点溶液中,c(Na+)________ [c(CH3COO−) + c(CH3COOH)](填“>”、“<”或“=”,下同),此时溶液中c(H+)_____________ c(OH-)。
(5)比较a、c两点水的电离程度:a___ c,并分别解释原因 a:__________ ,c__________ 。

(1)a点溶液的pH
(2)现有0.1 mol/L NaOH溶液,该溶液中c(OH-)≈
(3)b点溶液中,存在的电荷守恒关系式为
(4)c点溶液中,c(Na+)
(5)比较a、c两点水的电离程度:a
您最近一年使用:0次



