解题方法
1 . 请回答下列问题:
(1)已知常温下H2A的Ka1 = 1×10-8,Ka2 = 1×10-11,则NaHA溶液中呈_______ 性,计算说明理由_______ ,溶液中离子浓度排序_______ 。
(2)常温时,pH=3的盐酸中由水电离出的c(H+)为_______ mol·L-1。
(3)100℃时,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。此时水的离子积
_______ ,溶液中 为
为_______ mol·L-1。
(1)已知常温下H2A的Ka1 = 1×10-8,Ka2 = 1×10-11,则NaHA溶液中呈
(2)常温时,pH=3的盐酸中由水电离出的c(H+)为
(3)100℃时,向pH=6的蒸馏水中加入NaHSO4晶体,保持温度不变,测得溶液的pH=2。此时水的离子积

 为
为
您最近半年使用:0次
名校
解题方法
2 . 请根据要求回答下列问题。
(1)1 mol·L-1 Na2CO3溶液的pH_______ (填“>”“<”或“=”, 下同)0.1 mol·L-1Na2CO3溶液的pH;1 mol·L-1 Na2CO3溶液的水解程度_______ 0. 1 mol·L-1Na2CO3溶液的水解程度。
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则pH=9的NaOH溶液与pH=4的H2SO4溶液的体积之比为_______ 。
(3)X、Y、Z、 W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种。下表是常温下浓度均为0.01mol/L的X、Y、Z、W溶液的pH。将X、Y、Z各1 mol同时溶于水中得到混合溶液,则混合溶液中各离子的浓度由大到小的顺序为_______ 。
(1)1 mol·L-1 Na2CO3溶液的pH
(2)25℃时,将pH=9的NaOH溶液与pH=4的H2SO4溶液混合,若所得混合溶液的pH=7,则pH=9的NaOH溶液与pH=4的H2SO4溶液的体积之比为
(3)X、Y、Z、 W分别是HNO3、NH4NO3、NaOH、NaNO2四种强电解质中的一种。下表是常温下浓度均为0.01mol/L的X、Y、Z、W溶液的pH。将X、Y、Z各1 mol同时溶于水中得到混合溶液,则混合溶液中各离子的浓度由大到小的顺序为
| 0.01mol/L的溶液 | X | Y | Z | W |
| pH | 12 | 2 | 8.5 | 4.5 |
您最近半年使用:0次
解题方法
3 . 碳和硅是带来人类文明的重要元素。
(1)工业上用焦炭在高温下还原二氧化硅可制得含有少量杂质的粗硅。写出该反应的化学反应方程式_______ 。
(2)100℃时,将足量的碳酸氢钠固体置于V L真空恒容容器中,已知: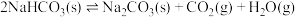 ,上述反应达平衡时体系的总压为100kpa。(分压=总压×物质的量分数)
,上述反应达平衡时体系的总压为100kpa。(分压=总压×物质的量分数)
①下列说法不正确的是_______ 。
A.可通过CO2(g)和H2O(g)的物质的量比值不变来判断该反应达到平衡
B.保持温度、体积不变,平衡体系中不断移走H2O(g),正反应速率增大,逆反应速率减小,平衡向右移动
C.保持体积不变,升高温度,反应速率加快
D.保持温度、体积不变,平衡体系中不断通入等物质的量的CO2(g)和H2O(g), 最终将完全转变为
最终将完全转变为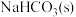
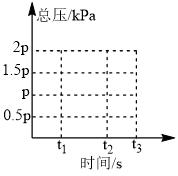
②上述平衡体系t1时刻总压为p(如图),保持温度不变,t1时刻突然将容器的体积变为原来一半且保持不变,到t2时刻达到平衡,在图中画出 时体系的总压
时体系的总压______ 。
(3)大气中部分CO2溶于水并与水进一步发生反应。常温下,反应方程式如下:
①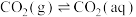
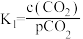
②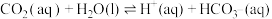 K2
K2
其中pCO2为CO2(g)在空气中的分压,c(CO2)为CO2在水溶液中的平衡浓度。当大气压强为p kPa,大气中CO2(g)的物质的量分数为x时,溶液中H+浓度为_______ mol/L(用K1、K2、p、x、Kw表示,考虑水的电离,忽略 的电离)
的电离)
(4)甲烷气相热分解反应方程式为: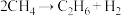 ,该反应的机理如下:
,该反应的机理如下:
① ,②_______,③
,②_______,③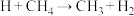 ④
④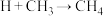 ,补充反应②反应方程式:
,补充反应②反应方程式:_______ 。
(5)在地壳内,深度每增加1km,压强约增加25250~30300kPa,这对固体物质的平衡会发生较大的影响。如:
地壳中存在CaAl2Si2O8、Mg2SiO4和CaMg2Al2Si3O12,在地壳区域高压条件下,有利于_______ (写化学式)生成,试结合上述数据解释原因_______ 。
(1)工业上用焦炭在高温下还原二氧化硅可制得含有少量杂质的粗硅。写出该反应的化学反应方程式
(2)100℃时,将足量的碳酸氢钠固体置于V L真空恒容容器中,已知:
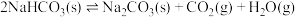 ,上述反应达平衡时体系的总压为100kpa。(分压=总压×物质的量分数)
,上述反应达平衡时体系的总压为100kpa。(分压=总压×物质的量分数)①下列说法不正确的是
A.可通过CO2(g)和H2O(g)的物质的量比值不变来判断该反应达到平衡
B.保持温度、体积不变,平衡体系中不断移走H2O(g),正反应速率增大,逆反应速率减小,平衡向右移动
C.保持体积不变,升高温度,反应速率加快
D.保持温度、体积不变,平衡体系中不断通入等物质的量的CO2(g)和H2O(g),
 最终将完全转变为
最终将完全转变为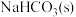
②上述平衡体系t1时刻总压为p(如图),保持温度不变,t1时刻突然将容器的体积变为原来一半且保持不变,到t2时刻达到平衡,在图中画出
 时体系的总压
时体系的总压
(3)大气中部分CO2溶于水并与水进一步发生反应。常温下,反应方程式如下:
①
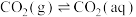
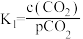
②
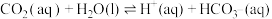 K2
K2其中pCO2为CO2(g)在空气中的分压,c(CO2)为CO2在水溶液中的平衡浓度。当大气压强为p kPa,大气中CO2(g)的物质的量分数为x时,溶液中H+浓度为
 的电离)
的电离)(4)甲烷气相热分解反应方程式为:
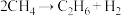 ,该反应的机理如下:
,该反应的机理如下:①
 ,②_______,③
,②_______,③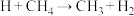 ④
④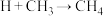 ,补充反应②反应方程式:
,补充反应②反应方程式:(5)在地壳内,深度每增加1km,压强约增加25250~30300kPa,这对固体物质的平衡会发生较大的影响。如:

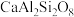 (钙长石) (钙长石) |  (镁橄榄石) (镁橄榄石) | 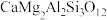 (钙镁石榴子石) | |
| 摩尔质量(g/mol) | 278 | 140 | 418 |
| 密度(g/cm) | 2.70 | 3.22 | 3.50 |
地壳中存在CaAl2Si2O8、Mg2SiO4和CaMg2Al2Si3O12,在地壳区域高压条件下,有利于
您最近半年使用:0次
解题方法
4 . 请回答下列问题:
(1)某温度下,水的离子积常数Kw=2×10-13,0.02mol·L-1的NaOH溶液的pH=___________ 。
(2)25℃时,0.10 mol·L-1的HA溶液中 =1010,该HA溶液的pH=
=1010,该HA溶液的pH=___________ 。
(3)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后,CH3COONa溶液的pH___________ NaOH溶液的pH(填“>”“<””或“=”)。
(4)将物质的量浓度相同的盐酸与氨水混合后,溶液中的c( )=c(Cl-),则盐酸的体积
)=c(Cl-),则盐酸的体积___________ 氨水的体积(填“>”“<””或“=”)。
(5)某学生用0.1 mol·L-1盐酸标准溶液滴定未知浓度的NaOH溶液,其操作步骤如下:
A.移取20.00 mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3 cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序___________ (填序号)。
(1)某温度下,水的离子积常数Kw=2×10-13,0.02mol·L-1的NaOH溶液的pH=
(2)25℃时,0.10 mol·L-1的HA溶液中
 =1010,该HA溶液的pH=
=1010,该HA溶液的pH=(3)pH相等的NaOH溶液与CH3COONa溶液,分别加热到相同的温度后,CH3COONa溶液的pH
(4)将物质的量浓度相同的盐酸与氨水混合后,溶液中的c(
 )=c(Cl-),则盐酸的体积
)=c(Cl-),则盐酸的体积(5)某学生用0.1 mol·L-1盐酸标准溶液滴定未知浓度的NaOH溶液,其操作步骤如下:
A.移取20.00 mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3 cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序
您最近半年使用:0次
解题方法
5 . Ⅰ.现有下列4种重要的有机物:
① ②
② ③
③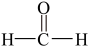 ④
④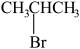
请回答:
(1)能与苯酚缩合成高分子化合物的是__________ 。(填序号)。
(2)能使酸性高锰酸钾溶液褪色的是__________ 。(填序号)。
(3)写出④在一定条件下发生消去反应的化学方程式__________ 。
Ⅱ.2020年3月22日为第28届世界水日,化学中有很多与水相关的化学知识。
(1)海水会腐蚀铁质海轮外壳,制造海轮时会在船底四周镶嵌_____ 。(填“锌块”或“铜块”)
(2)自来水厂常用含有Fe3+的净水剂净水,其原理是______ 。(用离子方程式表示)
(3)自来水常用氯气杀菌消毒,Cl2+H2O⇌HCl+HClO,要增大HClO的浓度,可以加入下列物质中的__________ 。
A.NaOH B.浓HCl C.CaCO3固体 D.H2O E.SO2
(4)常温下,0.01mol·L-1NaOH溶液,由水电离出的c(OH−)=______ mol·L-1。
①
 ②
② ③
③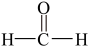 ④
④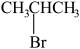
请回答:
(1)能与苯酚缩合成高分子化合物的是
(2)能使酸性高锰酸钾溶液褪色的是
(3)写出④在一定条件下发生消去反应的化学方程式
Ⅱ.2020年3月22日为第28届世界水日,化学中有很多与水相关的化学知识。
(1)海水会腐蚀铁质海轮外壳,制造海轮时会在船底四周镶嵌
(2)自来水厂常用含有Fe3+的净水剂净水,其原理是
(3)自来水常用氯气杀菌消毒,Cl2+H2O⇌HCl+HClO,要增大HClO的浓度,可以加入下列物质中的
A.NaOH B.浓HCl C.CaCO3固体 D.H2O E.SO2
(4)常温下,0.01mol·L-1NaOH溶液,由水电离出的c(OH−)=
您最近半年使用:0次
解题方法
6 . 请回答以下问题
(1)某温度时,测得pH=11的Ba(OH)2溶液浓度是0.005mol·L-1。
①该温度下水的离子积常数Kw=________ 。
②在此温度下,将pH=12的Ba(OH)2溶液Va L与pH=2的硫酸Vb L混合。若所得混合液为中性,则Va∶Vb=________ 。
(2)25 ℃时,部分物质的电离平衡常数如下表所示。请回答下列问题:
①下列说法正确的是__________
A.25 ℃时,向CH3COOH溶液中加入适量的NaOH溶液,CH3COOH的电离程度增大,电离平衡常数不变
B.0.1mol•L-1 CH3COOH溶液加水稀释,稀释后的溶液中水的电离程度减小
C.0.1mol•L-1 HClO溶液和0.1mol•L-1 NaClO溶液等体积混合呈溶液碱性
D.碳酸氢钠溶液中阴阳离子数目相等
② 同浓度的CH3COO-、HCO 、CO32-、ClO-结合H+的能力由强到弱的顺序为
、CO32-、ClO-结合H+的能力由强到弱的顺序为___
③ 25 ℃时,某CH3COOH和CH3COOK混合溶液呈中性,则该混合溶液中: =
=________
(3)煤燃烧排放的烟气含有SO2和NO,采用碱性的NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10−3mol·L−1。反应10min后溶液中离子浓度的分析结果如下表。
①写出NaClO2溶液脱硝过程中主要反应 的离子方程式______ 。
②如果采用Ca(ClO)2替代NaClO2,其脱硫效果会更好。试从化学平衡原理分析,Ca(ClO)2相比NaClO2具有的优点是________ 。
(1)某温度时,测得pH=11的Ba(OH)2溶液浓度是0.005mol·L-1。
①该温度下水的离子积常数Kw=
②在此温度下,将pH=12的Ba(OH)2溶液Va L与pH=2的硫酸Vb L混合。若所得混合液为中性,则Va∶Vb=
(2)25 ℃时,部分物质的电离平衡常数如下表所示。请回答下列问题:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.8×10—5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
①下列说法正确的是
A.25 ℃时,向CH3COOH溶液中加入适量的NaOH溶液,CH3COOH的电离程度增大,电离平衡常数不变
B.0.1mol•L-1 CH3COOH溶液加水稀释,稀释后的溶液中水的电离程度减小
C.0.1mol•L-1 HClO溶液和0.1mol•L-1 NaClO溶液等体积混合呈溶液碱性
D.碳酸氢钠溶液中阴阳离子数目相等
② 同浓度的CH3COO-、HCO
 、CO32-、ClO-结合H+的能力由强到弱的顺序为
、CO32-、ClO-结合H+的能力由强到弱的顺序为③ 25 ℃时,某CH3COOH和CH3COOK混合溶液呈中性,则该混合溶液中:
 =
=(3)煤燃烧排放的烟气含有SO2和NO,采用碱性的NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝。在鼓泡反应器中通入含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×10−3mol·L−1。反应10min后溶液中离子浓度的分析结果如下表。
| 离子 | SO42− | SO32− | NO3− | NO2− | Cl− |
| c/(mol·L−1) | 8.35×10−4 | 6.87×10−6 | 1.5×10−4 | 1.2×10−5 | 3.4×10−3 |
①写出NaClO2溶液脱硝过程中
②如果采用Ca(ClO)2替代NaClO2,其脱硫效果会更好。试从化学平衡原理分析,Ca(ClO)2相比NaClO2具有的优点是
您最近半年使用:0次
解题方法
7 . 苯乙腈主要用于有机合成及生产医药,农药的中间体,对环境有危害。常温常压下,苯乙腈水解一般需加入酸碱催化剂。但研究人员发现,在近临界水(指温度在523~623K之间的压缩液态水)中,不加任何催化剂的情况下,苯乙腈就能发生水解反应生成苯乙酞胺:
C6H5CH2CN(l)+H2O(l) C6H5CH2CONH2(l) △H
C6H5CH2CONH2(l) △H
(苯乙腈) (苯乙酰胺)
请回答下列问题:
(1)已知近临界水中,水的离子积常数为10-10,则此条件下,pH=7的NaAc溶液中由水电离的c(H+)=________ mol·L-1。该反应不加任何催化剂就能发生的主要原因是___________ 。
(2)研究反应的平衡常数(记作lgK)与温度(T)的关系,得到如图1所示的关系,判断该反应的△H__________ 0(填“>”“<”或“=”)。
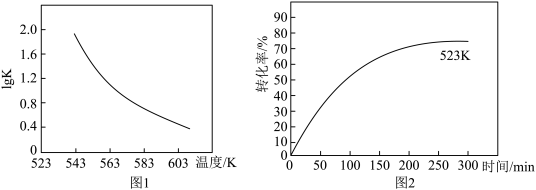
(3)图2表示其他条件不变时,温度和时间对苯乙腈转化率的影响曲线图(不完整)。若图中曲线对应的温度为523K,请你在原图中作出温度为583K的影响曲线。___________ 。
(4)下列哪种仪器可用于分析水解反应过程中苯乙腈浓度的变化_________ (填编号)。
A.元素分析仪B.核磁共振仪C.原子吸收光谱仪D.分光光度计
(5)科学家还在近临界水中分别添加CO2、NH3,研究后得到了如下的图示:
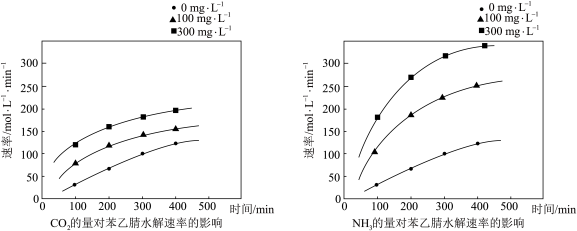
从中你可以得出什么结论(至少写出2点___________ 。
(6)水的用途很广,可利用太阳能光伏电池电解水制高纯氢,工作示意图如图。通过控制开关连接K1或K2,可交替得到H2和O2。
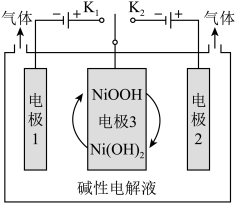
①制H2时,连接______________ ,可得H2。
②改变开关连接方式,产生O2的电极反应式__________________________ 。
③选用NiOOH、Ni(OH)2作为电极3材料的优点(请结合电极反应式进行阐述)___________ 。
C6H5CH2CN(l)+H2O(l)
 C6H5CH2CONH2(l) △H
C6H5CH2CONH2(l) △H(苯乙腈) (苯乙酰胺)
请回答下列问题:
(1)已知近临界水中,水的离子积常数为10-10,则此条件下,pH=7的NaAc溶液中由水电离的c(H+)=
(2)研究反应的平衡常数(记作lgK)与温度(T)的关系,得到如图1所示的关系,判断该反应的△H

(3)图2表示其他条件不变时,温度和时间对苯乙腈转化率的影响曲线图(不完整)。若图中曲线对应的温度为523K,请你在原图中作出温度为583K的影响曲线。
(4)下列哪种仪器可用于分析水解反应过程中苯乙腈浓度的变化
A.元素分析仪B.核磁共振仪C.原子吸收光谱仪D.分光光度计
(5)科学家还在近临界水中分别添加CO2、NH3,研究后得到了如下的图示:

从中你可以得出什么结论(至少写出2点
(6)水的用途很广,可利用太阳能光伏电池电解水制高纯氢,工作示意图如图。通过控制开关连接K1或K2,可交替得到H2和O2。

①制H2时,连接
②改变开关连接方式,产生O2的电极反应式
③选用NiOOH、Ni(OH)2作为电极3材料的优点(请结合电极反应式进行阐述)
您最近半年使用:0次
真题
解题方法
8 . 【加试题】水是“生命之基质”,是“永远值得探究的物质”。
(1) 关于反应H2(g)+1/2O2(g) H2O(l),下列说法
H2O(l),下列说法不正确 的是________ 。
A.焓变ΔH<0,熵变ΔS<0
B.可以把反应设计成原电池,实现能量的转化
C.一定条件下,若观察不到水的生成,说明该条件下反应不能自发进行
D.选用合适的催化剂,有可能使反应在常温常压下以较快的速率进行
(2) ①根据H2O的成键特点,画出与图中H2O分子直接相连的所有氢键(O-H…O)________ 。
②将一定量水放入抽空的恒容密闭容器中,测定不同温度(T)下气态、液态水平衡共存[H2O(l)H2O(g)]时的压强(p)。在图中画出从20℃开始经过100℃的p随T变化关系示意图(20℃时的平衡压强用p1表示)________ 。

(3) 水在高温高压状态下呈现许多特殊的性质。当温度、压强分别超过临界温度(374.2℃)、临界压强(22.1 MPa)时的水称为超临界水。
①与常温常压的水相比,高温高压液态水的离子积会显著增大。解释其原因________ 。
②如果水的离子积Kw从1.0×10−14增大到1.0×10−10,则相应的电离度是原来的________ 倍。
③超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定实验条件下,测得乙醇的超临界水氧化结果如图所示,其中x为以碳元素计的物质的量分数,t为反应时间。
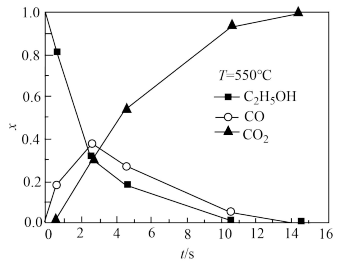
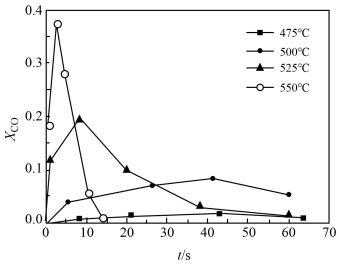
下列说法合理的是________ 。
A.乙醇的超临界水氧化过程中,一氧化碳是中间产物,二氧化碳是最终产物
B.在550℃条件下,反应时间大于15 s时,乙醇氧化为二氧化碳已趋于完全
C.乙醇的超临界水氧化过程中,乙醇的消耗速率或二氧化碳的生成速率都可以用来表示反应的速率,而且两者数值相等
D.随温度升高,xCO峰值出现的时间提前,且峰值更高,说明乙醇的氧化速率比一氧化碳氧化速率的增长幅度更大
(4) 以铂阳极和石墨阴极设计电解池,通过电解NH4HSO4溶液产生(NH4)2S2O8,再与水反应得到H2O2,其中生成的NH4HSO4可以循环使用。
①阳极的电极反应式是________ 。
②制备H2O2的总反应方程式是________ 。
(1) 关于反应H2(g)+1/2O2(g)
 H2O(l),下列说法
H2O(l),下列说法A.焓变ΔH<0,熵变ΔS<0
B.可以把反应设计成原电池,实现能量的转化
C.一定条件下,若观察不到水的生成,说明该条件下反应不能自发进行
D.选用合适的催化剂,有可能使反应在常温常压下以较快的速率进行
(2) ①根据H2O的成键特点,画出与图中H2O分子直接相连的所有氢键(O-H…O)
②将一定量水放入抽空的恒容密闭容器中,测定不同温度(T)下气态、液态水平衡共存[H2O(l)H2O(g)]时的压强(p)。在图中画出从20℃开始经过100℃的p随T变化关系示意图(20℃时的平衡压强用p1表示)


(3) 水在高温高压状态下呈现许多特殊的性质。当温度、压强分别超过临界温度(374.2℃)、临界压强(22.1 MPa)时的水称为超临界水。
①与常温常压的水相比,高温高压液态水的离子积会显著增大。解释其原因
②如果水的离子积Kw从1.0×10−14增大到1.0×10−10,则相应的电离度是原来的
③超临界水能够与氧气等氧化剂以任意比例互溶,由此发展了超临界水氧化技术。一定实验条件下,测得乙醇的超临界水氧化结果如图所示,其中x为以碳元素计的物质的量分数,t为反应时间。


下列说法合理的是
A.乙醇的超临界水氧化过程中,一氧化碳是中间产物,二氧化碳是最终产物
B.在550℃条件下,反应时间大于15 s时,乙醇氧化为二氧化碳已趋于完全
C.乙醇的超临界水氧化过程中,乙醇的消耗速率或二氧化碳的生成速率都可以用来表示反应的速率,而且两者数值相等
D.随温度升高,xCO峰值出现的时间提前,且峰值更高,说明乙醇的氧化速率比一氧化碳氧化速率的增长幅度更大
(4) 以铂阳极和石墨阴极设计电解池,通过电解NH4HSO4溶液产生(NH4)2S2O8,再与水反应得到H2O2,其中生成的NH4HSO4可以循环使用。
①阳极的电极反应式是
②制备H2O2的总反应方程式是
您最近半年使用:0次



