Ⅰ.现有下列4种重要的有机物:
① ②
② ③
③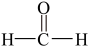 ④
④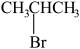
请回答:
(1)能与苯酚缩合成高分子化合物的是__________ 。(填序号)。
(2)能使酸性高锰酸钾溶液褪色的是__________ 。(填序号)。
(3)写出④在一定条件下发生消去反应的化学方程式__________ 。
Ⅱ.2020年3月22日为第28届世界水日,化学中有很多与水相关的化学知识。
(1)海水会腐蚀铁质海轮外壳,制造海轮时会在船底四周镶嵌_____ 。(填“锌块”或“铜块”)
(2)自来水厂常用含有Fe3+的净水剂净水,其原理是______ 。(用离子方程式表示)
(3)自来水常用氯气杀菌消毒,Cl2+H2O⇌HCl+HClO,要增大HClO的浓度,可以加入下列物质中的__________ 。
A.NaOH B.浓HCl C.CaCO3固体 D.H2O E.SO2
(4)常温下,0.01mol·L-1NaOH溶液,由水电离出的c(OH−)=______ mol·L-1。
①
 ②
② ③
③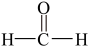 ④
④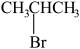
请回答:
(1)能与苯酚缩合成高分子化合物的是
(2)能使酸性高锰酸钾溶液褪色的是
(3)写出④在一定条件下发生消去反应的化学方程式
Ⅱ.2020年3月22日为第28届世界水日,化学中有很多与水相关的化学知识。
(1)海水会腐蚀铁质海轮外壳,制造海轮时会在船底四周镶嵌
(2)自来水厂常用含有Fe3+的净水剂净水,其原理是
(3)自来水常用氯气杀菌消毒,Cl2+H2O⇌HCl+HClO,要增大HClO的浓度,可以加入下列物质中的
A.NaOH B.浓HCl C.CaCO3固体 D.H2O E.SO2
(4)常温下,0.01mol·L-1NaOH溶液,由水电离出的c(OH−)=
更新时间:2020-07-15 21:42:45
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】异丁烯是一种重要的化工原料,常用于制备催化剂、农药、医药、香料、汽油添加剂及润滑油等。将异丁烷脱氢制备异丁烯具有良好的经济与社会效益,涉及的主要反应有:
反应Ⅰ: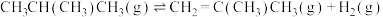

反应Ⅱ: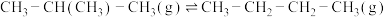

(1)已知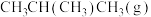 、
、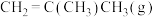 、
、 的燃烧热分别为
的燃烧热分别为 、
、 、
、 ,则
,则
_______ (用 、
、 、
、 表示)。
表示)。
(2)在恒温,2 L密闭容器中充入1 mol异丁烷,t min后达到平衡状态,异丁烷的转化率为50%,其中异丁烯的选择性为80%,则生成异丁烯的速率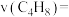
_______ 。脱氢反应的平衡常数
_______ 。(异丁烯的选择性 )
)
(3)在恒温,恒压条件下,初始反应气体组成 或
或 与平衡时异丁烷摩尔分数x的关系如图所示。
与平衡时异丁烷摩尔分数x的关系如图所示。

①其中 为曲线
为曲线_______ 。
②平衡时异丁烷摩尔分数x随 的增大而减小,其原因为
的增大而减小,其原因为_______ 。
(4)“O”表示催化剂固体杂多酸盐,“…O”表示吸附在该催化剂表面,异丁烷脱氢反应的机理如下,请补充基元反应ⅲ。
ⅰ.
ⅱ.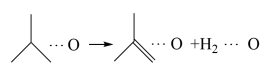
ⅲ._______
ⅳ.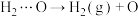
(5)有人提出加入适量空气,采用异丁烷氧化脱氢的方法制备异丁烯,发生反应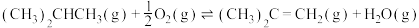
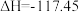 kJ/mol比较异丁烷直接脱氢制备异丁烯,从产率角度分析该方法的优点是
kJ/mol比较异丁烷直接脱氢制备异丁烯,从产率角度分析该方法的优点是_______ 。
反应Ⅰ:
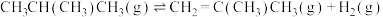

反应Ⅱ:
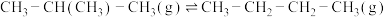

(1)已知
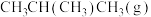 、
、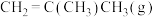 、
、 的燃烧热分别为
的燃烧热分别为 、
、 、
、 ,则
,则
 、
、 、
、 表示)。
表示)。(2)在恒温,2 L密闭容器中充入1 mol异丁烷,t min后达到平衡状态,异丁烷的转化率为50%,其中异丁烯的选择性为80%,则生成异丁烯的速率
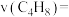

 )
)(3)在恒温,恒压条件下,初始反应气体组成
 或
或 与平衡时异丁烷摩尔分数x的关系如图所示。
与平衡时异丁烷摩尔分数x的关系如图所示。
①其中
 为曲线
为曲线②平衡时异丁烷摩尔分数x随
 的增大而减小,其原因为
的增大而减小,其原因为(4)“O”表示催化剂固体杂多酸盐,“…O”表示吸附在该催化剂表面,异丁烷脱氢反应的机理如下,请补充基元反应ⅲ。
ⅰ.

ⅱ.

ⅲ.
ⅳ.
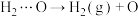
(5)有人提出加入适量空气,采用异丁烷氧化脱氢的方法制备异丁烯,发生反应
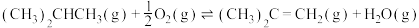
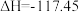 kJ/mol比较异丁烷直接脱氢制备异丁烯,从产率角度分析该方法的优点是
kJ/mol比较异丁烷直接脱氢制备异丁烯,从产率角度分析该方法的优点是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】目前工业上可利用CO或CO2来生产燃料甲醇,某研究小组对下列有关甲醇制取的三条化学反应原理进行探究。已知在不同温度下的化学反应平衡常数(K1、K2、K3)如下表所示:
请回答下列问题:
(1)反应②是__________ (填“吸热”或“放热”)反应。
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=___________ (用K1、K2表示);根据反应③判断△S__________ 0(填“>”、“=”或“<”),在____________ (填“较高”或“较低”)温度下有利于该反应自发进行。
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有______________ (填写字母序号)。
a.缩小反应容器的容积
b.扩大反应容器的容积
c.升高温度
d.使用合适的催化剂
e.从平衡体系中及时分离出CH3OH
(4)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol·L-1、0.8mol·L-1、0.3mol·L-1、0.15mol·L-1,则此时v正__________ v逆(填“>”、“=”或“<”)。
(5)某兴趣小组研究反应②的逆反应速率在下列不同条件随时间的变化曲线,开始时升温,t1时平衡,t2时降压,t3时增加CO浓度,t4时又达到平衡.请画出t2至t4的曲线______ 。

| 化学反应 | 平衡常数 | 温度(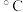 ) ) | |
| 500 | 800 | ||
①2H2(g)+CO(g) CH3OH(g) CH3OH(g) | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g) H2O(g)+CO(g) H2O(g)+CO(g) | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g) CH3OH(g)+H2O(g) CH3OH(g)+H2O(g) | K3 | ||
(1)反应②是
(2)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(3)要使反应③在一定条件下建立的平衡逆向移动,可采取的措施有
a.缩小反应容器的容积
b.扩大反应容器的容积
c.升高温度
d.使用合适的催化剂
e.从平衡体系中及时分离出CH3OH
(4)500℃时,测得反应③在某时刻,CO2(g)、H2(g)、CH3OH(g)、H2O(g)的浓度分别为0.1mol·L-1、0.8mol·L-1、0.3mol·L-1、0.15mol·L-1,则此时v正
(5)某兴趣小组研究反应②的逆反应速率在下列不同条件随时间的变化曲线,开始时升温,t1时平衡,t2时降压,t3时增加CO浓度,t4时又达到平衡.请画出t2至t4的曲线

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】减少氮的氧化物和碳的氧化物在大气中的排放是环境保护的重要内容之一。合理应用和处理碳、氮及其化合物,在生产生活中有重要意义。
(1)对温室气体二氧化碳的研究一直是科技界关注的重点。在催化剂存在下用H2还原CO2 是解决温室效应的重要手段之一,相关反应如下:
已知H2和CH4的燃烧热分别为285.5kJ/mol 和890.0kJ/mol。
H2O(1) =H2O(g) △H= +44 kJ/mol
试写出H2还原CO2生成CH4和H2O(g)的热化学方程式_____________ 。
(2)CO2在Cu-ZnO催化下,可同时发生如下的反应I、II,其可作为解决温室效应及能源短缺的重要手段。
I.CO2(g) +3H2(g) CH3OH(g) +H2O(g) △H1=-57.8 kJ/mol
CH3OH(g) +H2O(g) △H1=-57.8 kJ/mol
II.CO2(g) +H2(g) CO(g) + H2O(g) △H2 = +41.2 kJ/mol
CO(g) + H2O(g) △H2 = +41.2 kJ/mol
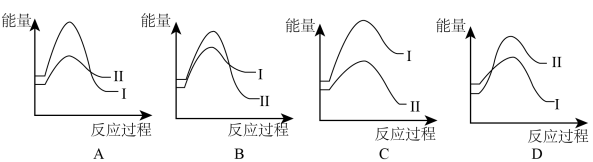
①某温度时,若反应I的速度v1大于反应II的速度以v2,则下列反应过程的能量变化正确的是_______ (填选项)。
②对于气体参加的反应,,表示平衡常数Kp时,用气体组分(B)的平衡分压p(B)代替该气体物质的量浓度c(B)。
已知:气体各组分的分压p(B),等于总压乘以其体积分数。
在Cu-ZnO存在的条件下,保持温度T时,在容积不变的密闭容器中,充入一定量的CO2 及H2,起始及达平衡时,容器内各气体物质的量如下表:
若反应I、II均达平衡时,P0=1.2p,则表中n1=____ ;若此时n2=3.则反应I的平衡常数Kp=__ (无需带单位,用含总压p的式子表示)。
(3)汽车尾气是雾霾形成的原因之一。研究氮氧化物的处理方法可有效减少雾霾的形成,可采用氧化还原法脱硝:
4NO(g) +4NH3(g) +O2(g) 4N2(g) +6H2O(g) △H <0
4N2(g) +6H2O(g) △H <0
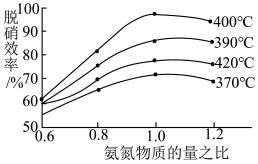
根据下图判断提高脱硝效率的最佳条件是________ ;氨氮比一定时,在400℃时,脱硝效率最大,其可能的原因是______________ 。
(4)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应:C(s) +2NO(g) N2(g) +CO2(g) △H>0
N2(g) +CO2(g) △H>0
在T℃时,反应进行到不同时间测得各物质的量浓度如下:
30min后,只改变某一条件,根据上表的数据判断改变的条件可能是_______ 。
A.通入一定量的CO2 B.加入合适的催化剂 C.适当缩小容器的体积
D.通入一定量的NO E.加入一定量的活性炭 F.适当升高温度
(1)对温室气体二氧化碳的研究一直是科技界关注的重点。在催化剂存在下用H2还原CO2 是解决温室效应的重要手段之一,相关反应如下:
已知H2和CH4的燃烧热分别为285.5kJ/mol 和890.0kJ/mol。
H2O(1) =H2O(g) △H= +44 kJ/mol
试写出H2还原CO2生成CH4和H2O(g)的热化学方程式
(2)CO2在Cu-ZnO催化下,可同时发生如下的反应I、II,其可作为解决温室效应及能源短缺的重要手段。
I.CO2(g) +3H2(g)
 CH3OH(g) +H2O(g) △H1=-57.8 kJ/mol
CH3OH(g) +H2O(g) △H1=-57.8 kJ/molII.CO2(g) +H2(g)
 CO(g) + H2O(g) △H2 = +41.2 kJ/mol
CO(g) + H2O(g) △H2 = +41.2 kJ/mol①某温度时,若反应I的速度v1大于反应II的速度以v2,则下列反应过程的能量变化正确的是

②对于气体参加的反应,,表示平衡常数Kp时,用气体组分(B)的平衡分压p(B)代替该气体物质的量浓度c(B)。
已知:气体各组分的分压p(B),等于总压乘以其体积分数。
在Cu-ZnO存在的条件下,保持温度T时,在容积不变的密闭容器中,充入一定量的CO2 及H2,起始及达平衡时,容器内各气体物质的量如下表:
| CO2 | H2 | CH3OH | CO | H2O(g) | 总压/kPa | |
| 起始/mol | 5.0 | 7.0 | 0 | 0 | 0 | p0 |
| 平衡/mol | n1 | n2 | p |
若反应I、II均达平衡时,P0=1.2p,则表中n1=
(3)汽车尾气是雾霾形成的原因之一。研究氮氧化物的处理方法可有效减少雾霾的形成,可采用氧化还原法脱硝:
4NO(g) +4NH3(g) +O2(g)
 4N2(g) +6H2O(g) △H <0
4N2(g) +6H2O(g) △H <0根据下图判断提高脱硝效率的最佳条件是

(4)用活性炭还原法也可以处理氮氧化物,某研究小组向某密闭容器加入一定量的活性炭和NO,发生反应:C(s) +2NO(g)
 N2(g) +CO2(g) △H>0
N2(g) +CO2(g) △H>0在T℃时,反应进行到不同时间测得各物质的量浓度如下:
| 时间/min 浓度/(mol/L) | 0 | 10 | 20 | 30 | 40 | 50 |
| NO | 1.0 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
| N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
| CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
30min后,只改变某一条件,根据上表的数据判断改变的条件可能是
A.通入一定量的CO2 B.加入合适的催化剂 C.适当缩小容器的体积
D.通入一定量的NO E.加入一定量的活性炭 F.适当升高温度
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】乙酸是典型的有机酸,在生产、生活中有广泛的应用。
(1)能证明 是弱酸的事实是
是弱酸的事实是___________ 。
A. 易挥发
易挥发
B.常温下, 溶液的
溶液的 大于7
大于7
C.醋酸不易腐蚀衣服
D. 的
的 溶液稀释10倍,溶液
溶液稀释10倍,溶液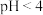
E.等体积等浓度的 溶液和盐酸,分别与足量镁粉反应,产生氢气一样多
溶液和盐酸,分别与足量镁粉反应,产生氢气一样多
F.将一定量的 溶液加入
溶液加入 溶液中,有气泡产生
溶液中,有气泡产生
(2) 时,
时, 溶液的
溶液的 ,则该温度下,水的离子积
,则该温度下,水的离子积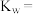
___________  ;该温度下,将
;该温度下,将 之和为13的
之和为13的 溶液和
溶液和 溶液等体积混合,所得溶液呈
溶液等体积混合,所得溶液呈___________ (填“酸”、“碱”或“中”)性。
(3)利用电催化还原 制备
制备 的装置如图所示。
的装置如图所示。___________ (填“正极”或“负极”);阴极的电极反应式为___________ 。
(4)常温下, 。
。
① 溶液中离子浓度大小关系为
溶液中离子浓度大小关系为___________ 。
②常温下,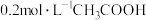 溶液和
溶液和 溶液等体积混合,所得混合溶液的
溶液等体积混合,所得混合溶液的
___________ 7(填“>”“<”或“=”)。
③某二元弱酸 的电离常数:
的电离常数: 。计算反应
。计算反应 的平衡常数为
的平衡常数为___________ (保留小数点后1位),由此说明该反应___________ (填“能发生”或“不能发生”)。
(1)能证明
 是弱酸的事实是
是弱酸的事实是A.
 易挥发
易挥发B.常温下,
 溶液的
溶液的 大于7
大于7C.醋酸不易腐蚀衣服
D.
 的
的 溶液稀释10倍,溶液
溶液稀释10倍,溶液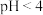
E.等体积等浓度的
 溶液和盐酸,分别与足量镁粉反应,产生氢气一样多
溶液和盐酸,分别与足量镁粉反应,产生氢气一样多F.将一定量的
 溶液加入
溶液加入 溶液中,有气泡产生
溶液中,有气泡产生(2)
 时,
时, 溶液的
溶液的 ,则该温度下,水的离子积
,则该温度下,水的离子积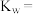
 ;该温度下,将
;该温度下,将 之和为13的
之和为13的 溶液和
溶液和 溶液等体积混合,所得溶液呈
溶液等体积混合,所得溶液呈(3)利用电催化还原
 制备
制备 的装置如图所示。
的装置如图所示。
(4)常温下,
 。
。①
 溶液中离子浓度大小关系为
溶液中离子浓度大小关系为②常温下,
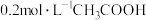 溶液和
溶液和 溶液等体积混合,所得混合溶液的
溶液等体积混合,所得混合溶液的
③某二元弱酸
 的电离常数:
的电离常数: 。计算反应
。计算反应 的平衡常数为
的平衡常数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】根据题意,完成下列填空:
(1)某温度时,测得0.1 mol·L-1的NaOH溶液的pH为13,则该温度下水的离子积常数KW=_______ 。
(2)浓度为0.1moL/L的二元弱酸H2S的水溶液中, H2S电离产生的离子有_______ 种(填数字),这几种离子中,浓度大小处于第二位的是_______ (填离子符号)。
(3)250C时,两种酸的电离平衡常数如下表所示。
①表中所列的二种酸中,酸性较弱的是_______ (写化学式)。
②向10mL0.1mol/L的H2R溶液中滴加10mL0.1mol/L的NaOH溶液充分反应后,混合溶液呈_______ 性(填酸性、碱性或中性),理由是(简略写出可做为判断理由的计算过程)______________ 。
(4)纯碱溶液呈碱性是因为它能与水发生水解反应,促进水的电离,但该溶液中由水电离产生的氢离子和氢氧根一定相等,请依此规律完善纯碱溶液中氢氧根浓度和其它相关粒子的相等关系式,即c(OH-)=_____________ 。
(1)某温度时,测得0.1 mol·L-1的NaOH溶液的pH为13,则该温度下水的离子积常数KW=
(2)浓度为0.1moL/L的二元弱酸H2S的水溶液中, H2S电离产生的离子有
(3)250C时,两种酸的电离平衡常数如下表所示。
| 化学式 | H2R | HClO |
| 电离平衡常数 | K1(H2R)=5×10-7,K2(H2R)=2×10-10 | 3.0×10-8 |
②向10mL0.1mol/L的H2R溶液中滴加10mL0.1mol/L的NaOH溶液充分反应后,混合溶液呈
(4)纯碱溶液呈碱性是因为它能与水发生水解反应,促进水的电离,但该溶液中由水电离产生的氢离子和氢氧根一定相等,请依此规律完善纯碱溶液中氢氧根浓度和其它相关粒子的相等关系式,即c(OH-)=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】成下列问题。
I.某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。
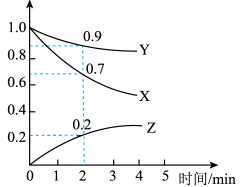
(1)由图中数据分析:该反应的化学方程式为___________ 。
(2)反应开始至2min,用Z表示的平均反应速率为___________ 。
II.回答下列有关水溶液的问题:
(3)写出下列物质的电离方程式:
NaHSO4___________
H2S___________
(4)下列两种溶液中,室温下由水电离生成的H+浓度之比(①:②)是___________ 。
①pH=1的盐酸 ②0.01mol·L-1的NaOH溶液
(5)已知在25℃和95℃时,水的电离平衡曲线如图所示:
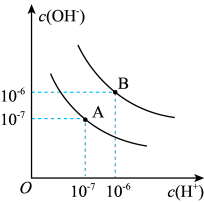
①在25℃时,水的电离平衡曲线应为________ (填“A”或“B”);95℃时水的离子积KW=______ 。
②25℃时,将pH=9的Ba(OH)2溶液与pH=4的H2SO4溶液混合,若冷却至25℃时所得混合溶液的pH=7,则Ba(OH)2溶液与H2SO4溶液的体积比为___________ 。
I.某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。

(1)由图中数据分析:该反应的化学方程式为
(2)反应开始至2min,用Z表示的平均反应速率为
II.回答下列有关水溶液的问题:
(3)写出下列物质的电离方程式:
NaHSO4
H2S
(4)下列两种溶液中,室温下由水电离生成的H+浓度之比(①:②)是
①pH=1的盐酸 ②0.01mol·L-1的NaOH溶液
(5)已知在25℃和95℃时,水的电离平衡曲线如图所示:

①在25℃时,水的电离平衡曲线应为
②25℃时,将pH=9的Ba(OH)2溶液与pH=4的H2SO4溶液混合,若冷却至25℃时所得混合溶液的pH=7,则Ba(OH)2溶液与H2SO4溶液的体积比为
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】根据有关信息完成下列各题:
(1)有机物A是有机物B( )的同分异构体,核磁共振氢谱测得其分子中只有两种不同化学环境的氢,且数目比为1:3,写出其中三种的结构简式:
)的同分异构体,核磁共振氢谱测得其分子中只有两种不同化学环境的氢,且数目比为1:3,写出其中三种的结构简式:____ 、____ 、____ 。
(2)有机物B在一定条件下反应生成有机物C,1mol有机物C最多可以和2molBr2发生加成反应,写出有机物B在一定条件下反应生成有机物C的化学方程式:____ 。
(3)已知: 。
。
写出用 为原料(其他无机试剂任选)制备高分子
为原料(其他无机试剂任选)制备高分子 的合成路线
的合成路线____ 。合成反应流程图表示方法例如:
(1)有机物A是有机物B(
 )的同分异构体,核磁共振氢谱测得其分子中只有两种不同化学环境的氢,且数目比为1:3,写出其中三种的结构简式:
)的同分异构体,核磁共振氢谱测得其分子中只有两种不同化学环境的氢,且数目比为1:3,写出其中三种的结构简式:(2)有机物B在一定条件下反应生成有机物C,1mol有机物C最多可以和2molBr2发生加成反应,写出有机物B在一定条件下反应生成有机物C的化学方程式:
(3)已知:
 。
。写出用
 为原料(其他无机试剂任选)制备高分子
为原料(其他无机试剂任选)制备高分子 的合成路线
的合成路线
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐2】环己烷可制备1,4-环己二醇,下列七步有关反应(其中无机产物都已经略去)中,其中有两步属于取代反应,两步属于消去反应,三步属于加成反应,试回答:

(1)写出下列化合物的结构简式:A:_______ C:_______
(2)①的化学方程式_______ ;反应类型______
②的化学方程式_______ 。

(1)写出下列化合物的结构简式:A:
(2)①的化学方程式
②的化学方程式
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
解题方法
【推荐3】已知可由乙烯合成高分子材料G 。
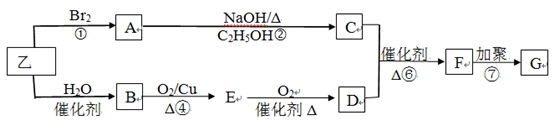
F的质谱图中最大质荷比为86, 其C、H、O的原子个数之比为2:3:1,F在酸性条件下水解可生成碳原子数相同的两种有机物D和E。请回答下列问题:
(1)B的分子式为________________ ,F分子含氧官能团的名称为_____________ 。
(2)E的结构简式为______________ ,G的结构简式为______________ 。
(3)反应①、⑥的反应类型均是__________________ 。
(4)反应②的化学方程式为______________________ 。
(5)在F的同分异构体中,核磁共振氢谱有三个峰,三个峰的面积之比为1:1:1,任意写出其中一种满足上述条件的结构简式____________________________ 。

F的质谱图中最大质荷比为86, 其C、H、O的原子个数之比为2:3:1,F在酸性条件下水解可生成碳原子数相同的两种有机物D和E。请回答下列问题:
(1)B的分子式为
(2)E的结构简式为
(3)反应①、⑥的反应类型均是
(4)反应②的化学方程式为
(5)在F的同分异构体中,核磁共振氢谱有三个峰,三个峰的面积之比为1:1:1,任意写出其中一种满足上述条件的结构简式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】实验室制备酚醛树脂的实验装置如图所示,主要步骤如下:

①在大试管中加入2 g苯酚和3 mL 40%的甲醛溶液。
②再加入1 mL浓盐酸,装好实验装置。
③将试管水浴加热至沸腾,到反应不再剧烈进行时,过一会儿便可停止加热。
④取出试管中的黏稠固体,用水洗净得到产品。
填写下列空白:
(1)在装置中,试管口加一带塞的长直导管的作用是_______ 。
(2)加入浓盐酸的作用是_______ 。若要形成网状结构的酚醛树脂还可用_______ 代替浓盐酸。
(3)此反应需水浴加热,不用温度计控制水浴温度的原因是_______ 。
(4)采用水浴加热的好处是_______ 。再列举两个需要水浴加热的有机实验,写出实验的名称:_______ 。
(5)实验完毕后,若试管用水不易洗涤,可以加入少量_______ 浸泡几分钟,然后洗净。
(6)写出实验室制取酚醛树脂的化学方程式:_______ ,此有机反应类型是_______ 。
(7)该实验装置中的一处错误是_______ 。

①在大试管中加入2 g苯酚和3 mL 40%的甲醛溶液。
②再加入1 mL浓盐酸,装好实验装置。
③将试管水浴加热至沸腾,到反应不再剧烈进行时,过一会儿便可停止加热。
④取出试管中的黏稠固体,用水洗净得到产品。
填写下列空白:
(1)在装置中,试管口加一带塞的长直导管的作用是
(2)加入浓盐酸的作用是
(3)此反应需水浴加热,不用温度计控制水浴温度的原因是
(4)采用水浴加热的好处是
(5)实验完毕后,若试管用水不易洗涤,可以加入少量
(6)写出实验室制取酚醛树脂的化学方程式:
(7)该实验装置中的一处错误是
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
【推荐2】已知B和E分别是生产酚醛树脂和有机玻璃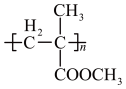 的重要原料。工业上生产B和E的一种途径是:
的重要原料。工业上生产B和E的一种途径是:
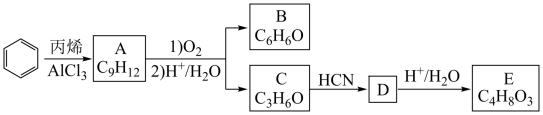
①A为苯的同系物,其一氯代物有5种;
②C、D、E的核磁共振氢谱图中峰的个数分别为1,2,3;
③等量的E分别与足量的Na和足量的 溶液反应,在相同条件下,生成的气体气体相同。
溶液反应,在相同条件下,生成的气体气体相同。
回答下列问题:
(1)C分子中所含官能团的名称是_______ 。
(2)C→D的反应类型是_______ 。
(3)A的含有苯环的同分异构体(除A外)有_______ 种。
(4)糠醛(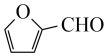 )是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂(线型),写出该反应的化学方程式
)是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂(线型),写出该反应的化学方程式_______ 。
(5)E有多种脱水产物,其中F具有六元环状结构,G是一种聚酯高分子材料,写出F和G的结构简式,F:_______ 、G:_______ 。
 的重要原料。工业上生产B和E的一种途径是:
的重要原料。工业上生产B和E的一种途径是:
①A为苯的同系物,其一氯代物有5种;
②C、D、E的核磁共振氢谱图中峰的个数分别为1,2,3;
③等量的E分别与足量的Na和足量的
 溶液反应,在相同条件下,生成的气体气体相同。
溶液反应,在相同条件下,生成的气体气体相同。回答下列问题:
(1)C分子中所含官能团的名称是
(2)C→D的反应类型是
(3)A的含有苯环的同分异构体(除A外)有
(4)糠醛(
 )是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂(线型),写出该反应的化学方程式
)是一种重要的化工原料,如同甲醛与苯酚反应生成酚醛树脂,它也可与苯酚反应生成糠醛树脂(线型),写出该反应的化学方程式(5)E有多种脱水产物,其中F具有六元环状结构,G是一种聚酯高分子材料,写出F和G的结构简式,F:
您最近一年使用:0次
解答题-有机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】文拉法辛(化合物H)是一种用于治疗各类抑郁症的药物,其合成路线如下图所示。
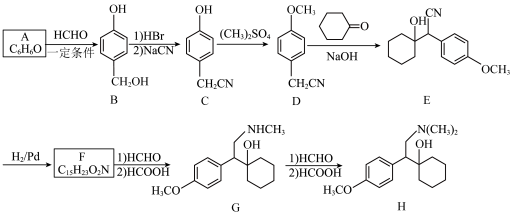
回答下列问题:
(1)A的化学名称是___________ 。
(2)D→E的反应类型是___________ 。
(3)F的结构简式为___________ 。
(4)G的含氧官能团名称为___________ 。
(5)A与HCHO反应形成线型结构高分子的反应方程式为___________ 。
(6)在D的同分异构体中,同时满足下列条件的共有___________ 种(不考虑立体异构)。
a.能使溴水褪色 b.含有酰胺基 c.含有苯环,不含其它环状
其中核磁共振氢谱有5组峰,且峰面积之比为2∶2∶2∶2∶1的同分异构体的结构简式为________ (只写一种)。

回答下列问题:
(1)A的化学名称是
(2)D→E的反应类型是
(3)F的结构简式为
(4)G的含氧官能团名称为
(5)A与HCHO反应形成线型结构高分子的反应方程式为
(6)在D的同分异构体中,同时满足下列条件的共有
a.能使溴水褪色 b.含有酰胺基 c.含有苯环,不含其它环状
其中核磁共振氢谱有5组峰,且峰面积之比为2∶2∶2∶2∶1的同分异构体的结构简式为
您最近一年使用:0次



