解题方法
1 . 25℃时,H2CO3的Ka1=4.5×10−7,Ka2=4.8×10−11。请回答:
(1)25℃时,水的离子积Kw=_______ 。
(2)NaHCO3溶液显_______ (填“酸性”、“中性”或“碱性”),结合数据 分析其原因是_______ 。
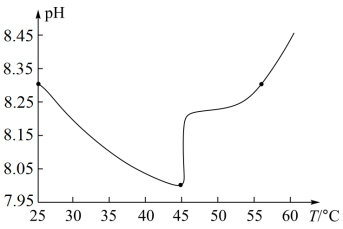
(3)某实验测得0.050 mol·L−1 NaHCO3溶液在加热过程中的pH变化如图所示。试分析45℃后,随温度升高NaHCO3溶液pH增大的原因是_______ 。
(4)氯气通入NaHCO3溶液中产生无色气体,该反应的离子方程式是_______ 。
(1)25℃时,水的离子积Kw=
(2)NaHCO3溶液显
(3)某实验测得0.050 mol·L−1 NaHCO3溶液在加热过程中的pH变化如图所示。试分析45℃后,随温度升高NaHCO3溶液pH增大的原因是

(4)氯气通入NaHCO3溶液中产生无色气体,该反应的离子方程式是
您最近一年使用:0次
2022-03-06更新
|
231次组卷
|
2卷引用:浙江省丽水市2021-2022学年高二上学期普通高中教学质量监控(期末)化学试题
20-21高二·浙江·阶段练习
2 . (1)在水的电离平衡中,c(H+)和c(OH-)的关系如图所示。A点水的离子积为1.0×10-14,B点水的离子积为_______ 。

(2)下列说法正确的是_______ (填字母)。
a. 图中A、B、D三点处Kw的大小关系:B>A>D
b. AB线上任意点的溶液均显中性
c. B点溶液的pH=6,显酸性
d. 图中温度T1>T2
(3)T2时,若盐酸中c(H+)=5×10-4mol·L-1,则由水电离产生的c(H+)=_______ 。

(2)下列说法正确的是
a. 图中A、B、D三点处Kw的大小关系:B>A>D
b. AB线上任意点的溶液均显中性
c. B点溶液的pH=6,显酸性
d. 图中温度T1>T2
(3)T2时,若盐酸中c(H+)=5×10-4mol·L-1,则由水电离产生的c(H+)=
您最近一年使用:0次
名校
3 . 回答下列问题:
(1) 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为___________ mol·L-1。
(2) 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
___________ ,溶液中 为
为___________ mol·L-1。
(3) 时,
时,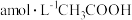 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
___________ 。
(1)
 时,
时, 的盐酸中由水电离出的
的盐酸中由水电离出的 为
为(2)
 时,向
时,向 的蒸馏水中加入
的蒸馏水中加入 晶体,保持温度不变,测得溶液的
晶体,保持温度不变,测得溶液的 。此时水的离子积
。此时水的离子积
 为
为(3)
 时,
时,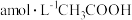 溶液的
溶液的 ,用含a和b的代数式表示
,用含a和b的代数式表示 的电离平衡常数
的电离平衡常数
您最近一年使用:0次
2021-03-01更新
|
245次组卷
|
2卷引用:浙江省温州市平阳县万全综合高级中学2021-2022学年高二上学期期中考试化学试题
4 . (1)某温度(t℃)时,测得0.01 mol·L-1 NaOH溶液的pH=13,请回答下列问题:
①该温度下水的Kw=________ 。
②此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va︰Vb=________ 。
(2)25℃时,pH=a的20mL的H2SO4溶液与c(H+)=10-b的200mL的NaOH溶液混合后,溶液呈中性,则a和b满足的关系_______ 。
①该温度下水的Kw=
②此温度下,将pH=a的NaOH溶液VaL与pH=b的H2SO4溶液VbL混合(忽略体积变化),若所得混合液为中性,且a=12,b=2,则Va︰Vb=
(2)25℃时,pH=a的20mL的H2SO4溶液与c(H+)=10-b的200mL的NaOH溶液混合后,溶液呈中性,则a和b满足的关系
您最近一年使用:0次
9-10高二下·江苏宿迁·期中
解题方法
5 . 已知水在25℃和95℃时,其电离平衡曲线如右图所示:

(1)25℃时,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,混合所得溶液的pH=7,则NaOH溶液与溶液的体积比为__________ 。
(2)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是__________ 。
(3)95℃时,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5 ,则HA是____________ (填“强酸”或“弱酸”)。

(1)25℃时,将pH=9的NaOH溶液与pH=4的盐酸溶液混合,混合所得溶液的pH=7,则NaOH溶液与溶液的体积比为
(2)95℃时,若100体积pH1=a的某强酸溶液与1体积pH2=b的某强碱溶液混合后溶液呈中性,则混合前,该强酸的pH1与强碱的pH2之间应满足的关系是
(3)95℃时,pH=2的某HA溶液和pH=10的NaOH溶液等体积混合后,混合溶液的pH=5 ,则HA是
您最近一年使用:0次
名校
6 . 某温度下的水溶液中,c(H+)=10xmol/L,c(OH-)=10ymol/L。x与y的关系如图所示:

(1)该温度下水的离子积为_____ 。
(2)该温度下0.01 mol/L的NaOH溶液pH为___ 。

(1)该温度下水的离子积为
(2)该温度下0.01 mol/L的NaOH溶液pH为
您最近一年使用:0次
2016-12-09更新
|
325次组卷
|
2卷引用:2014-2015浙江省嘉兴一中高二上学期期中化学(文)试卷
9-10高二下·浙江杭州·期中
7 . 常温下,将0.01 mol·L-1的Ba(OH)2溶液200mL和0.01 mol·L-1的NaHSO4溶液100mL混合,反应过程中生成______ g沉淀,反应后溶液的pH值为______________________ 。
您最近一年使用:0次
9-10高二下·浙江舟山·期末
8 . 一定温度下,测得某纯水的pH为6.5。试计算:
(1)此时水的离子积常数Kw为________ ?
(2)若在此纯水中加一定量Ba(OH)2固体,配制成0.005mol·L-1。的Ba(OH)2溶液,保持原温度,其溶液的pH为________ ?
(3)取上述Ba(OH)2溶液200mL,加入含0.01mol Na2SO4的浓溶液,待反应完全后,上层清液中Ba2+浓度变为________ ?[体积变化忽略不计,Ksp(BaSO4)=1.08×10-10]
(1)此时水的离子积常数Kw为
(2)若在此纯水中加一定量Ba(OH)2固体,配制成0.005mol·L-1。的Ba(OH)2溶液,保持原温度,其溶液的pH为
(3)取上述Ba(OH)2溶液200mL,加入含0.01mol Na2SO4的浓溶液,待反应完全后,上层清液中Ba2+浓度变为
您最近一年使用:0次
9 . 某温度下的溶液中c (H+)=1.0×10xmol/L,c (OH-)=1.0×10ymol/L。x与y的关系如图所示:

(1)求该温度下,中性溶液的pH___ ;
(2)求该温度下0.01mol/LNaOH溶液的pH___ ;
(3)该温度下,pH=a的醋酸溶液与pH=b的NaOH溶液等体积混合,恰好完全反应,求此醋酸溶液中醋酸的电离度____ 。

(1)求该温度下,中性溶液的pH
(2)求该温度下0.01mol/LNaOH溶液的pH
(3)该温度下,pH=a的醋酸溶液与pH=b的NaOH溶液等体积混合,恰好完全反应,求此醋酸溶液中醋酸的电离度
您最近一年使用:0次



