解题方法
1 . 25℃时,H2CO3的Ka1=4.5×10−7,Ka2=4.8×10−11。请回答:
(1)25℃时,水的离子积Kw=_______ 。
(2)NaHCO3溶液显_______ (填“酸性”、“中性”或“碱性”),结合数据 分析其原因是_______ 。
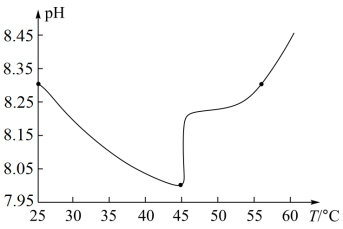
(3)某实验测得0.050 mol·L−1 NaHCO3溶液在加热过程中的pH变化如图所示。试分析45℃后,随温度升高NaHCO3溶液pH增大的原因是_______ 。
(4)氯气通入NaHCO3溶液中产生无色气体,该反应的离子方程式是_______ 。
(1)25℃时,水的离子积Kw=
(2)NaHCO3溶液显
(3)某实验测得0.050 mol·L−1 NaHCO3溶液在加热过程中的pH变化如图所示。试分析45℃后,随温度升高NaHCO3溶液pH增大的原因是

(4)氯气通入NaHCO3溶液中产生无色气体,该反应的离子方程式是
您最近一年使用:0次
2022-03-06更新
|
232次组卷
|
2卷引用:浙江省丽水市2021-2022学年高二上学期普通高中教学质量监控(期末)化学试题
9-10高二下·浙江舟山·期末
2 . 一定温度下,测得某纯水的pH为6.5。试计算:
(1)此时水的离子积常数Kw为________ ?
(2)若在此纯水中加一定量Ba(OH)2固体,配制成0.005mol·L-1。的Ba(OH)2溶液,保持原温度,其溶液的pH为________ ?
(3)取上述Ba(OH)2溶液200mL,加入含0.01mol Na2SO4的浓溶液,待反应完全后,上层清液中Ba2+浓度变为________ ?[体积变化忽略不计,Ksp(BaSO4)=1.08×10-10]
(1)此时水的离子积常数Kw为
(2)若在此纯水中加一定量Ba(OH)2固体,配制成0.005mol·L-1。的Ba(OH)2溶液,保持原温度,其溶液的pH为
(3)取上述Ba(OH)2溶液200mL,加入含0.01mol Na2SO4的浓溶液,待反应完全后,上层清液中Ba2+浓度变为
您最近一年使用:0次



