某温度下的水溶液中,c(H+)=10xmol/L,c(OH-)=10ymol/L。x与y的关系如图所示:

(1)该温度下水的离子积为_____ 。
(2)该温度下0.01 mol/L的NaOH溶液pH为___ 。

(1)该温度下水的离子积为
(2)该温度下0.01 mol/L的NaOH溶液pH为
更新时间:2016-12-09 07:00:40
|
相似题推荐
计算题
|
较易
(0.85)
解题方法
【推荐1】在某温度下的水溶液中, ,
,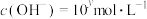 ,x与y的关系如图所示:
,x与y的关系如图所示:

(1)该温度下,水的离子积为______  。
。
(2)该温度下, NaOH溶液中
NaOH溶液中 为
为______ 。
 ,
,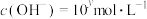 ,x与y的关系如图所示:
,x与y的关系如图所示:
(1)该温度下,水的离子积为
 。
。(2)该温度下,
 NaOH溶液中
NaOH溶液中 为
为
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐2】在某温度(T ℃)的水溶液中,c(H+)=10x mol/L,c(OH-)=10y mol/L,x与y关系如图所示。

(1)该温度下,水的离子积为________ ,T ℃_____ 25 ℃(填“大于”“小于”或“等于”)。
(2)将此温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为________ 。(已知lg2=0.3)
(3)在此温度下,将pH=13的NaOH溶液Va L与pH=1的硫酸溶液Vb L混合。若所得混合液的pH=2,则Va:Vb =_______ 。

(1)该温度下,水的离子积为
(2)将此温度下pH=11的NaOH溶液与pH=1的HCl溶液等体积混合,混合后溶液的pH约为
(3)在此温度下,将pH=13的NaOH溶液Va L与pH=1的硫酸溶液Vb L混合。若所得混合液的pH=2,则Va:Vb =
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】常温下有一PH为12的NaOH溶液100mL,如果将其PH将为11,那么
(1)若用蒸馏水应加入___ mL (2)若用PH=10的NaOH溶液应加入___ mL
(3)若用PH=2的盐酸应加入___ mL (4)若用0.01mol/L的硫酸溶液应加入___ mL
(1)若用蒸馏水应加入
(3)若用PH=2的盐酸应加入
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】Ⅰ.某温度(T℃)的溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-ymol·L-1,x与y的关系如图所示:
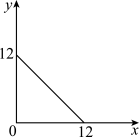
此温度下,0.01mol/L的NaOH溶液中水电离出的OH-浓度为____________ 。
Ⅱ.常温下,如果取 0.1 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)求出混合溶液中下列算式的精确计算结果(填具体数字):c(Na+)-c(A-)=________ mol·L-1,c(OH-)-c(HA)=________ mol·L-1;
(2)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH____ 7(填“>”、“<”或“=”)。

此温度下,0.01mol/L的NaOH溶液中水电离出的OH-浓度为
Ⅱ.常温下,如果取 0.1 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)求出混合溶液中下列算式的精确计算结果(填具体数字):c(Na+)-c(A-)=
(2)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐3】某温度下,纯水中c(H+)=1.0×10-6 mol·L-1,则此时c(OH-)=_____ mol·L-1。
在此温度下,将100 mL pH=1的稀硫酸和盐酸的混合液与100 mL未知浓度的Ba (OH)2溶液相混合,充分反应后过滤,得0.233g沉淀,滤液的pH值变为11(设混合液体积为两者之和,所得固体体积忽略不计)。则原混合酸液中SO42-的物质的量=____ mol;Cl-的物质的量=_____ mol;Ba(OH)2的物质的量浓度=______ mol·L-1 。
在此温度下,将100 mL pH=1的稀硫酸和盐酸的混合液与100 mL未知浓度的Ba (OH)2溶液相混合,充分反应后过滤,得0.233g沉淀,滤液的pH值变为11(设混合液体积为两者之和,所得固体体积忽略不计)。则原混合酸液中SO42-的物质的量=
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】N2H4的水溶液呈弱碱性,室温下其电离常数K1=1.0×10-6,则0.01 mol·L-1 N2H4水溶液的pH等于__________ 。(忽略N2H4的二级电离和H2O的电离)
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】向0.1mol/LNaOH溶液中加入等体积的cmol/L醋酸溶液后恰好呈中性(忽略溶液混合时的体积变化)。回答下列问题:
(1)混合溶液中离子浓度大小顺序为:___ ;
(2)计算CH3COOH的电离常数Ka=___ (用含c的代数式表示)。
(1)混合溶液中离子浓度大小顺序为:
(2)计算CH3COOH的电离常数Ka=
您最近一年使用:0次

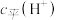 为
为 ,根据
,根据 ,则该酸溶液中的
,则该酸溶液中的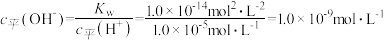 。
。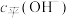 ,请填上空缺的数据。
,请填上空缺的数据。
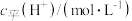
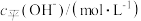

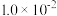




 某一元弱酸
某一元弱酸 的电离平衡常数约为
的电离平衡常数约为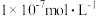 ,该溶液的pH为
,该溶液的pH为

