向0.1mol/LNaOH溶液中加入等体积的cmol/L醋酸溶液后恰好呈中性(忽略溶液混合时的体积变化)。回答下列问题:
(1)混合溶液中离子浓度大小顺序为:___ ;
(2)计算CH3COOH的电离常数Ka=___ (用含c的代数式表示)。
(1)混合溶液中离子浓度大小顺序为:
(2)计算CH3COOH的电离常数Ka=
更新时间:2020-02-26 19:10:20
|
相似题推荐
计算题
|
较易
(0.85)
【推荐1】已知室温时, 某一元弱酸
某一元弱酸 的电离平衡常数约为
的电离平衡常数约为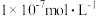 ,该溶液的pH为
,该溶液的pH为________ (列式计算)。
 某一元弱酸
某一元弱酸 的电离平衡常数约为
的电离平衡常数约为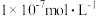 ,该溶液的pH为
,该溶液的pH为
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】六亚甲基四胺(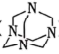 )的水溶液呈弱碱性,室温下其电离常数K1≈1.0×10-8。
)的水溶液呈弱碱性,室温下其电离常数K1≈1.0×10-8。
(1)室温下,0.01 mol/L 六亚甲基四胺水溶液的pH等于_______ ( 只考虑六亚甲基四胺的一级电离,忽略H2O的电离)。
(2)利用上述数据列式计算六亚甲基四胺的电离度____________ 。
 )的水溶液呈弱碱性,室温下其电离常数K1≈1.0×10-8。
)的水溶液呈弱碱性,室温下其电离常数K1≈1.0×10-8。(1)室温下,0.01 mol/L 六亚甲基四胺水溶液的pH等于
(2)利用上述数据列式计算六亚甲基四胺的电离度
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】按要求回答下列问题:
(1)25 ℃时,Kb(NH3·H2O)=1.8×10−5;H2SO3:Ka1=1.5×10−2,Ka2=1.0×10−7;Ksp(CaSO4)=7.1×10−5
第1步:用过量的浓氨水吸收SO2,并在空气中氧化;
第2步:加入石灰水,发生反应:Ca2++2OH-+2 +
+
 CaSO4↓+2NH3·H2O K
CaSO4↓+2NH3·H2O K
①25 ℃时,0.1 mol∙L−1 (NH4)2SO3溶液的pH___________ (填“>”“<”或“=”)7
②计算第2步中反应的K=___________
(2)“亚硫酸盐法”吸收烟气中的SO2
①将烟气通入1.0 mol∙L−1的Na2SO3溶液,若此过程中溶液体积不变,则溶液的pH不断___________ (填“减小”“不变”或“增大”)。当溶液pH约为6时,吸收SO2的能力显著下降,应更换吸收剂,此时溶液中c( )=0.2 mol∙L−1,则溶液中c(
)=0.2 mol∙L−1,则溶液中c( )=
)=___________
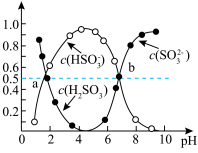
②室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与各组分物质的量分数的变化关系如图。b点时溶液pH=7,则n( )∶n(
)∶n( )=
)=___________
(3)常温下,H2CO3的电离常数为Ka1=4×10−7,Ka2=4×10−11。已知0.1 mol∙L−1 NH4HCO3溶液的pH=8,则在此溶液中:
①下列有关离子浓度的关系式中,不正确的是___________
A.c( )>c(
)>c( )>c(OH-)>c(H+)
)>c(OH-)>c(H+)
B.c( )+c(NH3·H2O)=c(
)+c(NH3·H2O)=c( )+c(H2CO3)
)+c(H2CO3)
C.c(H2CO3) −c( )−c(NH3·H2O)=9.9×10-7 mol∙L−1
)−c(NH3·H2O)=9.9×10-7 mol∙L−1
②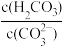 =
=___________
(1)25 ℃时,Kb(NH3·H2O)=1.8×10−5;H2SO3:Ka1=1.5×10−2,Ka2=1.0×10−7;Ksp(CaSO4)=7.1×10−5
第1步:用过量的浓氨水吸收SO2,并在空气中氧化;
第2步:加入石灰水,发生反应:Ca2++2OH-+2
 +
+
 CaSO4↓+2NH3·H2O K
CaSO4↓+2NH3·H2O K①25 ℃时,0.1 mol∙L−1 (NH4)2SO3溶液的pH
②计算第2步中反应的K=
(2)“亚硫酸盐法”吸收烟气中的SO2
①将烟气通入1.0 mol∙L−1的Na2SO3溶液,若此过程中溶液体积不变,则溶液的pH不断
 )=0.2 mol∙L−1,则溶液中c(
)=0.2 mol∙L−1,则溶液中c( )=
)=②室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与各组分物质的量分数的变化关系如图。b点时溶液pH=7,则n(
 )∶n(
)∶n( )=
)=
(3)常温下,H2CO3的电离常数为Ka1=4×10−7,Ka2=4×10−11。已知0.1 mol∙L−1 NH4HCO3溶液的pH=8,则在此溶液中:
①下列有关离子浓度的关系式中,不正确的是
A.c(
 )>c(
)>c( )>c(OH-)>c(H+)
)>c(OH-)>c(H+)B.c(
 )+c(NH3·H2O)=c(
)+c(NH3·H2O)=c( )+c(H2CO3)
)+c(H2CO3)C.c(H2CO3) −c(
 )−c(NH3·H2O)=9.9×10-7 mol∙L−1
)−c(NH3·H2O)=9.9×10-7 mol∙L−1②
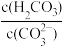 =
=
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐2】(1)一定条件下,在水的电离平衡中,c(H+)和c(OH-)的关系如下图所示。100 ℃时,若盐酸中c(H+)=5×10-4 mol·L-1,则由水电离产生的c(H+)=__________ 。
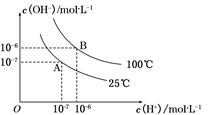
(2)pH=3的盐酸与pH=5的盐酸等体积混合,pH=_________ 。
(3)25℃时,在0.5L0.2mol/L的HA溶液中,有0.02mol的HA电离成离子,则该温度下的电离常数为_____________ 。

(2)pH=3的盐酸与pH=5的盐酸等体积混合,pH=
(3)25℃时,在0.5L0.2mol/L的HA溶液中,有0.02mol的HA电离成离子,则该温度下的电离常数为
您最近一年使用:0次
计算题
|
较易
(0.85)
名校
解题方法
【推荐3】Ⅰ.某温度(T℃)的溶液中,c(H+)=10-xmol·L-1,c(OH-)=10-ymol·L-1,x与y的关系如图所示:
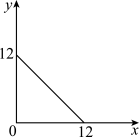
此温度下,0.01mol/L的NaOH溶液中水电离出的OH-浓度为____________ 。
Ⅱ.常温下,如果取 0.1 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)求出混合溶液中下列算式的精确计算结果(填具体数字):c(Na+)-c(A-)=________ mol·L-1,c(OH-)-c(HA)=________ mol·L-1;
(2)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH____ 7(填“>”、“<”或“=”)。

此温度下,0.01mol/L的NaOH溶液中水电离出的OH-浓度为
Ⅱ.常温下,如果取 0.1 mol·L-1 HA溶液与0.1 mol·L-1 NaOH溶液等体积混合(忽略混合后溶液体积的变化),测得混合溶液的pH=8,试回答以下问题:
(1)求出混合溶液中下列算式的精确计算结果(填具体数字):c(Na+)-c(A-)=
(2)已知NH4A溶液为中性,又知HA溶液加到Na2CO3溶液中有气体放出,试推断(NH4)2CO3溶液的pH
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐1】(1)联氨( )是二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为
)是二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为______ 。(已知: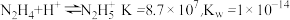 ),联氨与硫酸形成的酸式盐的化学式为
),联氨与硫酸形成的酸式盐的化学式为_______ 。
(2)0.20mol/L的小苏打溶液中各离子浓度由小到大的顺序是___ 。
(3)如图所示为二元酸H2A溶液中各微粒的物质的量分数(δ)随溶液pH的变化曲线(25°C)。
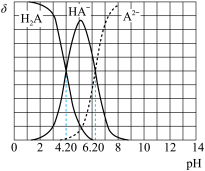
H2A的电离平衡常数 =
=_________ ,溶液pH=7时,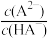 =
=_______ 。
 )是二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为
)是二元弱碱,在水中的电离方程式与氨相似,联氨第一步电离反应的平衡常数值为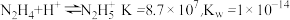 ),联氨与硫酸形成的酸式盐的化学式为
),联氨与硫酸形成的酸式盐的化学式为(2)0.20mol/L的小苏打溶液中各离子浓度由小到大的顺序是
(3)如图所示为二元酸H2A溶液中各微粒的物质的量分数(δ)随溶液pH的变化曲线(25°C)。

H2A的电离平衡常数
 =
=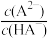 =
=
您最近一年使用:0次
计算题
|
较易
(0.85)
【推荐2】在常温下,用煮沸过的蒸馏水溶解14gKOH配成250mL溶液,取出50mL溶液与CO2恰好完全反应(溶液体积变化忽略不计)。
(1)取出的50mLKOH溶液的pH=___________ 。
(2)若反应后溶液中c(CO32-)=c(HCO3-),则溶液中c(HCO3-)=_______ mol·L-1(H2CO3忽略不计,计算结果保留2位有效数字)。
(1)取出的50mLKOH溶液的pH=
(2)若反应后溶液中c(CO32-)=c(HCO3-),则溶液中c(HCO3-)=
您最近一年使用:0次
计算题
|
较易
(0.85)
解题方法
【推荐3】电解质在水溶液中存在各种行为,如电离、水解等,依据所学知识回答下列问题:
(1)t℃时,纯水中c(H+)=1×10-6mol·L-1,该温度下,pH=10的NaOH溶液的物质的量浓度为___ 。
(2)25℃时,相同物质的量浓度的下列溶液中:①NaCl②NH3·H2O③H2SO4④(NH4)2SO4,其中水的电离程度由大到小顺序为___ (填标号)。
(3)25℃时,将amol·L-1的醋酸和bmol·L-1的氢氧化钠溶液等体积混合后,溶液的pH=7,则a___ b(填“>”“<”或“=”)。
(1)t℃时,纯水中c(H+)=1×10-6mol·L-1,该温度下,pH=10的NaOH溶液的物质的量浓度为
(2)25℃时,相同物质的量浓度的下列溶液中:①NaCl②NH3·H2O③H2SO4④(NH4)2SO4,其中水的电离程度由大到小顺序为
(3)25℃时,将amol·L-1的醋酸和bmol·L-1的氢氧化钠溶液等体积混合后,溶液的pH=7,则a
您最近一年使用:0次



