1 . 填空
(1)25℃时,亚碲酸( )的
)的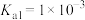 ,
,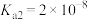 。常温下,
。常温下, 溶液的pH
溶液的pH______ (填“<”“>”或“=”)7。
(2)已知25℃时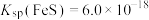 ,要使溶液中
,要使溶液中 沉淀完全[
沉淀完全[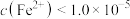 mol⋅L
mol⋅L ],则需控制溶液中
],则需控制溶液中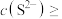
______ 。
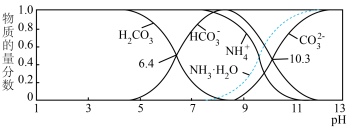
(3)室温下,测得用氨水吸收 时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液
时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液 ,则溶液中
,则溶液中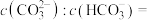
______ (已知) )。
)。
(4)若向浓烧碱溶液中通入 气体,使所得溶液
气体,使所得溶液 ,则此时溶液中的
,则此时溶液中的
______ mol⋅L (室温下,
(室温下, 的
的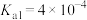 ,
,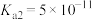 )。
)。
(5)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体 ,其产物之一是
,其产物之一是 。已知常温下碳酸的电离常数
。已知常温下碳酸的电离常数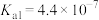 ,
, ,
, 的电离常数
的电离常数 ,则所得的
,则所得的 溶液中
溶液中
______ (填“>”“<”或“=”) 。
。
(6) 是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
①根据实验现象写出 和
和 反应的化学方程式:
反应的化学方程式:____________ 。
②利用 制备无水
制备无水 时,可用
时,可用 和
和 混合共热,试解释原因:
混合共热,试解释原因:____________ 。
(1)25℃时,亚碲酸(
 )的
)的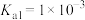 ,
,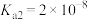 。常温下,
。常温下, 溶液的pH
溶液的pH(2)已知25℃时
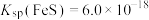 ,要使溶液中
,要使溶液中 沉淀完全[
沉淀完全[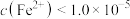 mol⋅L
mol⋅L ],则需控制溶液中
],则需控制溶液中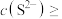
(3)室温下,测得用氨水吸收
 时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液
时,溶液中含碳(氮)各粒子的物质的量分数和pH的关系如图,若所得溶液 ,则溶液中
,则溶液中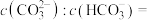
 )。
)。
(4)若向浓烧碱溶液中通入
 气体,使所得溶液
气体,使所得溶液 ,则此时溶液中的
,则此时溶液中的
 (室温下,
(室温下, 的
的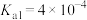 ,
,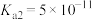 )。
)。(5)工业上常用氨水吸收含碳燃料燃烧中产生的温室气体
 ,其产物之一是
,其产物之一是 。已知常温下碳酸的电离常数
。已知常温下碳酸的电离常数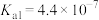 ,
, ,
, 的电离常数
的电离常数 ,则所得的
,则所得的 溶液中
溶液中
 。
。(6)
 是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。
是一种液态化合物,将其滴入水中,可观察到剧烈反应,液面上有白雾形成,并有带刺激性气味气体逸出,该气体可使品红溶液褪色。①根据实验现象写出
 和
和 反应的化学方程式:
反应的化学方程式:②利用
 制备无水
制备无水 时,可用
时,可用 和
和 混合共热,试解释原因:
混合共热,试解释原因:
您最近一年使用:0次
名校
2 . 一氯化碘(沸点97.4℃),是一种红棕色易挥发的液体,不溶于水,易溶于乙醇和乙酸。某校研究性学习小组的同学拟利用干燥、纯净的氯气与碘反应制备一氯化碘,其装置如下:

回答下列问题:
(1)ICl中I元素化合价为___________ 。
(2)各装置连接顺序为a→_________________________ ;
如何检验A装置的气密性:_________________________________________________ 。
(3)B装置烧瓶需放在冷水中,其目的是:__________________________ ;D装置中溶质如果改用Na2CO3溶液。发生反应的离子方程式为___________________________ 。
(已知电离平衡常数:H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11;HClO:Ka=3.0×10-8)
(4)将B装置得到的液态产物进一步提纯可得到较纯净的ICl,提纯采取的操作方法是____ 。
(5)测定ICl的纯度。实验过程如下(设杂质不参与反应):
步骤1:称取4.00 g ICl与冰醋酸配成500 mL标准液。
步骤2:取上述标准液25.00 mL于锥形瓶中,加入足量KI溶液、100 mL蒸馏水,滴入几滴_________ 作指示剂(填名称),用0.1000 mol•L-1 Na2S2O3溶液滴定(I2+2Na2S2O3=2NaI+Na2S4O6),滴定到终点时消耗Na2S2O3溶液24.00 mL。
①步骤1配制标准液需要的玻璃仪器除烧杯、量筒及玻璃棒外,还需要_________ (填仪器名称)。
②ICl的纯度是_________________________________________ 。(列式并计算)

回答下列问题:
(1)ICl中I元素化合价为
(2)各装置连接顺序为a→
如何检验A装置的气密性:
(3)B装置烧瓶需放在冷水中,其目的是:
(已知电离平衡常数:H2CO3:Ka1=4.4×10-7,Ka2=4.7×10-11;HClO:Ka=3.0×10-8)
(4)将B装置得到的液态产物进一步提纯可得到较纯净的ICl,提纯采取的操作方法是
(5)测定ICl的纯度。实验过程如下(设杂质不参与反应):
步骤1:称取4.00 g ICl与冰醋酸配成500 mL标准液。
步骤2:取上述标准液25.00 mL于锥形瓶中,加入足量KI溶液、100 mL蒸馏水,滴入几滴
①步骤1配制标准液需要的玻璃仪器除烧杯、量筒及玻璃棒外,还需要
②ICl的纯度是
您最近一年使用:0次
2017-06-03更新
|
642次组卷
|
3卷引用:山东省青岛市第二中学2022-2023学年高二上学期期末考试化学试题



