1 . 常温下,下列溶液可用来除铁锈的是
A. 溶液 溶液 | B.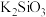 溶液 溶液 |
C. 溶液 溶液 | D. 溶液 溶液 |
您最近一年使用:0次
名校
2 . Ⅰ.铁是用途最广泛的金属,探究铁与卤素的相关性质,某化学小组查阅资料得知:无水 为黑棕色固体,无水
为黑棕色固体,无水 为灰黑色固体,二者都易溶于水,并且有强烈的吸水性,能吸收空气里的水分而潮解,加热易升华。实验小组甲设计了制备无水
为灰黑色固体,二者都易溶于水,并且有强烈的吸水性,能吸收空气里的水分而潮解,加热易升华。实验小组甲设计了制备无水 的实验,装置如图所示:
的实验,装置如图所示:___________ 。
(2)仪器F的名称为___________ ,装置F的作用___________ 。
(3)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质是___________ (填“甲”、“乙”、“丙”、“丁”)。
Ⅱ.用质量分数为98%,密度为1.84 g·cm-3的浓硫酸配制200 mL 1.84 mol·L-1的稀硫酸。
(4)配制该溶液,应取用浓硫酸的体积为___________ 。
(5)配制过程中若出现以下情况,对所配稀硫酸的浓度有什么影响?(填“偏大”“偏小”或“无影响”)
用量筒量取浓硫酸时,俯视量筒刻度线:___________ 。
 为黑棕色固体,无水
为黑棕色固体,无水 为灰黑色固体,二者都易溶于水,并且有强烈的吸水性,能吸收空气里的水分而潮解,加热易升华。实验小组甲设计了制备无水
为灰黑色固体,二者都易溶于水,并且有强烈的吸水性,能吸收空气里的水分而潮解,加热易升华。实验小组甲设计了制备无水 的实验,装置如图所示:
的实验,装置如图所示: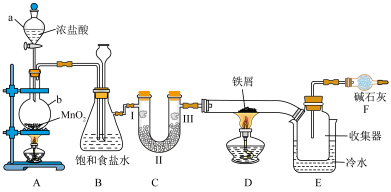
(2)仪器F的名称为
(3)装置C的作用是验证氯气是否具有漂白性,为此,实验时装置C中Ⅰ、Ⅱ、Ⅲ处依次放入的物质是
| Ⅰ | Ⅱ | Ⅲ | |
| 甲 | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
| 乙 | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
| 丙 | 干燥的有色布条 | 无水氯化钙 | 湿润的有色布条 |
| 丁 | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
Ⅱ.用质量分数为98%,密度为1.84 g·cm-3的浓硫酸配制200 mL 1.84 mol·L-1的稀硫酸。
(4)配制该溶液,应取用浓硫酸的体积为
(5)配制过程中若出现以下情况,对所配稀硫酸的浓度有什么影响?(填“偏大”“偏小”或“无影响”)
用量筒量取浓硫酸时,俯视量筒刻度线:
您最近一年使用:0次
3 . 化学与生活、生产密切相关。下列有关事实,与盐类水解无关的是
A. 溶液腐蚀铜制线路板 溶液腐蚀铜制线路板 | B.铵态氮肥和草木灰(含 )不可混合施用 )不可混合施用 |
C.工业制 溶液作除锈剂 溶液作除锈剂 | D.热的纯碱溶液去除油污 |
您最近一年使用:0次
4 . I.酸碱中和滴定是一种重要的实验方法,用 标准溶液溶液滴定未知浓度的醋酸
标准溶液溶液滴定未知浓度的醋酸
(1) 标准溶液盛放在
标准溶液盛放在_______ (填“酸或碱”)式滴定管中。
(2)该实验中选择的指示剂是_______ 。
(3)根据下列数据,请计算待测醋酸的浓度:_______  。
。
(4)量取标准液的碱式滴定管未润洗,会造成测定结果_______ (填“偏高或偏低或不变”) 。
Ⅱ.按要求填空
(5)FeCl3溶液蒸发灼烧最终得到的物质_______ (写化学式 )。
(6)泡沫灭火器原理_______ (写离子反应方程式)。
 标准溶液溶液滴定未知浓度的醋酸
标准溶液溶液滴定未知浓度的醋酸(1)
 标准溶液盛放在
标准溶液盛放在(2)该实验中选择的指示剂是
(3)根据下列数据,请计算待测醋酸的浓度:
 。
。| 滴定次数 | 待测液体积(mL) | 标准液体积(mL | |
| 滴定前读数 | 滴定后读数 | ||
| 第一次 | 20.00 | 0.60 | 20.60 |
| 第二次 | 20.00 | 2.00 | 24.10 |
| 第三次 | 20.00 | 4.00 | 24.00 |
(4)量取标准液的碱式滴定管未润洗,会造成测定结果
Ⅱ.按要求填空
(5)FeCl3溶液蒸发灼烧最终得到的物质
(6)泡沫灭火器原理
您最近一年使用:0次
5 . 下列生活中常用的方法,其原理与盐类的水解反应无关的是
| A.用草木灰去除油污 | B.焊接时用NH4Cl溶液除锈 |
| C.用白醋清洗水壶中的水垢 | D.浓的硫化钠溶液有臭味 |
您最近一年使用:0次
6 . 回答下列问题:
(1)FeCl3的水溶液呈___________ (填“酸”“中”或“碱”)性,原因是___________ (用离子方程式表示);实验室在配制FeCl3溶液时,常将FeCl3固体先溶于较浓的盐酸中,然后再用蒸馏水将其稀释到所需的浓度,以___________ (填“促进”或“抑制”)其水解。
(2)将FeCl3溶液蒸干、灼烧,最后得到的主要固体产物是___________ 。
(1)FeCl3的水溶液呈
(2)将FeCl3溶液蒸干、灼烧,最后得到的主要固体产物是
您最近一年使用:0次
2024-04-11更新
|
62次组卷
|
2卷引用:新疆维吾尔自治区皮山县高级中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
7 . 盐酸、醋酸和氨水是中学化学中常见的三种物质,某校实验小组利用浓盐酸、冰醋酸和浓氨水分别配制了浓度均为0.1mol•L-1的三种溶液各100mL并进行相关实验,据此回答下列问题:
(1)配制上述三种溶液的过程中会用到的玻璃仪器有量筒、烧杯、玻璃棒,以及___________ 。
(2)将浓度均为0.1mol•L-1的盐酸和氨水等体积混合,则
①所得混合溶液显___________ 性(填“酸性”、“碱性”或“中性”),原因是___________ (用离子方程式表示)
②所得混合溶液中所有离子的物质的量浓度由大到小的顺序为:___________ ;
③25℃时,使用pH计测得此混合溶液的pH为a,则混合溶液中c(NH )=
)=___________ mol•L-1(用含a的代数式表示,混合过程中溶液体积的微小变化忽略不计)。
(1)配制上述三种溶液的过程中会用到的玻璃仪器有量筒、烧杯、玻璃棒,以及
(2)将浓度均为0.1mol•L-1的盐酸和氨水等体积混合,则
①所得混合溶液显
②所得混合溶液中所有离子的物质的量浓度由大到小的顺序为:
③25℃时,使用pH计测得此混合溶液的pH为a,则混合溶液中c(NH
 )=
)=
您最近一年使用:0次
名校
解题方法
8 . 氯化铁是一种重要的盐,下列说法不正确的是
| A.氯化铁属于强电解质 |
| B.氯化铁溶液可腐蚀覆铜板 |
| C.氯化铁可由铁与氯气反应制得 |
D.直接加热氯化铁晶体( )可得 )可得 固体 固体 |
您最近一年使用:0次
2024-02-14更新
|
79次组卷
|
3卷引用:新疆 乌鲁木齐市实验学校2023-2024学年高二上学期1月期末化学试题
名校
9 . 下列相关条件下的离子方程式书写不正确的是
A. 溶液中通入适量氯气产生沉淀: 溶液中通入适量氯气产生沉淀: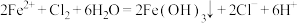 |
B.钢铁发生电化学腐蚀的负极反应: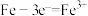 |
C.泡沫灭火器的灭火原理:Al3++3HCO =Al(OH)3↓+3CO2↑ =Al(OH)3↓+3CO2↑ |
D.氢氧酸性燃料电池的正极反应: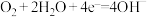 |
您最近一年使用:0次
2024-02-14更新
|
77次组卷
|
2卷引用:新疆乌鲁木齐市第101中学2023-2024学年高二上学期1月期末化学试题
名校
解题方法
10 . 化学与生产生活密切相关。下列说法错误的是
| A.用硫酸铁除去水中的悬浮物 |
| B.镀锡铁皮的镀层破损后,铁皮会加速腐蚀。 |
| C.铅蓄电池在充电时,其正极与外接电源的正极相连 |
| D.明矾可用作净水剂和消毒剂 |
您最近一年使用:0次
2024-01-10更新
|
62次组卷
|
2卷引用:新疆兵团第三师图木舒克市鸿德实验学校2023-2024学年高二上学期期末考试化学试卷



