解题方法
1 . 化学与生活、生产息息相关。下列说法正确的是
| A.铁管上镶嵌锌块,铁管不易被腐蚀 |
| B.铵态氮肥和草木灰混合施用肥效更好 |
C.医疗上常用 作X射线透视肠胃的内服剂 作X射线透视肠胃的内服剂 |
| D.盐酸的腐蚀性比醋酸大,不能用于卫生洁具的清洁 |
您最近一年使用:0次
名校
解题方法
2 . 下列离子方程式不正确的是
A.明矾的净水原理:Al3++3H2O Al(OH)3(胶体)+3H+ Al(OH)3(胶体)+3H+ |
B.泡沫灭火器的工作原理:Al3++3HCO = Al(OH)3↓+3CO2↑ = Al(OH)3↓+3CO2↑ |
C.HCO 的电离方程式:HCO 的电离方程式:HCO +H2O +H2O CO CO +H3O+ +H3O+ |
D.浓硫化钠溶液具有臭味:S2-+2H2O H2S↑+2OH- H2S↑+2OH- |
您最近一年使用:0次
名校
解题方法
3 . 化学与人类生活、生产息息相关。下列说法错误的是
| A.用纯碱溶液清洗油污,加热可增强去污力 |
| B.盛放硅酸钠溶液的试剂瓶不能用玻璃塞 |
| C.可施加适量熟石灰降低盐碱地(含较多NaCl、Na2CO3)土壤的碱性 |
| D.草木灰和铵态氮肥混合使用会降低肥效 |
您最近一年使用:0次
解题方法
4 . 工业制胆矾时,将粗制CuO粉末(含杂质FeO、Fe2O3)慢慢加入适量的稀H2SO4中完全溶解,除去杂质离子后,再蒸发结晶可得纯净的胆矾晶体。已知:pH≥9.6时,Fe2+以Fe(OH)2的形式完全沉淀;pH≥6.4时,Cu2+以Cu(OH)2的形式完全沉淀,pH接近4时,Fe3+以Fe(OH)3的形式完全沉淀。为除去溶液中的Fe2+,可先加入H2O2将Fe2+氧化为Fe3+,然后加入适量的_______,(从下面四个选项选择)调整溶液的pH使Fe3+转化为Fe(OH)3沉淀。
| A.CuO | B.Cl2 | C.Fe(OH)3 | D.H2O2 |
您最近一年使用:0次
名校
5 . 化学耗氧量COD是判断水体受污染程度的一个重要指标。测定某湖泊水样的COD并对测定后的废液进行处理的方法如下。
I.COD的测定
COD是以氧化1L水样中还原性物质所消耗的n(K2Cr2O7)为标准,并将其换算成O2的质量表示(换算关系:1molK2Cr2O7~4.8×104mgO2)。
【测定原理】
先用过量K2Cr2O7溶液氧化水体中还原性物质,再用硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定剩余的K2CrO7,(滴定反应为: +6Fe2++14H+=2Cr3++6Fe3++7H2O)
+6Fe2++14H+=2Cr3++6Fe3++7H2O)
【测定步骤】
i.将20.00mL水样和V1mL0.2500mol•L-1K2Cr2O7标准溶液混合,在Ag+催化和强酸性条件下充分反应。
ii.用0.1200mol•L-1(NH4)2Fe(SO4)2溶液滴定剩余的K2Cr2O7至终点,消耗V2mL(NH4)2Fe(SO4)2溶液。
(1)i中反应结束时,溶液颜色应为橙黄色,目的是___________ 。
(2)i中保持溶液强酸性可使平衡 +H2O⇌2
+H2O⇌2 +2H+向左移动,从而:
+2H+向左移动,从而:
①使___________ (填微粒符号)的浓度增大,其氧化性增强。
②避免生成Ag2CrO4沉淀,防止___________ 。
(3)由i、ii中数据计算:COD=___________ mg•L-1(化成最简式)。若滴定到终点后仰视读数,则使测定结果___________ (偏高、偏低或无影响)。
(4)常温下,用Na2CO3溶液浸泡BaSO4固体,也能将BaSO4转化为BaCO3,不考虑 的水解,向340mL3.0mol•L-1Na2CO3溶液中加入4.66gBaSO4,恰好完全转化为BaCO3,则Ksp(BaCO3)=
的水解,向340mL3.0mol•L-1Na2CO3溶液中加入4.66gBaSO4,恰好完全转化为BaCO3,则Ksp(BaCO3)=_______ 。[已知:Ksp(BaSO4)=1.0×10-10;溶液体积变化忽略不计]
I.COD的测定
COD是以氧化1L水样中还原性物质所消耗的n(K2Cr2O7)为标准,并将其换算成O2的质量表示(换算关系:1molK2Cr2O7~4.8×104mgO2)。
【测定原理】
先用过量K2Cr2O7溶液氧化水体中还原性物质,再用硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定剩余的K2CrO7,(滴定反应为:
 +6Fe2++14H+=2Cr3++6Fe3++7H2O)
+6Fe2++14H+=2Cr3++6Fe3++7H2O)【测定步骤】
i.将20.00mL水样和V1mL0.2500mol•L-1K2Cr2O7标准溶液混合,在Ag+催化和强酸性条件下充分反应。
ii.用0.1200mol•L-1(NH4)2Fe(SO4)2溶液滴定剩余的K2Cr2O7至终点,消耗V2mL(NH4)2Fe(SO4)2溶液。
(1)i中反应结束时,溶液颜色应为橙黄色,目的是
(2)i中保持溶液强酸性可使平衡
 +H2O⇌2
+H2O⇌2 +2H+向左移动,从而:
+2H+向左移动,从而:①使
②避免生成Ag2CrO4沉淀,防止
(3)由i、ii中数据计算:COD=
(4)常温下,用Na2CO3溶液浸泡BaSO4固体,也能将BaSO4转化为BaCO3,不考虑
 的水解,向340mL3.0mol•L-1Na2CO3溶液中加入4.66gBaSO4,恰好完全转化为BaCO3,则Ksp(BaCO3)=
的水解,向340mL3.0mol•L-1Na2CO3溶液中加入4.66gBaSO4,恰好完全转化为BaCO3,则Ksp(BaCO3)=
您最近一年使用:0次
解题方法
6 . 化学与生活、科技密切相关。下列说法正确的是
| A.盐碱地(含较多NaCl、Na2CO3),可通过施加适量熟石灰来降低土壤得碱性 |
| B.锅炉中的水垢主要成分是CaSO4,可用稀盐酸直接处理除去 |
| C.医疗上常用BaCO3作X射线透视肠胃的内服药剂,俗称“钡餐” |
| D.鲍鱼的外壳是呈棱柱状的方解石,内层是珠光层的霰石,两者成分相同,结构不同 |
您最近一年使用:0次
名校
解题方法
7 . 电子工业中,可用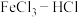 溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
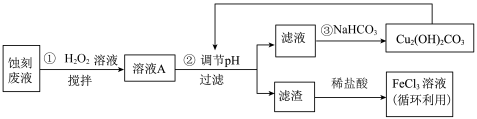
回答下列问题:
(1)把 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是___________ 。(填写化学式)
(2) 蚀刻液中加入盐酸的目的是
蚀刻液中加入盐酸的目的是___________ 。
(3)步骤①中加入 溶液的目的是(用离子方程式表示)
溶液的目的是(用离子方程式表示)___________ 。
(4)已知:生成氢氧化物沉淀的 如下表。
如下表。
根据表中数据推测调节 的范围是
的范围是___________ 。
(5)上述流程路线中,除 溶液外,还可用于循环利用的物质是
溶液外,还可用于循环利用的物质是___________ 。
(6)在 ,向浓度均为
,向浓度均为 的
的 溶液中逐滴加入氨水,若镁离子浓度为
溶液中逐滴加入氨水,若镁离子浓度为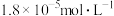 时溶液的
时溶液的 为
为___________ 。(已知 时
时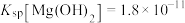 )。
)。
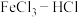 溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
溶液作为印刷电路铜板刻蚀液。某探究小组设计如下线路处理废液和资源回收:
回答下列问题:
(1)把
 溶液蒸干、灼烧,最后得到的主要固体产物是
溶液蒸干、灼烧,最后得到的主要固体产物是(2)
 蚀刻液中加入盐酸的目的是
蚀刻液中加入盐酸的目的是(3)步骤①中加入
 溶液的目的是(用离子方程式表示)
溶液的目的是(用离子方程式表示)(4)已知:生成氢氧化物沉淀的
 如下表。
如下表。| Cu(OH)2 | Fe(OH)2 | Fe(OH)3 | |
| 开始沉淀时 | 4.7 | 7.0 | 1.9 |
| 沉淀完全时 | 6.7 | 9.0 | 3.2 |
 的范围是
的范围是(5)上述流程路线中,除
 溶液外,还可用于循环利用的物质是
溶液外,还可用于循环利用的物质是(6)在
 ,向浓度均为
,向浓度均为 的
的 溶液中逐滴加入氨水,若镁离子浓度为
溶液中逐滴加入氨水,若镁离子浓度为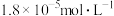 时溶液的
时溶液的 为
为 时
时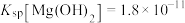 )。
)。
您最近一年使用:0次
名校
8 . 下列实验方案中,不能达到相应实验目的的是
 |  |  |  |
| A.研究温度对化学平衡的影响 | B.蒸干AlCl3溶液获得AlCl3晶体 | C.测定酸碱中和的热效应 | D.碱式滴定管排气泡 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
9 . 化学与生活、生产紧密相关。下列说法正确的是
A. 能杀灭水中的致病菌,其净水原理与明矾相同 能杀灭水中的致病菌,其净水原理与明矾相同 |
B.金属焊接时可用 溶液作除锈剂 溶液作除锈剂 |
| C.离子交换膜在现代工业中应用广泛,在氯碱工业中使用阴离子交换膜 |
| D.铁件上镀银时,铁件与电源正极相连 |
您最近一年使用:0次
2024-01-09更新
|
103次组卷
|
2卷引用:吉林省长春吉大附中实验学校2023-2024学年高二上学期11月期中化学试题
名校
解题方法
10 . 酸、碱、盐都是电解质,常温下,有7种电解质溶液:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ,已知:
,已知: 的电离常数
的电离常数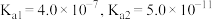 。
。
(1)用化学用语解释④呈酸性的原因:________ 。
(2) 的溶液①中由水电离出的
的溶液①中由水电离出的 为
为_______ 。
(3)浓度均为 的上述②③④三种溶液,
的上述②③④三种溶液, 由大到小为
由大到小为_______ 。
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ,已知:
,已知: 的电离常数
的电离常数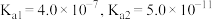 。
。(1)用化学用语解释④呈酸性的原因:
(2)
 的溶液①中由水电离出的
的溶液①中由水电离出的 为
为(3)浓度均为
 的上述②③④三种溶液,
的上述②③④三种溶液, 由大到小为
由大到小为
您最近一年使用:0次



