10-11高三·宁夏银川·阶段练习
名校
解题方法
1 . A、B、C、D是短周期元素形成的四种气体单质。E、F均为气体,且F为红棕色。有关的转化关系如下图所示(反应条件均已略去)。

请回答下列问题:
(1)D的化学式为_______________ 。
(2)反应③的离子方程式为_________________________ 。
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为_________________________ 。
(4)0.1 mol·L1的X溶液和0.1 mol·L1的Y溶液等体积混合,溶液呈________ 性(选填“酸”、“碱”或“中”);原因是____________________ (用离子方程式说明)。
(5)常温下0.1 mol·L1的Y溶液中c(H+)/c(OH―)=1×108,下列叙述正确的是_______ 。
A.该溶液的pH=11
B.该溶液中的溶质电离出的阳离子浓度为0.1 mol·L1
C.该溶液中水电离出的c(H+)与c(OH―)乘积为1×1022
D.pH=3的盐酸V1 L与该0.1 mol·L1的Y溶液V2 L混合,若混合溶液pH=7,则:V1>V2 E.将以上溶液加水稀释100倍后,pH为9 。

请回答下列问题:
(1)D的化学式为
(2)反应③的离子方程式为
(3)Y和E在一定条件下可反应生成B和Z,这是一个具有实际意义的反应,可消除E对环境的污染,该反应的化学方程式为
(4)0.1 mol·L1的X溶液和0.1 mol·L1的Y溶液等体积混合,溶液呈
(5)常温下0.1 mol·L1的Y溶液中c(H+)/c(OH―)=1×108,下列叙述正确的是
A.该溶液的pH=11
B.该溶液中的溶质电离出的阳离子浓度为0.1 mol·L1
C.该溶液中水电离出的c(H+)与c(OH―)乘积为1×1022
D.pH=3的盐酸V1 L与该0.1 mol·L1的Y溶液V2 L混合,若混合溶液pH=7,则:V1>V2 E.将以上溶液加水稀释100倍后,pH为9 。
您最近一年使用:0次
解题方法
2 . 实验室以苯、乙醛为原料,三氯化铝为催化剂来制备1,1-二苯乙烷,其反应原理为:
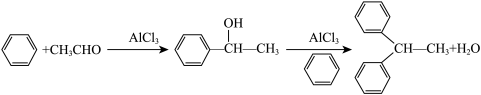
制备过程中其他产物会与AlCl3发生副反应。主要实验装置和步骤如下:

I.合成:
在250 mL三口烧瓶中加入140mL苯(密度0.88g/mL)、19gA1C13和5.5g乙醛,在20℃时充分反应。
Ⅱ.分离与提纯:
将反应混合物倒入装有150 mL,冰水和少量盐酸的烧杯中,充分搅拌,用分液漏斗分离出有机层,依次用水、2%碳酸钠溶液、水洗涤,在分离出的粗产品中加入少量无水硫酸镁固体,过滤后先常压蒸馏除去过量苯再改用减压蒸馏收集170~172℃/6.67kPa的馏分,得12.5g 1,l-二苯乙烷。
(1)仪器a的名称:_______ ;其他产物与A1C13发生副反应的化学方程式为:_________ ;装置c的作用:_________ 。
(2)连接装置b的作用是___ 。
(3)在洗涤操作中,第二次水洗的主要目的是____________________ 。实验中加入少量无水硫酸镁的目的是_______________ 。
(4)粗产品常压蒸馏提纯时,下列装置中温度计位置正确的是_____ ,可能会导致收集到的产品中混有低沸点杂质的装置是___ 。
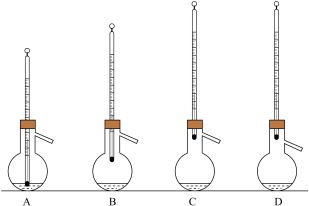
(5)本实验所得到的1,1—二苯乙烷产率约为_______ (填正确答案的序号)。

制备过程中其他产物会与AlCl3发生副反应。主要实验装置和步骤如下:

I.合成:
在250 mL三口烧瓶中加入140mL苯(密度0.88g/mL)、19gA1C13和5.5g乙醛,在20℃时充分反应。
Ⅱ.分离与提纯:
将反应混合物倒入装有150 mL,冰水和少量盐酸的烧杯中,充分搅拌,用分液漏斗分离出有机层,依次用水、2%碳酸钠溶液、水洗涤,在分离出的粗产品中加入少量无水硫酸镁固体,过滤后先常压蒸馏除去过量苯再改用减压蒸馏收集170~172℃/6.67kPa的馏分,得12.5g 1,l-二苯乙烷。
(1)仪器a的名称:
(2)连接装置b的作用是
(3)在洗涤操作中,第二次水洗的主要目的是
(4)粗产品常压蒸馏提纯时,下列装置中温度计位置正确的是

(5)本实验所得到的1,1—二苯乙烷产率约为
| A.41% | B.48% | C.55% | D.65% |
您最近一年使用:0次
2016-12-09更新
|
498次组卷
|
2卷引用:2016届宁夏石嘴山三中高三下四模理综化学试卷



