名校
1 . 工业上以软锰矿(主要成分为MnO2,另含有少量FeCO3、Al2O3、SiO2)为原料制取金属锰的工艺流程如下:

(1)“粉磨”的目的是_______ 。
(2)写出“滤渣1”的一种用途_______ 。
(3)“滤渣2”的主要成分是_______ (填化学式),“沉锰”过程_______ (填“能”或“不能”)用Na2CO3代替NH4HCO3。
(4)经检测,“浸取液”中无Fe2+,“浸取”时MnO2发生反应的离子方程式为_______ 。
(5)在“沉锰”操作中发生反应的离子方程式为_______ 。

(6)为测定“滤渣2”中铝元素的含量,设计以下方案:
①将m g滤渣2处理成a mL溶液;
②取少量①中溶液用EDTA滴定测得溶液中Fe3+、Al3+的浓度之和为b mmol/L;
③另取少量①中溶液,用盐酸羟胺将Fe3+还原为Fe2+;
④将③所得溶液利用吸光度法测得其吸光度为0.400(吸光度与Fe2+的浓度关系如下图所示)。该样品中Al元素的质量分数为_______ (用含字母的表达式表示,不必化简)。

(1)“粉磨”的目的是
(2)写出“滤渣1”的一种用途
(3)“滤渣2”的主要成分是
(4)经检测,“浸取液”中无Fe2+,“浸取”时MnO2发生反应的离子方程式为
(5)在“沉锰”操作中发生反应的离子方程式为

(6)为测定“滤渣2”中铝元素的含量,设计以下方案:
①将m g滤渣2处理成a mL溶液;
②取少量①中溶液用EDTA滴定测得溶液中Fe3+、Al3+的浓度之和为b mmol/L;
③另取少量①中溶液,用盐酸羟胺将Fe3+还原为Fe2+;
④将③所得溶液利用吸光度法测得其吸光度为0.400(吸光度与Fe2+的浓度关系如下图所示)。该样品中Al元素的质量分数为
您最近一年使用:0次
2 . 某湿法炼锌的萃余液中含有 、
、 、
、 、
、 、
、 、
、 及
及 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图所示。回答下列问题:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图所示。回答下列问题:

已知:
(1)常温下,测得某种萃余液中硫酸的浓度为 ,则此溶液中
,则此溶液中
___________  。
。
(2)在酸性条件下,加入 氧化时,
氧化时, 转化为
转化为 除去,生成
除去,生成 反应的离子方程式为
反应的离子方程式为___________ 。
(3)常温下,中和时,先调节 约为1,加入适量的
约为1,加入适量的 氧化,再调节
氧化,再调节 为4.0,“沉渣”的主要成分除
为4.0,“沉渣”的主要成分除 外还有
外还有___________ ;若加入过量 ,钴元素将会进入“沉渣”中,则水解后的溶液中
,钴元素将会进入“沉渣”中,则水解后的溶液中 约为
约为___________  。
。
(4)“沉锌”时,在近中性条件下加入 可得碱式碳酸锌[
可得碱式碳酸锌[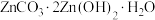 ]固体,同时产生大量气体,产生大量气体的原因是
]固体,同时产生大量气体,产生大量气体的原因是___________ 。
(5)不同质量分数的 溶液在不同温度下析出
溶液在不同温度下析出 晶体的物种如图所示。欲从含
晶体的物种如图所示。欲从含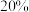
 及微量杂质的“沉锌后液”中直接析出无水
及微量杂质的“沉锌后液”中直接析出无水 ,“操作a”为
,“操作a”为___________ 。

 、
、 、
、 、
、 、
、 、
、 及
及 等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图所示。回答下列问题:
等,逐级回收有价值金属并制取活性氧化锌的工艺流程如图所示。回答下列问题:
已知:
| 沉淀物 |  |  |  |  |  |
 | 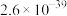 |  | 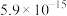 |  | 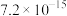 |
(1)常温下,测得某种萃余液中硫酸的浓度为
 ,则此溶液中
,则此溶液中
 。
。(2)在酸性条件下,加入
 氧化时,
氧化时, 转化为
转化为 除去,生成
除去,生成 反应的离子方程式为
反应的离子方程式为(3)常温下,中和时,先调节
 约为1,加入适量的
约为1,加入适量的 氧化,再调节
氧化,再调节 为4.0,“沉渣”的主要成分除
为4.0,“沉渣”的主要成分除 外还有
外还有 ,钴元素将会进入“沉渣”中,则水解后的溶液中
,钴元素将会进入“沉渣”中,则水解后的溶液中 约为
约为 。
。(4)“沉锌”时,在近中性条件下加入
 可得碱式碳酸锌[
可得碱式碳酸锌[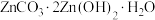 ]固体,同时产生大量气体,产生大量气体的原因是
]固体,同时产生大量气体,产生大量气体的原因是(5)不同质量分数的
 溶液在不同温度下析出
溶液在不同温度下析出 晶体的物种如图所示。欲从含
晶体的物种如图所示。欲从含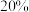
 及微量杂质的“沉锌后液”中直接析出无水
及微量杂质的“沉锌后液”中直接析出无水 ,“操作a”为
,“操作a”为
您最近一年使用:0次
18-19高二下·四川成都·开学考试
3 . Ⅰ.(1) 硫酸铜晶体的溶解度虽大,但溶解过程较慢,实验室常用热水配制以加快溶解速率,但常常会产生浑浊,请用文字简要说明原因___________________ , 用热水配制出澄清的较浓的 CuSO4 溶液时应再加入少量____________________ 。
(2) 稀 Na2S 溶液有一种腐卵气味,加入 AlCl3 溶液后,腐卵气味加剧,用离子方程式表 示气味加剧过程所发生的化学反应__________________ 。
(3) 下列物质水溶液经加热浓缩、蒸干灼烧后能得到原溶质物质的是_____
①NH4 HCO3;②CaCl2;③AlCl3;④Cu(NO3)2;⑤FeCl2;⑥K2SO3;⑦KMnO4;⑧ KAl(SO4)2
(Ⅱ)依据氧化还原反应:MnO4- + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4H2O,欲采用滴定的方法测定 FeSO4 的质量分数,实验步骤如下:
① 称量绿矾样品,配成 100 mL 待测溶液,② 取一定体积待测液置于锥形瓶中,并加入一定量的硫酸,③ 将标准浓度的 KMnO4 溶液装入滴定管中,调节液面至 a mL 处,④ 滴定待测液至滴定终点时,滴定管的液面读数 b mL,⑤重复滴定 2~3 次。
(1) 如何确定滴定到达终点?现象是_____________
(2) 下列操作会导致测定结果偏低的是_____
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(3)下列每种量器的数量不限,在上述实验中,必须 使用的有_____
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管
(2) 稀 Na2S 溶液有一种腐卵气味,加入 AlCl3 溶液后,腐卵气味加剧,用离子方程式表 示气味加剧过程所发生的化学反应
(3) 下列物质水溶液经加热浓缩、蒸干灼烧后能得到原溶质物质的是
①NH4 HCO3;②CaCl2;③AlCl3;④Cu(NO3)2;⑤FeCl2;⑥K2SO3;⑦KMnO4;⑧ KAl(SO4)2
(Ⅱ)依据氧化还原反应:MnO4- + 5Fe2+ + 8H+ = Mn2+ + 5Fe3+ + 4H2O,欲采用滴定的方法测定 FeSO4 的质量分数,实验步骤如下:
① 称量绿矾样品,配成 100 mL 待测溶液,② 取一定体积待测液置于锥形瓶中,并加入一定量的硫酸,③ 将标准浓度的 KMnO4 溶液装入滴定管中,调节液面至 a mL 处,④ 滴定待测液至滴定终点时,滴定管的液面读数 b mL,⑤重复滴定 2~3 次。
(1) 如何确定滴定到达终点?现象是
(2) 下列操作会导致测定结果偏低的是
A.盛标准溶液的滴定管用蒸馏水洗涤后未用标准液润洗就装液滴定
B.锥形瓶用蒸馏水洗涤后未用待测液润洗
C.读取标准液读数时,滴定前平视,滴定到终点后俯视
D.滴定前滴定管尖嘴处有气泡未排除,滴定后气泡消失
(3)下列每种量器的数量不限,在上述实验中,
A.托盘天平 B.量筒 C.碱式滴定管 D.酸式滴定管
您最近一年使用:0次



