解题方法
1 . 下列实验操作规范且能达到目的的是
实验目的 | 实验操作 | |
A | 证明: | 向 溶液中滴加几滴 溶液中滴加几滴 的 的 溶液,再滴加几滴 溶液,再滴加几滴 溶液 溶液 |
B | 证明非金属性: | 分别用玻璃棒蘸取 与 与 溶液,点在湿润的 溶液,点在湿润的 试纸上 试纸上 |
C | 配制 溶液 溶液 | 将 固体溶于适量浓盐酸中,再加水稀释至所需浓度 固体溶于适量浓盐酸中,再加水稀释至所需浓度 |
D | 探究浓度对化学反应速率的影响 | 常温下,用相同大小的铁片分别与浓硫酸、稀硫酸反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 下图所示的实验,能达到实验目的的是
| A | B | C | D |
 |  |  片刻后在 Fe 电极附近滴入铁氰化钾溶液 |  |
| 验证化学能转化为电能 | 证明温度对平衡移动的影响 | 验证 Fe 电极被保护 | 验证AgCl 溶解度大于Ag2S |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
3 . 完成下列实验目的所采取的实验方法和对应原理都正确的是
| 选项 | 目的 | 实验方法 | 原理 |
| A | 除去蛋白质溶液中混有的(NH4)2SO4 | 将混合物倒入过滤器中过滤 | 胶体不能透过滤纸 |
| B | 提取溴水中 的溴单质 | 用乙醇萃取 | 溴在乙醇中的溶解度较大 |
| C | 检验FeSO4溶液是否在空气中氧化变质 | 向盛有FeSO4溶液的试管中滴入KSCN溶液,观察溶液是否变红色 | Fe3+和SCN-反应生成Fe(SCN)3,溶液显红色 |
| D | 证明:Ksp[ Fe(OH)3]< Ksp[ Mg(OH)2] | 向盛有2 mL浓度均为0.1 mol/L的FeCl3和MgCl2的混合溶液的试管中滴加1 mol/L NaOH溶液,观察到析出红褐色沉淀 | Ksp越小的物质越容易沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
4 . 实验:①向盛有1mL0.1 mol/LMgCl2溶液试管中加2 mL 0.2 mol/L NaOH溶液,得到浊液a,过滤得到滤液b和白色沉淀c。
②向沉淀c中滴加0.1mol/LFeCl3溶液,沉淀变为红褐色。
③ 向浊液a中滴加0.1mol/LFeCl3溶液,沉淀变为红褐色。
下列分析不正确 的是
②向沉淀c中滴加0.1mol/LFeCl3溶液,沉淀变为红褐色。
③ 向浊液a中滴加0.1mol/LFeCl3溶液,沉淀变为红褐色。
下列分析
| A.浊液a中存在沉淀溶解平衡:Mg (OH)2(s)→Mg2+(aq)+2OH-(aq) |
| B.滤液b中含有Mg2+ |
| C.③实验中颜色变化说明Mg (OH)2转化为Fe(OH)3 |
| D.②实验可以证明Fe(OH)3比Mg (OH)2更难溶 |
您最近一年使用:0次
5 . 钡(Ba)和锶(Sr)及其化合物在工业上有着广泛的应用,它们在地壳中常以硫酸盐的形式存在,BaSO4和SrSO4都是难溶性盐。工业上提取钡和锶时首先将BaSO4和SrSO4转化成难溶弱酸盐。
已知:SrSO4(s) Sr2+(aq)+SO
Sr2+(aq)+SO (aq)Ksp=2.5×10-7
(aq)Ksp=2.5×10-7
SrCO3(s) Sr2+(aq)+CO
Sr2+(aq)+CO (aq)Ksp=2.5×10-9
(aq)Ksp=2.5×10-9
(1)将SrSO4转化成SrCO3的离子方程式为__ ;该反应的平衡常数表达式为__ 。
(2)对于上述反应,实验证明增大CO 的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”)。
的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”)。
①升高温度,平衡常数K将__ 。
②增大CO 的浓度,平衡常数K将
的浓度,平衡常数K将__ 。
已知:SrSO4(s)
 Sr2+(aq)+SO
Sr2+(aq)+SO (aq)Ksp=2.5×10-7
(aq)Ksp=2.5×10-7SrCO3(s)
 Sr2+(aq)+CO
Sr2+(aq)+CO (aq)Ksp=2.5×10-9
(aq)Ksp=2.5×10-9(1)将SrSO4转化成SrCO3的离子方程式为
(2)对于上述反应,实验证明增大CO
 的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”)。
的浓度或降低温度都有利于提高SrSO4的转化率。判断在下列两种情况下,平衡常数K的变化情况(填“增大”“减小”或“不变”)。①升高温度,平衡常数K将
②增大CO
 的浓度,平衡常数K将
的浓度,平衡常数K将
您最近一年使用:0次
名校
解题方法
6 . 下列实验中,能达到相应实验目的的是
| A | B | C | D |
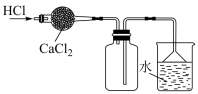 | 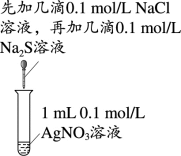 | 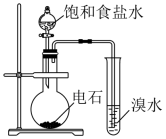 | 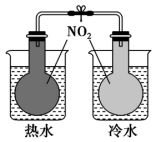 |
| 收集HCl | 证明氯化银溶解度大于硫化银 | 证明乙炔可使溴水褪色 | 验证温度对平衡移动的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-10-23更新
|
265次组卷
|
4卷引用:上海市复旦大学附属中学2021届高三上学期第一次教学质量检测化学试题
上海市复旦大学附属中学2021届高三上学期第一次教学质量检测化学试题(已下线)专题3.4.2 沉淀溶解平衡的应用(备作业)-【上好课】2021-2022学年高二化学同步备课系列(人教版2019选择性必修1)上海行知中学2022-2023学年高三上学期第一次月考化学试题上海市控江中学2022-2023学年高三上学期期中考试化学试题
7 . 下列实验中,能达到相应实验目的的是
 |  | 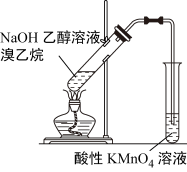 | 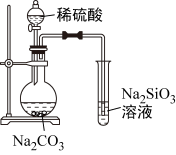 |
| A.证明乙炔可使溴水褪色 | B.证明氯化银溶解度大于硫化银 | C.验证溴乙烷的消去产物是乙烯 | D.推断S、C、Si的非金属性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
8 . 下列实验能达到预期目的的是
| 实验内容 | 实验目的 | |
| A | 将石蜡油(液态石蜡)分解的产物通入溴的四氯化碳溶液中,溶液逐渐褪色 | 分解产物中一定含有乙烯 |
| B | 向1mL0.2mol/LNaOH溶液中滴入2滴0.1mol/LMgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下,Ksp[Mg(OH)2]>Ksp[Fe(OH)3] |
| C | 测定同温度下相同浓度的碳酸钠和硫酸钠溶液的pH,前者大于后者 | 证明碳元素非金属性弱于硫 |
| D | 向某溶液中滴加少量稀NaOH溶液,将湿润的红色石蕊试纸置于试管口试纸不变蓝 | 证明溶液中无NH |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-12-16更新
|
141次组卷
|
2卷引用:四川省眉山市洪雅中学2021届高三12月月考理综化学试题
名校
9 . 下列实验操作现象及解释或结论均正确的是
| 选项 | 实验操作及现象 | 解释或结论 |
| A | 常温下,相同体积相同浓度的盐酸、醋酸与大小相同的镁片反应,产生气泡的速率:前者快 | 得出结论:盐酸是强电解质,醋酸是弱电解质 |
| B | 常温下,向浓度、体积都相同的Na2CO3和NaHCO3溶液中各滴加1滴酚酞,变红,前者红色更深 红色更深 | 结合质子的能力:CO >HCO >HCO |
| C | 向FeCl3和KSCN混合溶液中,加入少量KCl的固体,溶液颜色变浅 | FeCl3+3KSCN Fe(SCN)3+3KCl平衡向逆反应方向移动 Fe(SCN)3+3KCl平衡向逆反应方向移动 |
| D | 将0.1mol/L的AgNO3加入到0.1mol/L的NaCl溶液中至不再产生白色沉淀,再向悬浊液中加入0.1mol/L的KI溶液,有黄色沉淀产生 | 证明:Ksp(AgCl)>Ksp(AgI) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
10 . 下述实验方案能达到实验目的的是
A.验证铁钉发生吸氧腐蚀 |
B.证明Fe电极被保护 |
C.测定中和热 |
D.溶解度:Mg(OH)2>Fe(OH)3 |
您最近一年使用:0次



