名校
解题方法
1 . 下列实验操作能达到实验目的的是
| 目的 | 操作 | |
| A | 测定NaClO溶液的pH | 取一张pH试纸放在表面皿上,用洁净的玻璃棒蘸取待测液点滴于试纸的中部,与标准比色卡对比 |
| B | 验证Ksp(AgCl)>Ksp( AgI) | 取2 mL0. 1mol·L-1AgNO3溶液,先后滴加3滴0.1mol·L-1NaCl溶液和5滴0.1mol·L-1KI溶液,先生成白色沉淀,后又产生黄色沉淀 |
| C | 证明Na2CO3溶液中存在水解平衡 | 向含有酚酞的Na2CO3溶液中滴入BaCl2溶液,观察溶液的变化 |
| D | 检验Fe(NO3)2晶体是否已 氧化变质 | 将Fe(NO3)2样品溶于稀盐酸后,滴加KSCN溶液,观察溶液是否变红 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-11-24更新
|
624次组卷
|
8卷引用:山东省聊城市2020-2021学年高二上学期期中考试化学试题
2 . 为研究沉淀的生成及其转化,某小组进行如下实验。关于该实验分析不正确 的是( )
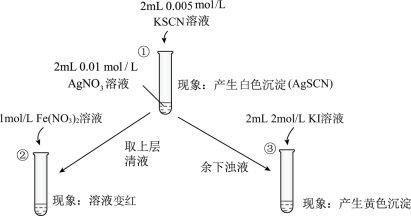

A.①浊液中存在平衡:AgSCN(s)  Ag+(aq)+SCN-(aq) Ag+(aq)+SCN-(aq) |
| B.②中颜色变化说明上层清液中含有SCN- |
| C.③中颜色变化说明有AgI生成 |
| D.该实验可以证明AgI比AgSCN更难溶 |
您最近一年使用:0次
2020-03-21更新
|
1353次组卷
|
32卷引用:内蒙古通辽实验中学2018-2019学年高二上学期期中考试化学试题
内蒙古通辽实验中学2018-2019学年高二上学期期中考试化学试题2017届北京市西城区普通中学高三上学期期中化学试卷北京市第101中学2017-2018学年高二下学期期末考试化学试题人教版高二化学选修4 第三章 第四节 难溶电解质的溶解平衡练习题【全国百强校】广东省深圳外国语学校2017-2018学年高二上学期期中化学试题(已下线)考点14 化学基本理论——《备战2020年高考精选考点专项突破题集》云南省玉溪第一中学2019-2020学年高二上学期第二次月考化学试题上海市十二校2016届高三3月联考化学试题北京清华附中2019—2020学年第二学期高二年级居家自主学习在线检测化学试卷北京清华附中2019-2020学年度第二学期高三化学统考试卷四川省成都市第七中学2021届高三上学期入学考试化学试题鲁科版(2019)选择性必修1 第3章 物质在水溶液中的行为 第3节 沉淀溶解平衡福建省福州第三中学2019-2020学年高二上学期期末考试化学试题人教版(2019)高二选择性必修第一册 第三章 水溶液中的离子反应与平衡 第四节 沉淀溶解平衡 教材帮河南省焦作市博爱县英才学校2020-2021学年高二上学期11月月考化学试题吉林省长春市实验中学2020-2021学年高二上学期期中考试化学试题山西省山西大学附属中学、汾阳中学2020-2021学年高二上学期12月月考化学试题吉林省长春市十一高中2020-2021学年高二上学期第三学程考试化学试题江西省赣县第三中学2020-2021学年高二上学期12月月考化学试题甘肃省静宁县第一中学2021-2022学年高二上学期第一次月考(实验班)化学试题(已下线)第10练 沉淀溶解平衡-2022年【寒假分层作业】高二化学(人教版2019选择性必修1)河南省开封市五县2021-2022学年高二上学期期末考试化学试题(已下线)第24讲 沉淀溶解平衡(练)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)易错点26 沉淀溶解平衡-备战2023年高考化学考试易错题(已下线)第八章 水溶液中的离子反应与平衡 第52讲 难溶电解质的溶解平衡黑龙江省哈尔滨市第三中学校2022-2023学年高二上学期期末考试化学试题作业(二十一) 沉淀溶解平衡的应用第2课时 沉淀的溶解与生成、转化及应用(已下线)第5讲 难溶电解质的溶解平衡北京市第五十中学2022-2023学年高二上学期期中考试化学试题北京市第二十中学2021-2022学年高二上学期期中考试化学试卷黑龙江省哈尔滨市第四中学校2023-2024学年高二上学期11月月考化学试题
3 . 下列实验能达到预期目的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 取两支试管,分别加入4mL 0.01mol/L KMnO4酸性溶液,然后向一支试管中加入0.1mol/L H2C2O4溶液2mL,向另一支试管中加入0.1mol/L H2C2O4溶液4mL,记录褪色时间 | 证明草酸浓度越大,反应速率越快 |
| B | 向含有酚酞的Na2CO3溶液中加入少量BaCl2固体,溶液红色变浅 | 证明Na2CO3溶液中存在水解平衡 |
| C | 向10mL 0.2mol/L NaOH溶液中滴入2滴0.1mol/L MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol/LFeCl3溶液,又生成红褐色沉淀 | 证明在相同温度下的Ksp:Mg(OH)2>Fe(OH)3 |
| D | 室温下,用pH试纸测定浓度为0.1mol·L-1NaClO溶液和0.1mol·L-1CH3COONa溶液的pH | 比较HClO和CH3COOH的酸性强弱 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2019-12-23更新
|
131次组卷
|
2卷引用:内蒙古呼和浩特市第十六中学2020-2021学年高二上学期期中考试化学试题
18-19高二下·内蒙古·阶段练习
名校
4 . 下列实验能达到相应实验目的的是( )
| 选项 | 实验内容 | 实验目的 |
| A | 向一定量AgNO3溶液中,先滴加几滴KCl溶液,再滴加几滴KI溶液,先出现白色沉淀,后出现黄色沉淀 | 比较Ksp(AgCl)和Ksp(AgI)的大小 |
| B | 用pH计测定NaClO溶液和CH3COONa溶液的pH可知,pH (NaClO) >pH(CH3COONa) | 比较HClO和CH3COOH酸性强弱 |
| C | 用铁作阴极、石墨作阳极电解煮沸过的NaOH溶液(液面上覆盖一层苯) | 制取纯净的Fe(OH)2 |
| D | 常温下,等体积、pH均为2的HA和HB两种酸分别与足量Zn反应,HA放出的H2多 | 证明HA是弱酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
5 . 实验是化学学习中非常重要的内容,根据下面两个实验回答问题。
(一)某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
(查阅资料)25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
(实验探究)向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀。
(1)分别向两支试管中加入不同试剂,记录实验现象如表:(表中填空填下列选项中字母代号)
A.白色沉淀转化为红褐色沉淀 B.白色沉淀不发生改变
C.红褐色沉淀转化为白色沉淀 D.白色沉淀溶解,得无色溶液
(2)同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。
猜想2:____________________________________________________________ 。
(3)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明猜想正确的是____ (填 “1”或“2”)。
(二)测定某品牌的碘盐(含有碘酸钾)中碘元素的百分含量。准确称取5.000 0 g该碘盐,溶于蒸馏水,然后与足量的KI溶液在酸性条件下混合(发生的反应为KIO3+3H2SO4+5KI===3K2SO4+3I2+3H2O),充分反应后将混合溶液稀释至250 mL,然后取25.00 mL用5.0×10-4 mol·L-1的Na2S2O3标准溶液进行滴定(用淀粉作指示剂,反应为I2+2S2O32-===2I-+S4O62-)。有关实验数值如下表所示。
该碘盐中碘元素的百分含量为________ 。(保留三位有效数字)下列操作中,会导致所测得的碘元素的百分含量偏大的是________ 。
a.滴定终点时,俯视刻度
b.没有用Na2S2O3标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水
(一)某研究小组进行Mg(OH)2沉淀溶解和生成的实验探究。
(查阅资料)25℃时,Ksp[Mg(OH)2]=1.8×10-11,Ksp[Fe(OH)3]=4.0×10-38
(实验探究)向2支均盛有1mL0.1mol/LMgCl2溶液的试管中分别加入2滴2mol/L NaOH溶液,制得等量Mg(OH)2沉淀。
(1)分别向两支试管中加入不同试剂,记录实验现象如表:(表中填空填下列选项中字母代号)
| 试管编号 | 加入试剂 | 实验现象 |
| Ⅰ | 2滴0.1mol/LFeCl3溶液 | ① |
| Ⅱ | 4mL2mol/LNH4Cl溶液 | ② |
A.白色沉淀转化为红褐色沉淀 B.白色沉淀不发生改变
C.红褐色沉淀转化为白色沉淀 D.白色沉淀溶解,得无色溶液
(2)同学们猜想实验Ⅱ中沉淀溶解的主要原因有两种:
猜想1:NH4+结合Mg(OH)2电离出的OH-,使Mg(OH)2的溶解平衡正向移动。
猜想2:
(3)为验证猜想,同学们取少量相同质量的氢氧化镁盛放在两支试管中,一支试管中加入醋酸铵溶液(pH=7),另一支试管中加入NH4Cl和氨水混合液(pH=8),两者沉淀均溶解。该实验证明猜想正确的是
(二)测定某品牌的碘盐(含有碘酸钾)中碘元素的百分含量。准确称取5.000 0 g该碘盐,溶于蒸馏水,然后与足量的KI溶液在酸性条件下混合(发生的反应为KIO3+3H2SO4+5KI===3K2SO4+3I2+3H2O),充分反应后将混合溶液稀释至250 mL,然后取25.00 mL用5.0×10-4 mol·L-1的Na2S2O3标准溶液进行滴定(用淀粉作指示剂,反应为I2+2S2O32-===2I-+S4O62-)。有关实验数值如下表所示。
| 滴定次数 | 待测液的体积(mL) | 滴定前的读数(mL) | 滴定后的读数(mL) |
| 第一次 | 25.00 | 0.00 | 15.90 |
| 第二次 | 25.00 | 0.00 | 14.99 |
| 第三次 | 25.00 | 0.00 | 15.01 |
该碘盐中碘元素的百分含量为
a.滴定终点时,俯视刻度
b.没有用Na2S2O3标准溶液润洗相应的滴定管
c.锥形瓶中有少量的蒸馏水
您最近一年使用:0次
2018-11-12更新
|
333次组卷
|
2卷引用:内蒙古通辽实验中学2018-2019学年高二上学期期中考试化学试题
名校
6 . 下列实验操作规范且能达到目的的是
| 目的 | 操作 | |
| A. | 取20.00 mL盐酸 | 在50 mL酸式滴定管中装入盐酸,调整初始读数为30.00 mL后,将剩余盐酸放入锥形瓶 |
| B. | 除去锅炉中沉积的CaSO4 | 可用Na2CO3溶液浸泡后,再将不溶物用酸溶解去除 |
| C. | 测定醋酸钠溶液pH | 用玻璃棒蘸取溶液,点在湿润的pH试纸上 |
| D. | 证明Ksp(ZnS) > Ksp(CuS) | 在0.1mol/LNa2S溶液中滴加少量等浓度的ZnSO4溶液,再加入少量等浓度的CuSO4溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-11-07更新
|
776次组卷
|
8卷引用:内蒙古通辽实验中学2018-2019学年高二上学期期中考试化学试题
内蒙古通辽实验中学2018-2019学年高二上学期期中考试化学试题2020届高三化学二轮冲刺新题专练——仪器的连接和实验的操作正误判断2020届高三化学化学二轮复习——常考题型:浓度积及浓度积常数【精编24题】夯基提能2020届高三化学选择题对题专练——选修4化学反应原理——酸碱中和滴定(基础过关)河北省石家庄市辛集市第一中学2019-2020学年高二第二次考试(二)化学试题福建省莆田第一中学2020-2021学年高二上学期期末考试化学试题湖南常德淮阳中学2021-2022学年高二上学期期中考试化学试题广东省梅州市三校(蕉岭中学、虎山中学、平远中学)2021-2022学年高二上学期(11月)联考化学试题
名校
7 . 下列实验方案能达到实验目的的是
实验目的 | 实验方案 | |
| A | 证明Mg(OH)2 沉淀可以转化为Fe(OH)3 | 向2mL1mol/LNaOH溶液中先加入3滴1mol/L MgCl2溶液,再加入3滴1mol/LFeCl3 |
| B | 比较氯和碳的非金属性强弱 | 将盐酸滴入碳酸氢钠溶液中 |
| C | 配制100mL1.0mol/LCuSO4溶液 | 将25gCuSO4·5H2O溶于100mL蒸馏水中 |
| D | 验证氧化性:Fe3+>I2 | 将KI和FeCl3溶液在试管中混合后,加入CCl4,振荡,静置,观察下层液体是否变成紫色 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2018-01-18更新
|
296次组卷
|
8卷引用:内蒙古自治区乌拉特前旗一中2019届高三上学期第一次月考化学试题
名校
解题方法
8 . 下列实验方案中,不能达到实验目的是
| 选项 | 实验目的 | 实验方案 |
| A | 证明氧化性:H2O2比Fe3+强 | 用硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中,溶液变黄色 |
| B | 鉴别溴蒸气和NO2 | 分别通入硝酸银溶液中,产生淡黄色沉淀的是溴蒸汽 |
| C | 证明盐类水解是吸热反应 | 在醋酸钠溶液中滴入酚酞试液,加热后红色加深 |
| D | 证明难溶物存在沉淀溶解平衡 | 往黄色固体难溶物PbI2加水中振荡,静置取上层清液加入NaI固体产生黄色沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2016-12-09更新
|
414次组卷
|
13卷引用:2015届内蒙古赤峰市宁城县高三第三次模拟考试化学试卷
2015届内蒙古赤峰市宁城县高三第三次模拟考试化学试卷2014-2015福建省厦门市高三上学期期末质量检查化学试卷2017届陕西省宝鸡中学高三月考二化学试卷2017届湖南省衡阳市第八中学高三实验班第六次月考理综化学试卷山东省济南外国语学校2018届高三12月考试化学试题【全国百强校】福建省厦门外国语学校2019届高三上学期第一次月考化学试题会做实验2020届高三化学实验复习——物质(离子)的检验【选择突破33题】天津市实验中学2020届高三下学期4月第一次测试化学试题(已下线)2020年高考化学押题预测卷02(新课标Ⅱ卷)--《2020年高考押题预测卷》(已下线)考点32 化学实验方案设计与评价-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点35 化学实验方案的设计与评价-备战2022年高考化学一轮复习考点帮(浙江专用)河南省鹤壁高中2021-2022学年高三上学期一轮复习第二次质量检测化学试题(已下线)考点53 化学实验方案设计与评价-备战2023年高考化学一轮复习考点帮(全国通用)
名校
解题方法
9 . 25℃时,下列4种盐的溶度积常数(Ksp)分别是:
结合相关数据分析,下列说法错误的是
| Ag2SO4(白色) | Ag2S(黑色) | FeS(黑色) | MnS(肉色) |
| 1.4×10-5mol3·L-3 | 6.3×10-50mol3·L-3 | 3.3×10-18mol2·L-2 | 2.5×10-13mol2·L-2 |
| A.除去某溶液中的Ag+用Na2S溶液比Na2SO4溶液效果好 |
| B.25℃时,MnS的溶解度大于FeS的溶解度 |
| C.向少量FeS悬浊液中加入足量饱和MnCl2溶液,沉淀颜色会由黑色变为肉色 |
| D.向Ag2S(s)⇌2Ag+(aq)+S2-(aq)平衡体系中加入少量Na2S固体,溶液中c(Ag+)不变 |
您最近一年使用:0次
2020-07-31更新
|
791次组卷
|
6卷引用:内蒙古通辽市开鲁县第一中学2021届高三上学期第二次阶段性考试化学试题
内蒙古通辽市开鲁县第一中学2021届高三上学期第二次阶段性考试化学试题山东省烟台市2019-2020学年高二下学期期末考试化学试题(已下线)第03章 水溶液中的离子平衡(A卷基础篇)——2020-2021学年高二化学选修四同步单元AB卷(人教版)(已下线)3.4.1 难溶电解质的沉淀溶解平衡(练习)-2020-2021学年上学期高二化学同步精品课堂(新教材人教版选择性必修1)河南省济源市第五中学2020-2021学年高二下学期期末考试化学试题(已下线)易错点26 沉淀溶解平衡-备战2023年高考化学考试易错题
10 . 常温下,将0.025molBaSO4粉末置于盛有蒸馏水的烧杯中形成1L 悬浊液,然后向烧杯中加入Na2CO3固体(忽略溶液体积的变化)并充分搅拌。加入Na2CO3固体的过程中溶液中几种离子的浓度变化曲线如图所示,下列说法中正确的是


| A.常温下,Ksp(BaSO4)=2.5×10-9 |
| B.BaSO4在水中的溶解度、Ksp均比在BaCl2溶液中的大 |
| C.若要使BaSO4全部转化为BaCO3至少要加入0.65mol Na2CO3 |
D.BaSO4恰好全部转化为BaCO3时,溶液中离子浓度大小关系为:c( )>c( )>c( )>c(Ba2+)>c(OH-) )>c(Ba2+)>c(OH-) |
您最近一年使用:0次
2020-06-23更新
|
1077次组卷
|
3卷引用:内蒙古包头市2020届高三普通高等学校招生全国统一考试(第二次模拟考试)理科综合化学试题
内蒙古包头市2020届高三普通高等学校招生全国统一考试(第二次模拟考试)理科综合化学试题内蒙古赤峰二中2020-2021学年高二上学期第二次月考化学试题(已下线)专题八 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)



