18. CO、H
2可以合成很多有机物,简称C1化学。工业上,利用水煤气法造气(CO和H
2),其中发生了反应:CO(g)+H
2O(g)

CO
2(g)+H
2(g)
△H。回答下列问题:
(1)已知:CO、H
2的燃烧热(
△H)分别为-283.0kJ·mol
-1、-285.8kJ·mol
-1;H
2O(g)=H
2O(l)
△H=-44.0kJ·mol
-1。则上述反应中
△H=
___kJ·mol
-1。
(2)830℃时,在体积为2L的恒容密闭容器中,充入2molCO(g)和2molH
2O(g)。从反应开始经过5min达到平衡。H
2的平均生成速率为0.1mol·L
-1·min
-1,平衡时H
2的物质的量为n
1mol。其他条件不变,平衡时再充入2molCO(g)和2molH
2O(g),达到新平衡时H
2的物质的量为n
2mol。
①
 ___
___(填“>”“<”或“=”)

。
②下列情况能说明上述反应达到平衡状态的是
___(填标号)。
A.混合气体总压强保持不变
B.CO和CO
2的消耗速率相等
C.混合气体平均摩尔质量保持不变
D.混合气体密度保持不变
③上述反应的速率表达式:v
正=k
正·c(CO)·c(H
2O),v
逆=k
逆·c(CO
2)·c(H
2)(k
正、k
逆为化学反应速率常数,只与温度有关,与浓度、压强无关)。

=
___。若达到平衡后,将温度由830℃调到850℃,则k
正增大的倍数
___(填“大于”“小于”或“等于”)k
逆增大的倍数。
(3)在恒容密闭容器中加入适量催化剂,充入一定量H
2和CO合成甲醇:2H
2(g)+CO(g)

CH
3OH(g)。测得相同时间内CH
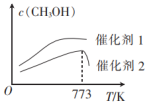
3OH(g)的浓度与温度、催化剂的关系如图所示。催化剂
___(填“1”或“2”)对该反应的活化能降低程度较大;对于催化剂2,温度高于773K时,CH
3OH浓度突减的主要原因可能是
___。
(4)CO和H
2的混合气体与空气构成碱性(KOH为电解质)燃料电池。若CO和H
2体积比为3:1,碳元素仅转化成KHCO
3,则负极的总电极反应式为
___。