名校
解题方法
1 . 下列解释事实的离子方程式不正确 的是
A.电解精炼铜的阴极反应: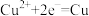 |
| B.钢铁腐蚀发生的反应:Fe−2e- = Fe2+ |
C.铜在潮湿空气中被腐蚀: |
D.草酸使酸性KMnO4溶液褪色:5 + 2 + 2 + 16H+ = 2Mn2+ + 10CO2↑+ 8H2O + 16H+ = 2Mn2+ + 10CO2↑+ 8H2O |
您最近一年使用:0次
名校
解题方法
2 . 某小组进行电化学研究, 甲同学设计如图的原电池装置,乙同学利用甲设计的装置及提供的药品与材料,不能完成的实验是
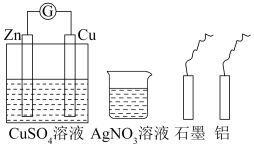

| A.在石墨电极上镀锌 | B.设计一个新的原电池 |
| C.使甲同学的正极变为负极 | D.使锌电极受到保护 |
您最近一年使用:0次
3 . 下列属于放热反应的是
| A.灼热的碳与二氧化碳的反应 | B.铁丝缓慢氧化生锈 |
| C.石灰石在高温下分解 | D. 晶体与NH4Cl晶体反应 晶体与NH4Cl晶体反应 |
您最近一年使用:0次
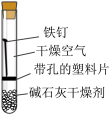
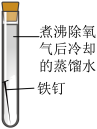
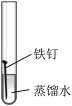
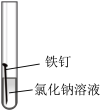
4 . 某小组同学对不同条件下铁钉的锈蚀进行了实验。
(1)一周后观察,铁钉被腐蚀程度最大的是___________ (填实验序号)。
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。___________ (填字母,下同)。
a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
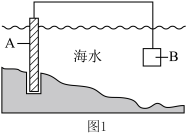
(3)电化学原理在保护海水中钢闸门中有广泛应用。______ 。
a.牺牲阳极法 b.外加电流法
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择______ 。
a.碳棒 b.锌板 c.铜板
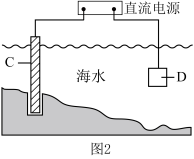
③图2中,钢闸门C应连接直流电源的___________ (填“正”或“负”)极。
| 序号 | ① | ② | ③ | ④ |
| 实验 |
|
|
|
|
(1)一周后观察,铁钉被腐蚀程度最大的是
(2)实验小组将实验④中氯化钠溶液分别替换为pH=2和pH=4的盐酸溶液。在密闭容器中,分别用压强传感器记录实验过程中的压强变化,如图所示。

a.两容器中负极反应均为Fe-2e⁻=Fe2+
b.曲线a记录的是pH=2的盐酸中压强的变化
c.在弱酸性溶液中,铁钉能发生吸氧腐蚀
d.曲线b记录的容器中正极反应是O2+4e⁻+2H2O=4OH⁻
(3)电化学原理在保护海水中钢闸门中有广泛应用。
a.牺牲阳极法 b.外加电流法
②为了减缓海水对钢闸门A的腐蚀,图1中材料B可以选择
a.碳棒 b.锌板 c.铜板
③图2中,钢闸门C应连接直流电源的
您最近一年使用:0次
2023-12-25更新
|
163次组卷
|
2卷引用:北京市第十五中学2022-2023学年高二上学期期中考试 化学试题
名校
解题方法
5 . 下列做法或实验(图中部分夹持略),能达到目的的是
| 防止铁管道被腐蚀 | 探究化学反应速率的影响因素 | 精炼粗铜 | 检验产生的SO2 |
 |  | 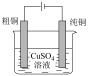 |  |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
6 . 化学小组研究金属的电化学腐蚀,实验如下:
下列说法不正确的是
| 序号 | 实验I | 实验Ⅱ |
| 实验 |  | 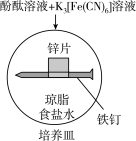 |
| 现象 | 铁钉周边出现蓝色铜片周边略显红色 | 铁钉周边出现_______色 锌片周边未见明显变化 |
A.实验I中正极的电极反应式: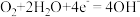 |
| B.实验Ⅱ中铁钉周边出现红色 |
C.实验Ⅱ中负极的电极反应式: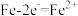 |
| D.对比实验I、Ⅱ可知,生活中镀锌铁板比镀铜铁板在镀层破损后更耐腐蚀 |
您最近一年使用:0次
7 . 用铁铆钉固定铜板,通常会发生腐蚀,如图所示。下列说法不正确 的是


| A.铁铆钉做负极发生锈蚀 |
B.铁失去的电子通过水膜传递给 |
| C.铜板的存在会加速铁铆钉腐蚀 |
D.铁元素变化过程: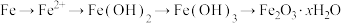 |
您最近一年使用:0次
8 . 用下图所示的实验装置,按下列实验设计不能 完成的实验是
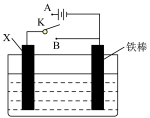

| 选项 | 实验目的 | 实验设计 |
| A | 制备金属钠 | X为石墨棒,水溶液含 、 、 ,开关K置于A处 ,开关K置于A处 |
| B | 减缓铁的腐蚀 | X为锌棒,水溶液含 、 、 ,开关K置于B处 ,开关K置于B处 |
| C | 在铁棒上镀铜 | X为铜棒,水溶液含 、 、 ,开关K置于A处 ,开关K置于A处 |
| D | 比较铁和铜的金属活动性强弱 | X为铜棒,水溶液含H+、 ,开关K置于B处 ,开关K置于B处 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
9 . 某小组学生研究常见的金属腐蚀现象,分析其原理。按要求回答下列问题。
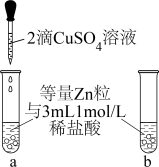
(1)甲同学设计如图所示对比实验。当a中滴入 溶液后,观察到其中产生气泡的速率较b中的
溶液后,观察到其中产生气泡的速率较b中的__ (填“快”或“慢”)。其原因是_____________________________________________________ 。
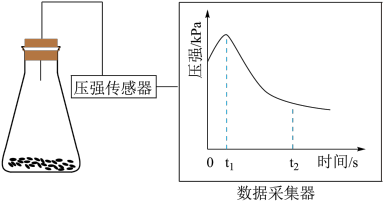
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。
①0~ 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为____________ 。
② ~
~ 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为_____________________________________________________ 。
③0~ 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为________________________________________________ 。
(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
①暖贴工作时,铁粉发生的反应为________________________ (填“氧化反应”或“还原反应”)。
②当暖贴放热结束时,铁粉转化成的物质中可能含有________________________ 。
(1)甲同学设计如图所示对比实验。当a中滴入
 溶液后,观察到其中产生气泡的速率较b中的
溶液后,观察到其中产生气泡的速率较b中的
(2)乙同学将锥形瓶内壁用酸化的饱和食盐水润洗后,放入混合均匀的铁粉和碳粉,塞紧瓶塞,同时用压强传感器测得锥形瓶内压强的变化,如图所示。

①0~
 时,碳粉表面生成的气体为
时,碳粉表面生成的气体为②
 ~
~ 时,碳粉表面发生的电极反应式为
时,碳粉表面发生的电极反应式为③0~
 电化学腐蚀过程中,铁极的电极反应式为
电化学腐蚀过程中,铁极的电极反应式为(3)丙同学研读如下一次性保暖贴说明书,并分析暖贴工作原理。
| 品名:一次性保暖贴 主要成分:铁粉、水、食盐、活性炭、蛭石、吸水性树脂 产品性能:平均温度55,最高温度63,发热时间12小时以上 |
②当暖贴放热结束时,铁粉转化成的物质中可能含有
您最近一年使用:0次
10 . 甲、乙同学分别用下图所示装置验证铁的电化学防腐原理。
相同时间后进行如下实验
实验①:甲同学分别向Ⅰ、Ⅱ中Fe电极附近滴加 溶液,Ⅰ中产生蓝色沉淀,Ⅱ中无沉淀。
溶液,Ⅰ中产生蓝色沉淀,Ⅱ中无沉淀。
实验②:乙同学分别取Ⅰ、Ⅱ中Fe电极附近溶液,滴加 溶液,Ⅰ、Ⅱ中均无沉淀。
溶液,Ⅰ、Ⅱ中均无沉淀。

下列说法正确的是
相同时间后进行如下实验
实验①:甲同学分别向Ⅰ、Ⅱ中Fe电极附近滴加
 溶液,Ⅰ中产生蓝色沉淀,Ⅱ中无沉淀。
溶液,Ⅰ中产生蓝色沉淀,Ⅱ中无沉淀。实验②:乙同学分别取Ⅰ、Ⅱ中Fe电极附近溶液,滴加
 溶液,Ⅰ、Ⅱ中均无沉淀。
溶液,Ⅰ、Ⅱ中均无沉淀。
下列说法正确的是
A.Ⅰ是牺牲阳极保护法,负极反应式为 |
| B.Ⅱ为外加电流阴极保护法,Fe电极与外接电源的正极相连 |
C.由实验①中Ⅰ、Ⅱ现象的差异,推测 在Ⅰ中氧化性强于Ⅱ 在Ⅰ中氧化性强于Ⅱ |
| D.由实验可知,两种保护法均能保护Fe,且Ⅱ保护得更好 |
您最近一年使用:0次