名校
解题方法
1 . 回答下列问题:
(1)金属腐蚀是指金属与周围接触到的空气或液体发生
(2)金属腐蚀可分为
(3)金属发生电化学腐蚀时,可分为析氢腐蚀和 吸氧腐蚀。两者的本质相同,但正极反应不同,析氢腐蚀的正极反应为
(4)钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。

①钢铁腐蚀主要是吸氧腐蚀,该腐蚀过程中负极电极反应式为
②为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
③图乙所示的方案也可以降低铁闸门的腐蚀速率,其中铁闸门应该连接在直流电源的
您最近半年使用:0次
解题方法
2 . 港珠澳大桥设计使用寿命为120年,可以对桥体钢构件采用多种方法防腐。下列分析错误的是
| A.防腐原理主要是避免发生电化学腐蚀 |
| B.钢构件表面进行发蓝处理是为了隔绝空气、水等,防止形成原电池 |
| C.在钢构件上绑上锌块的保护方法叫外加电流法 |
| D.钢材中加入Cr、Ni形成不锈钢材料以减缓腐蚀速率 |
您最近半年使用:0次
解题方法
3 . 研究青铜器(含Cu、Sn等)在潮湿的环境中发生的腐蚀对于文物保护和修复有重要意义。如图为青铜器在潮湿的环境中发生电化学腐蚀的原理示意图。下列说法正确的是
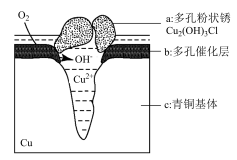

| A.青铜器发生析氢腐蚀,图中c作负极,被氧化 |
| B.环境中的Cl-与电极产物生成a离子方程式为2Cu2++3OH-+Cl-=Cu2(OH)3Cl |
| C.将青铜长时间浸泡在稀硝酸中是除去青铜表面粉状锈的一种有效方法 |
| D.青铜基体与外接电源正极相连可以减缓青铜的腐蚀 |
您最近半年使用:0次
解题方法
4 . 电化学原理在金属防腐、物质制备方面有重要的作用。
Ⅰ.某研究小组利用如图所示装置探究金属Fe的腐蚀与防护条件,将裹有锌片的铁钉放入溶有琼脂的饱和 溶液中,滴入少量酚酞(如图甲所示),回答下列问题。
溶液中,滴入少量酚酞(如图甲所示),回答下列问题。
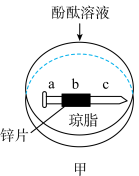
(1)一段时间后a处可能出现的现象是___________ ,相关电极反应式为___________ 。
(2)某同学为验证选择的铁钉未被腐蚀,取少量溶液于试管,滴加灵敏的黄色检验试剂,该试剂化学式为___________ ,证明铁钉未被腐蚀的现象为___________ 。实验表明,相对不活泼的金属得到了保护,该金属防护的方法称为___________ 。
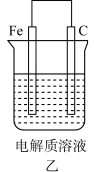
(3)钢铁的吸氧腐蚀示意图如图乙,在图某处稍作修改构成利用外加电流保护钢铁的装置,请在图上作出修改___________ 。
Ⅱ.某研究小组又利用如图装置电解 溶液制备
溶液制备 ,同时获得氢气。请回答以下问题:
,同时获得氢气。请回答以下问题:
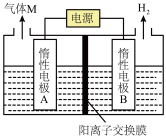
(4)B电极的电极反应式为___________ 。
(5)工作过程中,A电极上每生成 气体M,理论上制得
气体M,理论上制得
___________ g。
(6)电解池的总反应为___________ (化学方程式)。
Ⅰ.某研究小组利用如图所示装置探究金属Fe的腐蚀与防护条件,将裹有锌片的铁钉放入溶有琼脂的饱和
 溶液中,滴入少量酚酞(如图甲所示),回答下列问题。
溶液中,滴入少量酚酞(如图甲所示),回答下列问题。
(1)一段时间后a处可能出现的现象是
(2)某同学为验证选择的铁钉未被腐蚀,取少量溶液于试管,滴加灵敏的黄色检验试剂,该试剂化学式为
(3)钢铁的吸氧腐蚀示意图如图乙,在图某处稍作修改构成利用外加电流保护钢铁的装置,请在图上作出修改

Ⅱ.某研究小组又利用如图装置电解
 溶液制备
溶液制备 ,同时获得氢气。请回答以下问题:
,同时获得氢气。请回答以下问题:
(4)B电极的电极反应式为
(5)工作过程中,A电极上每生成
 气体M,理论上制得
气体M,理论上制得
(6)电解池的总反应为
您最近半年使用:0次
名校
5 . 下列实验装置不能达到实验目的的是
| 实验装置 | 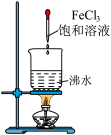 |  | 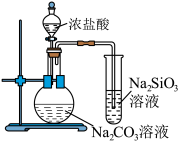 | 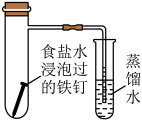 |
| 实验目的 | 制备 胶体 胶体 | 分离乙酸乙酯和乙醇 | 证明酸性: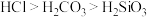 | 证明铁钉能够发生吸氧腐蚀 |
| 选项 | A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
解题方法
6 . 用下图所示装置及试剂进行铁的电化学腐蚀实验探究,测得具支锥形瓶中压强、溶解氧随时间变化关系的曲线如下。下列分析不正确的是
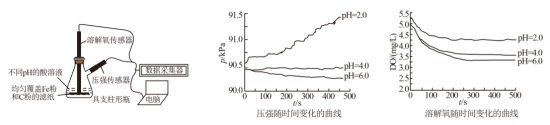

| A.pH=4时,既发生吸氧腐蚀,又发生析氢腐蚀 |
| B.pH=6时,正极反应主要是:O2+ 4e+ 4H+ = 2H2O |
| C.不同pH时,负极的反应都是:Fe-2e-= Fe2+ |
| D.压强增大主要是因为该反应为放热反应 |
您最近半年使用:0次
解题方法
7 . 为防止城市地下金属管道被锈蚀,延长管道的使用寿命,可用如图所示方法进行保护。下列说法不正确的是
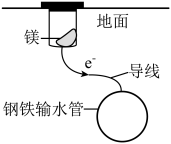

| A.该方法称为“牺牲阳极法” | B.该方法中钢铁输水管作负极 |
| C.该方法将化学能转化成了电能 | D.镁块上发生的电极反应为: |
您最近半年使用:0次
8 . 钢铁制品经常要进行烤蓝处理,即在铁制品的表面生成一层致密的 。某化学兴趣小组为了研究烤蓝铁片,进行了以下实验操作:
。某化学兴趣小组为了研究烤蓝铁片,进行了以下实验操作:
Ⅰ.把一定量烤蓝铁片加工成均匀粉末;
Ⅱ.取一定量的粉末,放入28.00mL1mol/L的盐酸中,二者恰好完全反应,生成 (标况),再向溶液中滴入KSCN溶液,无现象。
(标况),再向溶液中滴入KSCN溶液,无现象。
已知:①不考虑空气对反应的影响;②杂质不参与反应,下列说法错误的是
 。某化学兴趣小组为了研究烤蓝铁片,进行了以下实验操作:
。某化学兴趣小组为了研究烤蓝铁片,进行了以下实验操作:Ⅰ.把一定量烤蓝铁片加工成均匀粉末;
Ⅱ.取一定量的粉末,放入28.00mL1mol/L的盐酸中,二者恰好完全反应,生成
 (标况),再向溶液中滴入KSCN溶液,无现象。
(标况),再向溶液中滴入KSCN溶液,无现象。已知:①不考虑空气对反应的影响;②杂质不参与反应,下列说法错误的是
A.由实验可知,反应后所得的溶液中一定无 |
| B.样品中氧元素的物质的量为0.008mol |
| C.样品中铁元素的含量约为70% |
| D.钢铁制品表面进行烤蓝处理可以防止钢铁制品的腐蚀生锈 |
您最近半年使用:0次
解题方法
9 . 在实验室中进行下列实验,下列操作能实现实验目的的是
| 选项 | 实验目的 | 操作 |
| A | 检验甲酸中是否含有羧基 | 取其水溶液于试管中,向其中加入少量金属钠,观察溶液中有无气泡产生 |
| B | 检验某溶液中是否含有 | 取少量待测液于试管中,向其中滴加浓氨水,生成白色沉淀,继续滴加浓氨水,观察沉淀是否溶解 |
| C | 检验牺牲阳极法对钢铁防腐的效果 | 将镀层有破损的镀锌铁片放入酸化的3%NaCl溶液中,一段时间后,取少量溶液向其中加入 溶液,观察有无蓝色沉淀生成 溶液,观察有无蓝色沉淀生成 |
| D | 探究氢离子浓度对 、 、 互相转化影响 互相转化影响 | 向 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 溶液中缓慢滴加浓盐酸,观察溶液颜色的变化 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-01-02更新
|
338次组卷
|
2卷引用:山西省三重教育2023-2024学年高三上学期联考理科综合试题
解题方法
10 . “乌铜走银”是我国非物质文化遗产之一、匠人以铜为胎,将氧化变黑的银丝( )嵌入铜器表面已錾刻好的花纹内,然后用汗湿的手边捂边揉搓铜器,使铜胎变得乌黑,银丝变得光亮,呈现出黑白分明的装饰效果。下列叙述正确的是
)嵌入铜器表面已錾刻好的花纹内,然后用汗湿的手边捂边揉搓铜器,使铜胎变得乌黑,银丝变得光亮,呈现出黑白分明的装饰效果。下列叙述正确的是

 )嵌入铜器表面已錾刻好的花纹内,然后用汗湿的手边捂边揉搓铜器,使铜胎变得乌黑,银丝变得光亮,呈现出黑白分明的装饰效果。下列叙述正确的是
)嵌入铜器表面已錾刻好的花纹内,然后用汗湿的手边捂边揉搓铜器,使铜胎变得乌黑,银丝变得光亮,呈现出黑白分明的装饰效果。下列叙述正确的是
| A.揉搓工序中电子从铜器经汗液流向银丝 |
| B.铜作为原电池的负极发生了吸氧腐蚀 |
| C.铜和银均不活泼,在任何条件下都不能形成原电池 |
| D.用铁丝代替银丝,铜器不会变黑 |
您最近半年使用:0次
2023-12-24更新
|
742次组卷
|
3卷引用:山西省忻州市名校2023-2024学年高三上学期联合质量检测化学试卷
山西省忻州市名校2023-2024学年高三上学期联合质量检测化学试卷广东省部分名校2023-2024学年高三上学期联合质量检测化学试题(已下线)寒假收官卷01-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)



