解题方法
1 . 下列叙述中正确的是
A.保持容器容积不变,向反应 中充入 中充入 ,反应速率一定加快 ,反应速率一定加快 |
| B.若在海轮外壳上附着一些铜块,则可以减缓海轮外壳的腐蚀 |
| C.医用硝酸铵速冷冰袋是利用硝酸铵溶于水吸热的性质 |
D.稀盐酸和稀氢氧化钠反应的中和热为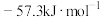 ,则稀醋酸和稀氨水反应的中和热也为 ,则稀醋酸和稀氨水反应的中和热也为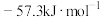 |
您最近半年使用:0次
2 . 下列有关化学与生活和科技发展等的解释,不正确的一项是
| A.以硅树脂为基体的自供电软机器人成功挑战马里亚纳海沟,硅树脂是一种高分子材料 |
| B.铜梁非物质文化遗产“打铁花”,是利用了铁元素的焰色试验 |
| C.长江边上停靠的166舰,舰底镶嵌了很多锌块,这是利用牺牲阳极法对舰底进行保护 |
D.核电站反应堆所用轴棒中含有的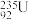 与 与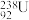 互为同位素 互为同位素 |
您最近半年使用:0次
解题方法
3 . 下列实验装置或操作设计正确、且能达到目的的是


| A.实验①,设计铜银双液原电池 |
| B.实验②,将钢闸门与外接电源的负极相连,可防止钢闸门腐蚀 |
C.实验③,准确量取一定体积 标准溶液 标准溶液 |
D.实验④,蒸干氯化铁溶液制 |
您最近半年使用:0次
4 . 某锂电池的反应式为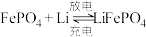 ,回答下列问题:
,回答下列问题:
(1)为防止水体中的钢铁制品发生化学腐蚀,可采用外加电源的阴极保护法,如图是以海水中的钢铁闸门为例的保护图示,则锂电池_______ (填“正极”或“负极”)接钢铁闸门。
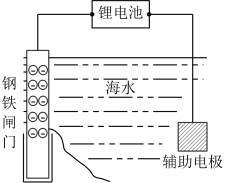
(2)碳钢管发生电化学腐蚀是因为形成了原电池,其负极的电极反应式为_______ 。在铁制品表面镀锌也可防止铁制品被腐蚀,镀锌层即使局部破损,仍可防止破损部位被腐蚀,原因是_______ 。
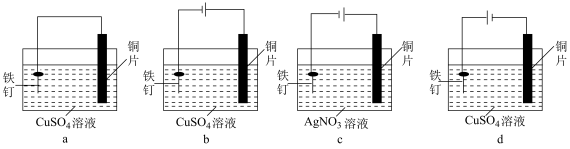
(3)下列“铁钉镀铜”实验装置设计正确的是_______ 。
(4)若以该锂电池为电源,电解 稀溶液,制备
稀溶液,制备 和
和 ,则阴极的电极反应式为
,则阴极的电极反应式为_______ 。
(5)该蓄电池放电过程中发生还原反应的物质是_______ (写化学式),充电时外电路中转移了 ,则阴极产物的质量为
,则阴极产物的质量为_______ g。
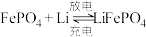 ,回答下列问题:
,回答下列问题:(1)为防止水体中的钢铁制品发生化学腐蚀,可采用外加电源的阴极保护法,如图是以海水中的钢铁闸门为例的保护图示,则锂电池

(2)碳钢管发生电化学腐蚀是因为形成了原电池,其负极的电极反应式为
(3)下列“铁钉镀铜”实验装置设计正确的是

(4)若以该锂电池为电源,电解
 稀溶液,制备
稀溶液,制备 和
和 ,则阴极的电极反应式为
,则阴极的电极反应式为(5)该蓄电池放电过程中发生还原反应的物质是
 ,则阴极产物的质量为
,则阴极产物的质量为
您最近半年使用:0次
名校
解题方法
5 . 某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,其中不正确的是
A.可逆反应中反应物的转化率都小于 |
| B.使用催化剂既不会改变反应的限度也不会改变反应的焓变 |
| C.吸热反应就是反应物的总能量比生成物的总能量高 |
| D.金属的电化学腐蚀要比化学腐蚀的速率大得多 |
您最近半年使用:0次
名校
解题方法
6 . 完成下列问题:
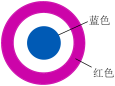
(1)取一块打磨过的生铁片,在其表面滴一滴含酚酞和K3[Fe(CN)6]的食盐水,放置一段时间后,生铁片上出现如图所示“斑痕”,其边缘为红色,中心区域为蓝色,在两色环交界处出现铁锈,生铁片发生___________ 腐蚀,边缘区的电极反应式为___________ 。
(2)区分晶体和非晶体最可靠的方法是___________ 。
(3)以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为___________ 。
(4)以多孔铂为电极,如图装置中A、B口分别通入CH3CH2OH和O2构成乙醇燃料电池,则b电极是___________ (填“正极”或“负极”),该电池的负极的电极反应式为___________

用该燃料电池作为电源进行电解,将两个铂电极插入500 mL CuSO4溶液中进行电解,通电一定时间后,某一电极增重0.064 g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化),此时溶液中氢离子浓度约为___________ 。
(5)利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,装置如图所示:
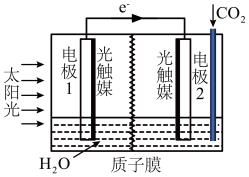
①电极2的电极反应式是___________ 。
②在标准状况下,当产生22.4 L O2时,理论上电极1室液体质量变化___________ g。
(学法题)书写电极反应式时应注意哪些问题___________ 。
(1)取一块打磨过的生铁片,在其表面滴一滴含酚酞和K3[Fe(CN)6]的食盐水,放置一段时间后,生铁片上出现如图所示“斑痕”,其边缘为红色,中心区域为蓝色,在两色环交界处出现铁锈,生铁片发生

(2)区分晶体和非晶体最可靠的方法是
(3)以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极反应式为
(4)以多孔铂为电极,如图装置中A、B口分别通入CH3CH2OH和O2构成乙醇燃料电池,则b电极是

用该燃料电池作为电源进行电解,将两个铂电极插入500 mL CuSO4溶液中进行电解,通电一定时间后,某一电极增重0.064 g(设电解时该电极无氢气析出,且不考虑水解和溶液体积变化),此时溶液中氢离子浓度约为
(5)利用人工光合作用可将CO2转化为甲酸,反应原理为2CO2+2H2O=2HCOOH+O2,装置如图所示:

①电极2的电极反应式是
②在标准状况下,当产生22.4 L O2时,理论上电极1室液体质量变化
(学法题)书写电极反应式时应注意哪些问题
您最近半年使用:0次
名校
7 . 如图所示,某同学设计了一个甲醚( )燃料电池并探究氯碱工业原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:
)燃料电池并探究氯碱工业原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:
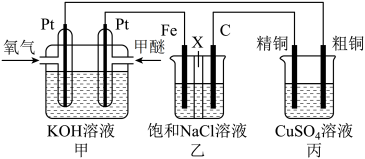
(1)通入氧气的电极为______ (填“正极”或“负极”),写出负极的电极反应式___________ 。
(2)铁电极为_______ (填“阳极”或“阴极”),石墨电极的电极反应式为________ 。
(3)反应一段时间后,乙装置中生成 主要在
主要在_____ (填“铁极”或“石墨极”)区。
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为___________ 。反应一段时间,硫酸铜溶液浓度将______ (填“增大”“减小”或“不变”)。
(5)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为_______ L;丙装置中阴极析出铜的质量为_______ g。
(6)培养皿内装有含 饱和溶液的琼脂,再滴入5~6滴酚酞溶液和
饱和溶液的琼脂,再滴入5~6滴酚酞溶液和______ 溶液,混合均匀,铁钉用砂纸磨光,缠上铜丝放入培养皿中。一段时间后,可观察到没有缠铜丝的铁钉附近产生_____ 色的______ (填化学式)沉淀;铜丝周围的现象是________ ,发生的电极反应式为___________ 。

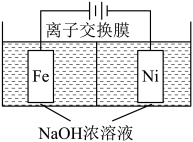
(7)工业上用电解法制取 ,同时获得氢气:
,同时获得氢气: ,工作原理如图所示,电解一段时间后,阳极室发生的电极反应式为
,工作原理如图所示,电解一段时间后,阳极室发生的电极反应式为___________ 。
 )燃料电池并探究氯碱工业原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:
)燃料电池并探究氯碱工业原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:
(1)通入氧气的电极为
(2)铁电极为
(3)反应一段时间后,乙装置中生成
 主要在
主要在(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为
(5)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为
(6)培养皿内装有含
 饱和溶液的琼脂,再滴入5~6滴酚酞溶液和
饱和溶液的琼脂,再滴入5~6滴酚酞溶液和
(7)工业上用电解法制取
 ,同时获得氢气:
,同时获得氢气: ,工作原理如图所示,电解一段时间后,阳极室发生的电极反应式为
,工作原理如图所示,电解一段时间后,阳极室发生的电极反应式为
您最近半年使用:0次
名校
解题方法
8 . 某同学利用如图所示装置探究金属的腐蚀与防护条件。对于该实验下列说法正确的是
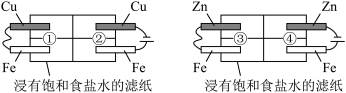

| A.①区铁电极被腐蚀,Cu电极上产生大量气泡 |
| B.②区铁电极被腐蚀,Cu电极附近滴加酚酞溶液后变成红色 |
| C.③区铁电极被防护,Fe电极反应式为2H2O+2e-=H2↑+2OH- |
| D.④区铁电极被防护,Zn电极反应式为Zn-2e-=Zn2+ |
您最近半年使用:0次
名校
解题方法
9 . 化学与生产生活息息相关,下列说法错误的是
| A.TiCl4经水解、焙烧可得到TiO2 |
| B.二氧化硫可用作葡萄酒中的添加剂 |
| C.在钢铁部件表面进行发蓝处理是通过生成一层致密的Fe2O3薄膜达到防腐效果 |
| D.FeSO4可用作污水处理的混凝剂 |
您最近半年使用:0次
名校
10 . 能正确表达下列反应的离子方程式为。
A.电解饱和食盐水获取烧碱和氯气: |
B. 与过量浓氨水反应的离子方程式: 与过量浓氨水反应的离子方程式: |
C.硫酸铝溶液中滴加少量氢氧化钾溶液: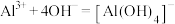 |
D.钢铁发生吸氧腐蚀,负极反应: |
您最近半年使用:0次



