名校
1 . 埋在地下的钢管道可以用如图所示方法进行电化学保护。下列说法正确的是( )
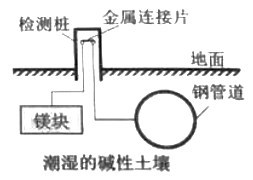

| A.该方法将电能转化成化学能 | B.该方法称为“外加电流的阴极保护法” |
| C.在此装置中钢管道作正极 | D.镁块上发生的电极反应为O2+2H2O+4e-=4OH- |
您最近一年使用:0次
2017-08-25更新
|
444次组卷
|
10卷引用:福建省长乐高级中学2018-2019学年高二下学期期末考试化学试题
福建省长乐高级中学2018-2019学年高二下学期期末考试化学试题河北省衡水中学2016-2017学年高一下学期期末考试化学试题吉林省辽源市第五中学2016-2017学年高二下学期期末考试化学试题吉林省白城市通榆县第一中学2018届高三12月月考理综化学试题高中化学人教版 选修四 第四章 电化学基础 第四节 金属的电化学腐蚀与防护 金属的电化学腐蚀与防护湖南省衡阳市第八中学2018届高三上学期第五次月考化学试题山东省青岛市第58中学2018-2019学年高二上学期期中考试化学试题四川师范大学附属中学2021届高三下学期4月月考理综化学试题四川省眉山市彭山一中高2022届高三入学考试化学试题吉林省长春市十一高中2021-2022学年高一下学期第二学程考试化学试题
真题
名校
2 . 在一块表面无锈的铁片上滴食盐水,放置一段时间后看到铁片上有铁锈出现,铁片腐蚀过程中发生的总化学方程式:2Fe+2H2O+O2===2Fe(OH)2,Fe(OH)2进一步被氧气氧化为Fe(OH)3,再在一定条件下脱水生成铁锈,其原理如图。
下列说法正确的是
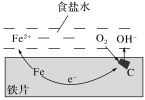
下列说法正确的是
| A.铁片发生还原反应而被腐蚀 |
| B.铁片腐蚀最严重区域应该是生锈最多的区域 |
| C.铁片腐蚀中负极发生的电极反应:2H2O+O2+4e-===4OH- |
| D.铁片里的铁和碳与食盐水形成无数微小原电池,发生了电化学腐蚀 |
您最近一年使用:0次
2017-08-19更新
|
3096次组卷
|
16卷引用:福建省泉州市泉港区第一中学2020-2021学年高二上学期期中考试化学试题
福建省泉州市泉港区第一中学2020-2021学年高二上学期期中考试化学试题浙江省2018版考前特训(2017年10月)学考70快练:原电池2016年10月浙江省普通高校招生选考科目考试化学试题浙江省宁波诺丁汉大学附属中学2017-2018学年高一下学期期末考试化学试题(已下线)考点10 电解原理 金属的腐蚀与防护——备战2019年浙江新高考化学考点北京市中国人民大学附属中学 2020届高三下学期第三次模拟化学试题(已下线)【浙江新东方】【2020】【高二上】【期中】【HD-LP406】【化学】(已下线)小题必刷26 电解池原理及其应用——2021年高考化学一轮复习小题必刷(通用版本)(已下线)6.3.1化学能转化为电能 练习-2020-2021学年下学期高一化学同步精品课堂(苏教版2019必修第二册)浙江省绍兴市第一中学2020-2021学年高三1月高考适应性考试化学试题黑龙江省大庆市铁人中学2020-2021学年高一下学期期末考试化学试题(已下线)专题六 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)专题11.电化学-十年(2012-2021)高考化学真题分项汇编(浙江专用)(已下线)4.3 金属的腐蚀和防护-2021-2022学年高二化学课后培优练(人教版2019选择性必修1)吉林省长春市农安县2021-2022学年高二上学期期末考试化学试题(已下线)考点20 金属的腐蚀与防护-备战2023年高考化学一轮复习考点帮(全国通用)
名校
3 . 下列有关说法不正确的是
| A.实验室制取氢气,为了加快反应速率,可向稀H2SO4中滴加少量Cu(NO3)2溶液 |
| B.铅蓄电池在放电过程中,负极和正极质量均增加 |
| C.在硫酸型酸雨地区,不纯的铜发生电化学腐蚀,正极反应为:O2 + 4e- + 4H+ = 2H2O |
| D.生铁发生吸氧腐蚀和析氢腐蚀的负极反应均为:Fe - 2e- = Fe2+ |
您最近一年使用:0次
2017-07-10更新
|
398次组卷
|
6卷引用:【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期10月月考化学试题
4 . 如图所示的钢铁腐蚀中,下列说法正确的是
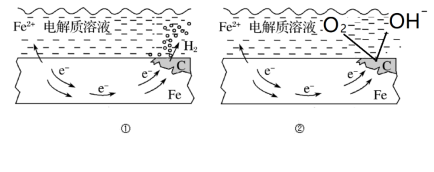

| A.碳表面发生氧化反应 |
| B.钢铁被腐蚀的最终产物为FeO |
| C.生活中钢铁制品的腐蚀以图①所示为主 |
| D.图②中,正极反应式为O2+4e-+2H2O═4OH- |
您最近一年使用:0次
2017-02-17更新
|
334次组卷
|
7卷引用:2015-2016学年福建省连江县尚德中学高二上期中考试化学试卷
名校
5 . 钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。

(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为_________ 。
(2)利用如图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于________ 处。
②若X为锌,开关K置于M处,该电化学防护法称为_______ 。
(3)图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2 g时,X电极溶解的铜的质量________ 3.2 g(填“<”“>”或“=”)。
(4)图中若X为铜,容器中海水替换为FeCl3溶液,开关K置于M处,铜电极发生的反应是______________ ,若将开关K置于N处,发生的总反应是___________ 。

(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为
(2)利用如图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于
②若X为锌,开关K置于M处,该电化学防护法称为
(3)图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2 g时,X电极溶解的铜的质量
(4)图中若X为铜,容器中海水替换为FeCl3溶液,开关K置于M处,铜电极发生的反应是
您最近一年使用:0次
2016-12-09更新
|
376次组卷
|
7卷引用:福建省南安第一中学2017-2018学年高二上学期期中考试化学试题
6 . 下列金属防腐的措施中,属于牺牲阳极的阴极保护法的是
| A.水中的钢闸门连接电源的负极 | B.地下钢管连接锌板 |
| C.汽车底盘喷涂高分子膜 | D.金属护栏表面涂漆 |
您最近一年使用:0次
2016-12-09更新
|
296次组卷
|
7卷引用:2015-2016学年福建省四地六校高二上学期第三次联考化学试卷
名校
7 . 下列有关金属腐蚀与防护的说法正确的是
| A.钢柱在水下部分比在空气与水交界处更容易腐蚀 |
| B.当镀锡铁制品的镀层破损时,镀层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
您最近一年使用:0次
2016-12-09更新
|
212次组卷
|
5卷引用:2015-2016学年福建省八县一中高二上学期期中测试化学试卷
12-13高二上·山东东营·阶段练习
名校
8 . 如图所示,装置中都盛有0.1mol·L-1的NaCl 溶液,放置一定时间后,装置中的四块相同的锌片腐蚀速率由快到慢的正确顺序是:( )


| A.①②③④ | B.①②④③ | C.②①④③ | D.③①④② |
您最近一年使用:0次
2016-12-09更新
|
196次组卷
|
13卷引用:2016-2017学年福建省莆田二十五中高二上第一次月考化学卷
2016-2017学年福建省莆田二十五中高二上第一次月考化学卷福建省清流一中2017-2018学年高二上学期第二阶段(期中)考试化学(理)试题(已下线)2012-2013学年山东东营一中高二上学期第一次模块考试化学试卷(已下线)2013-2014学年辽宁省大连普通高中高二上学期期末考试理科化学试卷(已下线)2015安徽望江中学同步课时(人教选修4)4.4金属的电化学腐蚀与防护2015-2016学年山东枣庄三中高二10月学情调查化学卷2015-2016学年山东省烟台市莱山一中高二化学上学期段考试卷2016-2017学年吉林省松原油田高中高二上期初化学卷2016-2017学年山东省枣庄八中高二上10月月考化学卷2016-2017学年河南省郑州一中高二上期中化学卷2016-2017学年江苏省沭阳县高二下学期期中调研测试化学试卷河北省定州中学2017届高三(高补班)下学期第二次月考(4月)化学试题山东省日照市第一中学2019-2020学年高二10月月考化学试题
11-12高二下·福建福州·期末
名校
9 . 下列各个装置中铁棒被腐蚀由易到难的顺序正确的是
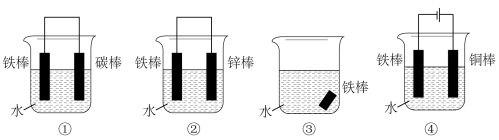

| A.③①②④ | B.④①③② | C.①③②④ | D.②④①③ |
您最近一年使用:0次
2016-12-09更新
|
435次组卷
|
11卷引用:2011-2012学年福建省福州八中高二下学期期末考试化学试卷
(已下线)2011-2012学年福建省福州八中高二下学期期末考试化学试卷(已下线)2013-2014福建省师大附中高二上学期期末考试化学试卷2015-2016学年福建省莆田二十五中高二上学期期中测试化学试卷福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题福建省莆田华侨中学2021-2022学年高二上学期期中考试化学试题福建省平潭翰英中学2021-2022学年高二上学期期中考试化学试题福建省福州市延安中学2023-2024学年高二上学期期中考试化学试题(已下线)2012-2013学年重庆市杨家坪中学高二12月月考化学试卷浙江省台州市五校2020届高三10月联考化学试题上海市七宝中学2019-2020学年高三上学期期中考化学试题鲁科版(2019)高二选择性必修第一册第1章 化学反应与能量变化 第4节 金属的腐蚀与防护 高效手册
名校
10 . 如图是自来水表的常见安装方式。下列有关说法不正确的是


| A.该安装方式的水表更容易被腐蚀 |
| B.发生腐蚀过程中,电子从接头流向水表 |
C.腐蚀时水表发生的电极反应为: 2H2O+O2+4e− 4OH− 4OH− |
D.腐蚀过程还涉及反应:4Fe(OH)2+2H2O+O2 4Fe(OH)3 4Fe(OH)3 |
您最近一年使用:0次
2016-12-09更新
|
541次组卷
|
9卷引用:福建省福州第三中学2019-2020学年高二上学期期末考试化学试题
福建省福州第三中学2019-2020学年高二上学期期末考试化学试题2014-2015广东省肇庆市高二上学期期末考试化学试卷河北省衡水市安平县安平中学2019届高三上学期期中考试化学试题【全国百强校】甘肃省兰州市第一中学2018-2019学年高二上学期期末考试化学试题浙江省温州市环大罗山联盟2020-2021学年高二上学期期中考试化学试题(已下线)考点20 金属的腐蚀与防护-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)第36练 金属的腐蚀与防护-2023年高考化学一轮复习小题多维练(全国通用)(已下线)考点20 金属的腐蚀与防护(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)第四章 第三节 金属的腐蚀与防护



