30. 氯及其化合物在生活和生产中应用广泛。
(1)已知:900 K时,4HCl(g)+O
2(g)

2Cl
2(g)+2H
2O(g),反应自发。
①该反应是放热还是吸热,判断并说明理由
______________________________________。
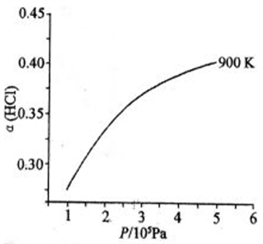
②900 K时,体积比为4:l的HCl和O
2在恒温恒容的密闭容器中发生反应,HCl的平衡转化率α(HCl) 随压强(P)变化曲线如图。保持其他条件不变,升温到T K(假定反应历程不变),请画出压强在1.5×l0
5~4.5×10
5Pa范围内,HCl的平衡转化率α(HCl)随压强(P)变化曲线示意图
_________。
(2)已知:Cl
2(g)+2NaOH(aq)==NaCl(aq)+NaClO(aq)+H
2O(l)
△H
l=―102 kJ·mol
-13Cl
2(g)+6NaOH(aq)==5NaCl(aq)+NaClO
3(aq)+3H
2O(1)
△H
2=―422 kJ·mol
—1①写出在溶液中NaClO分解生成NaClO
3的热化学方程式
_____________________。
②用过量的冷NaOH溶液吸收氯气,制得NaClO溶液(不含NaClO
3),此时ClO
―的浓度为c
0 mol·L
-1;加热时NaClO转化为NaClO
3,测得t时刻溶液中ClO
―浓度为c
t mol·L
-1,写出该时刻溶液中Cl
―浓度的表达式;c(Cl
―)=
_________ mol·L
-1 (用c
0、c
t表示)
③有研究表明,生成NaClO
3的反应分两步进行:
I、2ClO
―=ClO
2―+Cl
―II、ClO
2―+ClO
―=ClO
3―+Cl
―常温下,反应II能快速进行,但氯气与NaOH溶液反应很难得到NaClO
3,试用碰撞理论解释其原因:
_______________________________。
(3)电解NaClO
3水溶液可制备NaClO
4。在电解过程中由于阴极上吸附氢气,会使电解电压升高,电解效率下降。为抑制氢气的产生,可选择合适的物质(不引入杂质),写出该电解的总化学方程式
________________________________________。