名校
解题方法
1 . 以下实验目的、方法和相关解释都正确的是
| 选项 | 实验目的 | 实验方法 | 相关解释 |
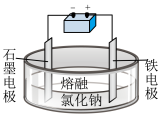
| A | 电解熔融氯化钠 |
| 该装置阳极反应为2Cl--2e-=Cl2 |
| B | 金属防腐 |
| 该图采用的是外加电流法对铁管道进行保护 |
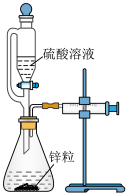
| C | 测量锌粒和不同浓度的硫酸溶液反应速率的快慢 |
| 该实验用到的实验仪器有恒压滴液漏斗、锥形瓶、双孔塞、注射器 |
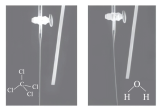
| D | 验证分子极性 |
| 该实验是用毛皮摩擦过的橡胶棒靠近 和 和 ,由图中现象可知 ,由图中现象可知 为非极性分子, 为非极性分子, 为极性分子 为极性分子 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-04-05更新
|
260次组卷
|
4卷引用:福建省厦门第一中学2023-2024学年高三下学期5月第2次月考化学试卷
解题方法
2 . 下列有关电化学腐蚀原理的应用说法错误的是
| A.利用铁腐蚀快速测定空气中氧气含量 | B.利用牺牲阳极保护法在潜艇外壳上镶嵌铜块 |
| C.以铁作为阴极在铁表面镀铜 | D.采用阴极电保护法防止铁管道腐蚀 |
您最近一年使用:0次
3 . 下列实验设计或所选装置合理的是
 | 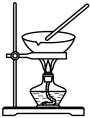 |  |  |
A.通过注射器活塞右移,验证 与 与 反应放热 反应放热 | B.由 制无水 制无水 固体 固体 | C.电解 溶液,制备金属 溶液,制备金属 | D.模拟钢铁的吸氧腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
4 . 化学与社会、生活、生产密切相关,下列有关说法错误的是
| A.洗涤油污常用热的Na2CO3溶液,这是利用了盐类水解的原理 |
| B.航天员所穿航天服的主要成分是由碳化硅、陶瓷和碳纤维复合而成的,它是一种新型无机非金属材料 |
| C.“闽鹭”是我国制造的第四艘LNG船,船底镶嵌锌块,锌作负极,以防船体被腐蚀 |
| D.高纯硅是制备光导纤维的原料 |
您最近一年使用:0次
5 . 化学与生活密切相关,下列说法正确的是
A.一氧化碳与血红蛋白 存在反应: 存在反应: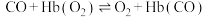 ,当 ,当 中毒时,平衡向右移动,使人体组织局部氧气浓度过高而中毒 中毒时,平衡向右移动,使人体组织局部氧气浓度过高而中毒 |
| B.海轮的外壳附上一些锌块,是利用了电解原理的牺牲阳极的阴极保护法 |
C.汽车尾气治理原理为: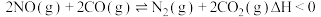 ,由于需要借助催化转化器,因此推断该反应在常温下不能自发反应 ,由于需要借助催化转化器,因此推断该反应在常温下不能自发反应 |
| D.比色分析法可用于某些化学反应速率测定,是利用有色物质浓度与溶液颜色的关系 |
您最近一年使用:0次
名校
解题方法
6 . 回答下列问题
(1)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:
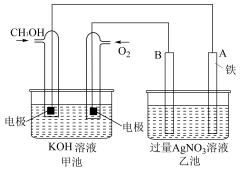
①放电时,甲醇在___________ (填“正”或“负”)极发生反应,正极的电极反应为___________ 。
②工作时,B极的电极反应式为___________ ,A极的电极反应式为___________ 。
(2)某同学设计了一种用电解法制取Fe(OH)2的实验装置(如图所示)通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。

(3)如图所示将铁棒和石墨棒插入盛有饱和NaCl溶液的 型管中。
型管中。
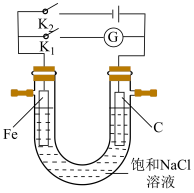
①K1闭合,铁电极的反应为___________ 。
②K2闭合,铁棒不会被腐蚀,属于___________ 保护法。
(1)某公司开发了一种以甲醇为原料,以KOH为电解质的用于手机可充电的高效燃料电池,充一次电可连续使用一个月。其中B电极的电极材料为碳,如图是一个电化学过程的示意图。请填空:

①放电时,甲醇在
②工作时,B极的电极反应式为
(2)某同学设计了一种用电解法制取Fe(OH)2的实验装置(如图所示)通电后,溶液中产生大量的白色沉淀,且较长时间不变色。下列说法不正确的是___________(填序号)。

A. 为电源正极, 为电源正极, 为电源负极 为电源负极 | B.可以用NaCl溶液作为电解质溶液 |
| C.A、B两端都必须用铁作电极 | D.阴极发生的反应为2H2O+2e-=2OH-+H2↑ |
(3)如图所示将铁棒和石墨棒插入盛有饱和NaCl溶液的
 型管中。
型管中。
①K1闭合,铁电极的反应为
②K2闭合,铁棒不会被腐蚀,属于
您最近一年使用:0次
名校
解题方法
7 . 下列说法正确的是
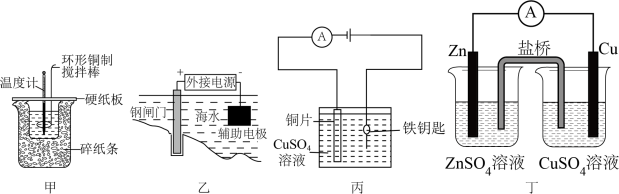

A.用图甲装置测得中和热 偏大 偏大 |
| B.图乙可以保护钢闸门不被腐蚀 |
| C.图丙用于铁上镀铜且硫酸铜溶液浓度不变 |
D.图丁装置盐桥中阴离子向 溶液中迁移 溶液中迁移 |
您最近一年使用:0次
2023-12-14更新
|
417次组卷
|
4卷引用:福建省福州格致中学2023-2024学年高二上学期期中考试化学试题
福建省福州格致中学2023-2024学年高二上学期期中考试化学试题(已下线)寒假收官卷02-【寒假分层作业】2024年高二化学寒假培优练(人教版2019)江西省宜春市宜丰中学2023-2024学年高一上学期1月期末化学试题重庆市万州二中2023-2024学年高二下学期开学考试 化学
8 . 化学与生活等密切相关,下列说法错误的是
| A.铁质菜刀生锈与氧化还原反应有关 |
| B.明矾溶于水后能形成胶体,可用于净水 |
| C.铵态氮肥与熟石灰混合研磨时有刺激性气味的气体产生 |
| D.利用同位素的放射性可以进行医疗诊断和治疗,所以放射性同位素都是有益的 |
您最近一年使用:0次
名校
解题方法
9 . 请回答下列问题:
(1)高铁酸钾( )不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图所示是高铁电池的模拟实验装置。
)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图所示是高铁电池的模拟实验装置。
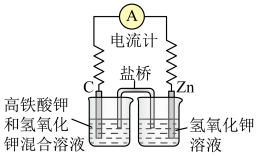
①该电池放电时正极反应式为___________ 。
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向___________ (填“左”或“右”)移动;
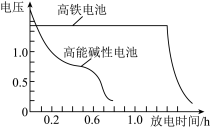
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有___________ 。
(2)铜是人类最早使用的金属,它与人类生产、生活关系密切,请运用所学知识解释下列与铜有关的化学现象。
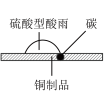
①如图,在硫酸型酸雨地区,不纯的铜制品发生电化学腐蚀,Cu发生___________ (填“氧化”或“还原”)反应,写出正极的电极反应式:___________ 。
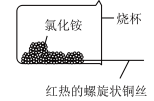
②如下图,将螺旋状的铜丝在酒精灯上灼烧,铜丝变黑色,然后将红热的铜丝插入 固体中,过一会取出,发现插入部分黑色变为光亮的红色,查阅资料可知,该过程有
固体中,过一会取出,发现插入部分黑色变为光亮的红色,查阅资料可知,该过程有 生成,写出由黑色变为光亮红色过程中反应的化学方程式:
生成,写出由黑色变为光亮红色过程中反应的化学方程式:___________ 。
(3)一定温度下,反应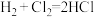 中的某一基元反应为
中的某一基元反应为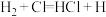 ,其能量变化如图所示。
,其能量变化如图所示。 表示反应物分子旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
表示反应物分子旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
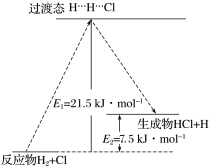
该基元反应的活化能为___________ kJ/mol, 为
为___________ kJ/mol。
(4)键能也可以用于估算化学反应的反应热( )。下表是部分化学键的键能数据:
)。下表是部分化学键的键能数据:
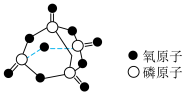
已知白磷的标准燃烧热为-2378kJ/mol,白磷的结构为正四面体,白磷完全燃烧的产物结构如图所示,则上表中
___________ 。
(1)高铁酸钾(
 )不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图所示是高铁电池的模拟实验装置。
)不仅是一种理想的水处理剂,而且高铁电池的研制也在进行中。如图所示是高铁电池的模拟实验装置。
①该电池放电时正极反应式为
②盐桥中盛有饱和KCl溶液,此盐桥中氯离子向
③下图为高铁电池和常用的高能碱性电池的放电曲线,由此可得出高铁电池的优点有

(2)铜是人类最早使用的金属,它与人类生产、生活关系密切,请运用所学知识解释下列与铜有关的化学现象。
①如图,在硫酸型酸雨地区,不纯的铜制品发生电化学腐蚀,Cu发生

②如下图,将螺旋状的铜丝在酒精灯上灼烧,铜丝变黑色,然后将红热的铜丝插入
 固体中,过一会取出,发现插入部分黑色变为光亮的红色,查阅资料可知,该过程有
固体中,过一会取出,发现插入部分黑色变为光亮的红色,查阅资料可知,该过程有 生成,写出由黑色变为光亮红色过程中反应的化学方程式:
生成,写出由黑色变为光亮红色过程中反应的化学方程式:
(3)一定温度下,反应
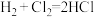 中的某一基元反应为
中的某一基元反应为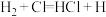 ,其能量变化如图所示。
,其能量变化如图所示。 表示反应物分子旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
表示反应物分子旧化学键没有完全断裂、新化学键没有完全形成的过渡态。
该基元反应的活化能为
 为
为(4)键能也可以用于估算化学反应的反应热(
 )。下表是部分化学键的键能数据:
)。下表是部分化学键的键能数据:| 化学键 |  |  |  | 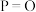 |
| 键能/(kJ/mol) | 172 | 335 | 498 | X |


您最近一年使用:0次
解题方法
10 . 研究金属腐蚀和防腐的原理很有现实意义。
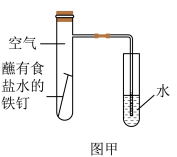
(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有_______(填序号)。
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化如表,根据数据判断腐蚀的速率随时间逐渐_______ (填“加快”、“不变”、“减慢”),你认为影响因素为_______ 。
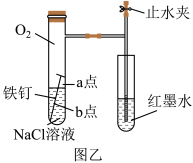
(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,完成表格空白(已知铁氰化钾溶液遇亚铁离子显蓝色,常用于亚铁离子的检验);
根据以上实验探究,试判断③_______ (填“a”或“b”)为负极,该点腐蚀更严重。
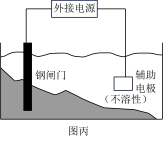
(4)图丙中钢闸门应与外接电源的_______ 相连(填“正极”或“负极”)钢闸门不会被腐蚀,属于_______ 保护法。
(5)金属阳极钝化是另一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,写出该阳极电极反应式是_______ 。
(1)甲图为人教版教材中探究钢铁的吸氧腐蚀的装置。某兴趣小组按该装置实验,导管中液柱上升缓慢,下列措施可以更快更清晰观察到水柱上升现象的有_______(填序号)。

| A.用纯氧气代替试管内空气 | B.用酒精灯加热试管提高温度 |
| C.将铁钉换成铁粉和炭粉混合粉末 | D.换成更细的导管,水中滴加红墨水 |
(2)该小组将甲图装置改进成乙图装置并进行实验,导管中红墨水液柱高度随时间的变化如表,根据数据判断腐蚀的速率随时间逐渐

| 时间/min | 1 | 3 | 5 | 7 | 9 |
| 液柱高度/cm | 0.8 | 2.1 | 3.0 | 3.7 | 4.2 |
(3)为探究铁钉腐蚀实验a、b两点所发生的反应,进行以下实验,完成表格空白(已知铁氰化钾溶液遇亚铁离子显蓝色,常用于亚铁离子的检验);
| 实验操作 | 实验现象 | 实验结论 |
| 向NaCl溶液中滴加2~3滴酚酞指示剂 | a点附近溶液出现红色 | a点电极反应为① |
| 然后再滴加2~3滴铁氰化钾溶液 | b点周围出现蓝色沉淀 | b点电极反应为② |
(4)图丙中钢闸门应与外接电源的

(5)金属阳极钝化是另一种电化学防腐方法。将Fe作阳极置于H2SO4溶液中,一定条件下Fe钝化形成致密Fe3O4氧化膜,写出该阳极电极反应式是
您最近一年使用:0次
2023-11-18更新
|
172次组卷
|
2卷引用:福建省漳州市十校2023-2024学年高二上学期期中联考化学试题