名校
1 . 用如图所示的装置进行实验,能达到实验目的是
| A | B | C | D |
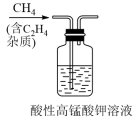 | 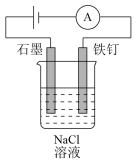 | 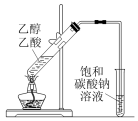 | 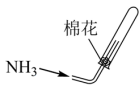 |
| 提纯CH4 | 防止铁钉生锈 | 制备并收集乙酸乙酯 | 收集氨气 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 炒过菜的铁锅未及时洗净(残液中含NaCl),不久便会因被腐蚀而出现红褐色锈班,腐蚀原理如图所示,下列说法正确的是


| A.腐蚀过程中,负极是Fe,发生电极反应:Fe-3e-=Fe3+ |
| B.该过程为金属的吸氧腐蚀 |
| C.正极的电极反应式为4OH--4e-=O2↑+2H2O |
| D.C是正极,O2在C表面上发生氧化反应 |
您最近一年使用:0次
2021-12-14更新
|
63次组卷
|
2卷引用:福建省福州市连江尚德中学等六校2021-2022学年高二上学期期中考化学试题
解题方法
3 . 深埋在潮湿土壤中的铁管道,在硫酸盐还原菌作用下,能被硫酸根离子腐蚀,其电化学腐蚀原理如下图所示。下列转述正确的是
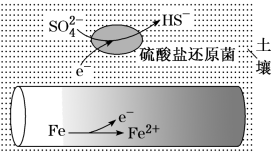

| A.此铁管道发生的是吸氧腐蚀 |
| B.输送暖气的管道也易发生此类腐蚀 |
| C.在这种情况下,土壤的c(OH-)增大 |
| D.若管道上刷富铜油漆可以延缓管道的腐蚀 |
您最近一年使用:0次
2021-12-14更新
|
300次组卷
|
2卷引用:福建省漳州市正兴学校2021-2022学年高二上学期期中考试化学试题
名校
解题方法
4 . 下列表述不正确 的是
| A | B | C | D |
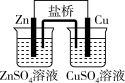 |  | 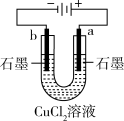 | 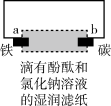 |
| 盐桥中的Cl-移向ZnSO4溶液 | 外电路电流由a极流向b极 | a极附近产生的气体能使湿润的淀粉碘化钾试纸变蓝 | 正极反应式为O2+4e-+2H2O= 4OH- |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-17更新
|
213次组卷
|
5卷引用:福建省福州市外国语学校2022-2023学年高二上学期12月阶段性测试化学试题
名校
解题方法
5 . 如图所示三套实验装置,分别回答下列问题。
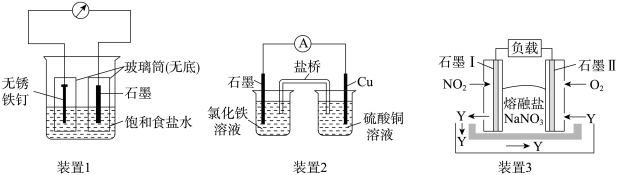
(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被___________ (填“氧化”或“还原”);向插入石墨的玻璃筒内滴入酚酞溶液,可观察到石墨附近的溶液变红,该电极反应式为___________ 。
(2)装置2中的石墨作___________ (填“正”或“负”)极,该装置发生的总反应的离子方程式为___________ 。
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为___________ (填化学式);石墨II极的电极反应式为:___________ ;当石墨I极中有1molNO2参加反应时,石墨II极消耗的O2的体积___________ (标准状况下)。

(1)装置1为铁的吸氧腐蚀实验。一段时间后,向插入铁钉的玻璃筒内滴入K3[Fe(CN)6]溶液,即可观察到铁钉附近的溶液出现蓝色沉淀,表明铁被
(2)装置2中的石墨作
(3)装置3为由NO2、O2、熔融盐NaNO3组成的燃料电池示意图。在使用过程中石墨I电极反应生成一种氧化物Y,则Y为
您最近一年使用:0次
6 . 将金属M连接在钢铁设施表面构成原电池,可减缓水体中钢铁设施的腐蚀。在如图所示的情境中,下列有关说法正确的是
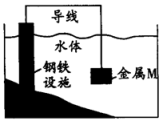

A.钢铁设施上的电极反应式为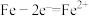 | B.电子流向:金属M→水体→钢铁设施表面 |
| C.M的金属性比Fe的金属性强 | D.钢铁设施在河水中的腐蚀速率比在海水中的快 |
您最近一年使用:0次
2021-10-28更新
|
143次组卷
|
2卷引用:福建泉州现代中学2021-2022学年高二上学期期中考试化学试题
名校
解题方法
7 . 下列有关电化学装置的说法正确的是




| A.甲图中正极的电极反应式为Ag2O+2e-+2H+=2Ag+H2O |
| B.乙图表示钢闸门用牺牲阳极的阴极保护法加以防护 |
| C.丙图中,盐桥中的K+向盛有ZnSO4溶液的烧杯中移动 |
| D.丁图中,X处补充稀NaOH溶液以增强溶液导电性 |
您最近一年使用:0次
2021-10-27更新
|
304次组卷
|
5卷引用:福建省厦门外国语学校石狮分校2021-2022学年高二上学期第一次月考化学试题
名校
解题方法
8 . 下列与金属腐蚀有关的说法,正确的是




| A.图1中,铁钉容易被腐蚀而生锈 |
B.图2中,滴加少量 溶液,溶液变为血红色 溶液,溶液变为血红色 |
| C.图3中,燃气灶的中心部位容易生锈,主要是发生电化学腐蚀 |
| D.图4中,用牺牲阳极的阴极保护法来防止地下钢铁管道的腐蚀 |
您最近一年使用:0次
名校
解题方法
9 . 装置中的纯锌棒都浸在相同浓度的稀硫酸中,锌棒腐蚀速度从快到慢的顺序是


| A.③④②① | B.②③①④ | C.④②①③ | D.③②①④ |
您最近一年使用:0次
2021-10-15更新
|
334次组卷
|
3卷引用:福建省莆田第二十五中学2021-2022学年高二上学期期中考试化学试题
名校
10 . 自嗨锅的发热包主要成分有:硅藻土、铁粉、铝粉、焦炭粉、盐、生石灰,使用时使发热包里面的物质与水接触即可。下列说法错误的是
| A.铁粉发生析氢腐蚀,缓慢放出热量,延长放热时间 |
| B.硅藻土可增大反应物的接触面积 |
| C.主要反应物为生石灰,与水反应放热 |
| D.使用后的发热包属于有害垃圾 |
您最近一年使用:0次
2021-09-17更新
|
214次组卷
|
4卷引用:福建省武平县第一中学2021-2022学年高二上学期10月月考化学试题



