名校
解题方法
1 . 如图所示,水槽中试管内有一枚铁钉,放置数天观察:

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生_______ 腐蚀,电极反应:负极:_______ 。
(3)若试管内液面下降,则原溶液呈_______ 性,发生的电极反应:正极:_______ 。

(1)铁钉在逐渐生锈。
(2)若试管内液面上升,发生
(3)若试管内液面下降,则原溶液呈
您最近一年使用:0次
解题方法
2 . “对比实验”是科学探究中的重要方法。请根据图回答下列问题:

(1)图甲铜片上白磷燃烧而水中白磷不燃烧,说明燃烧条件之一是________ 。
(2)图乙A中溶液呈紫红色,B中溶液无色,说明A中溶液呈紫红色的原因是________ 含有(填离子符号或名称)。
(3)图丙中铁钉最容易生锈的是________ (填序号)。自行车链条防锈措施是________ (任填一条)。

(1)图甲铜片上白磷燃烧而水中白磷不燃烧,说明燃烧条件之一是
(2)图乙A中溶液呈紫红色,B中溶液无色,说明A中溶液呈紫红色的原因是
(3)图丙中铁钉最容易生锈的是
您最近一年使用:0次
解题方法
3 . 生铁在干燥的空气中不易被腐蚀,但在潮湿的空气中却很快被腐蚀,为什么?为什么生铁比纯铁更易被腐蚀_______ 。
您最近一年使用:0次
名校
解题方法
4 . 某博物馆修复出土铁器的过程如下:
检测锈蚀产物
(1)铁器在潮湿的空气里容易发生_____腐蚀; 中铁元素的化合价为_____。
中铁元素的化合价为_____。
(2)不锈钢中一般加入铬元素,Cr元素基态原子的简化核外电子排布式_____ 。
分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Fe转化为 。
。
(3) 和
和 反应形成致密的
反应形成致密的 保护层,
保护层, 的作用是
的作用是_____ (填字母)。
A.氧化剂 B.还原剂 C.既不是氧化剂也不是还原剂
(4)工业上冶炼Fe常用的方法是_____(填字母)。
(5)不同价态铁离子在水溶液中转化的离子反应有: ,为了探究该反应存在一定的限度,某化学兴趣小组取
,为了探究该反应存在一定的限度,某化学兴趣小组取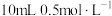 的KI溶液于试管中,再加入
的KI溶液于试管中,再加入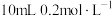 的
的 溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_____(填字母)。
溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_____(填字母)。
检测锈蚀产物
| 主要成分的化学式 | |||
 | 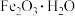 |  |  |
 中铁元素的化合价为_____。
中铁元素的化合价为_____。| A.化学 | B.电化学 | C. | D. |
分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Fe转化为
 。
。(3)
 和
和 反应形成致密的
反应形成致密的 保护层,
保护层, 的作用是
的作用是A.氧化剂 B.还原剂 C.既不是氧化剂也不是还原剂
(4)工业上冶炼Fe常用的方法是_____(填字母)。
| A.电解法 | B.还原法 | C.热分解法 | D.物理方法 |
 ,为了探究该反应存在一定的限度,某化学兴趣小组取
,为了探究该反应存在一定的限度,某化学兴趣小组取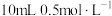 的KI溶液于试管中,再加入
的KI溶液于试管中,再加入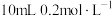 的
的 溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_____(填字母)。
溶液,振荡,使试管中的物质充分反应一段时间。为了达到实验目的,还需要再向试管中加入下列试剂中的_____(填字母)。| A.淀粉溶液 | B.KSCN溶液 | C. | D.酸性高锰酸钾溶液 |
您最近一年使用:0次
5 . 铜和铁是常见金属。但生铁易生锈,请讨论电化学实验中有关铁的性质

(1)①已知甲总反应为Fe+2HCl=FeCl2+H2↑,右电极产生H2则甲池中右电极材料为_____ ,左电极材料为_____ 。(填“Fe”或“C”)
②乙中的电解质为硫酸酸化的CuSO4溶液,现用来电解精炼铜,则左电极材料为_____ 。(填“粗铜”或“纯铜”)
③装置丙中,易生锈的是_____ (填“a”或“b”)点,发生_____ (填“析氢”或“吸氧”)腐蚀,其正极反应式为_____ 。
(2)下图为保护钢闸门的两种方法,根据所学知识完成下列填空:

①利用原电池原理保护钢闸门的是_____ (填“丁”或“戊”),在此过程中_____ (填“Fe”“Zn”或“辅助阳极”)失电子。
②戊装置中通电后,电子流向_____ (填“钢闸门”或“辅助阳极”)

(1)①已知甲总反应为Fe+2HCl=FeCl2+H2↑,右电极产生H2则甲池中右电极材料为
②乙中的电解质为硫酸酸化的CuSO4溶液,现用来电解精炼铜,则左电极材料为
③装置丙中,易生锈的是
(2)下图为保护钢闸门的两种方法,根据所学知识完成下列填空:

①利用原电池原理保护钢闸门的是
②戊装置中通电后,电子流向
您最近一年使用:0次
6 . 改变金属材料的组成
在金属中添加其他金属或非金属制成性能优异的_______ ,如普通钢加入_______ 制成不锈钢,_______ 合金不仅具有优异的_______ 能且具有良好的_______ 。
在金属中添加其他金属或非金属制成性能优异的
您最近一年使用:0次
7 . 简要回答下列问题。
(1)除去Na2CO3固体中混有少量NaHCO3的方法是___________ 。
(2)用食醋除去水壶内壁的水垢主要成分是CaCO3和Mg(OH)2的原因是___________ 。
(3)写出一种防止自行车上金属部件腐蚀的方法是___________
(1)除去Na2CO3固体中混有少量NaHCO3的方法是
(2)用食醋除去水壶内壁的水垢主要成分是CaCO3和Mg(OH)2的原因是
(3)写出一种防止自行车上金属部件腐蚀的方法是
您最近一年使用:0次
8 . 金属的防护方法
(1)在金属表面覆盖保护层,如在钢铁表面___________ 、覆盖___________ 、镀___________ 等。
(2)改变金属组成或结构,如___________ 。
(3)利用___________ 原理来保护金属,防止金属腐蚀。
(1)在金属表面覆盖保护层,如在钢铁表面
(2)改变金属组成或结构,如
(3)利用
您最近一年使用:0次
解题方法
9 . 钢铁的电化学腐蚀
(1)实验探究——钢铁的电化学腐蚀原理
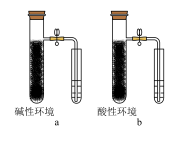
①向铁粉中加入碳粉的目的是___________ ;
②实验现象:a装置右边的小试管中液面________ ;b装置中右边小试管中液面_________ 。
(2)钢铁的电化学腐蚀
根据钢铁表面水溶液薄膜的酸碱性不同,钢铁的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,如下图所示:
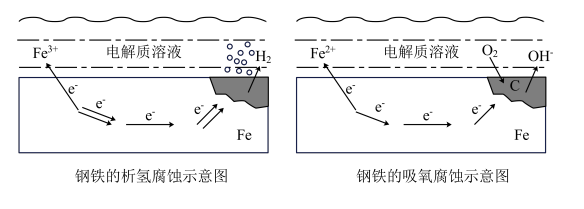
①钢铁的吸氧腐蚀:
通常情况下,在潮湿的空气中,钢铁表面凝结了一层溶有氧气的水膜,将会发生___________ 腐蚀。
负极反应式:_________ ;正极反应式:________ 。
总反应式:___________ 。
Fe(OH)2被进一步氧化成Fe(OH)3:___________ ,Fe(OH)3部分脱水生成Fe2O3·nH2O,是铁锈的主要成分。
②钢铁的析氢腐蚀:
当钢铁表面的电解质溶液_______ 较强时,腐蚀过程中有________ 放出。其中,Fe是_________ 极,C是__________ 极。
负极反应式:___________ ;正极反应式:__________ 。
总反应式:___________ 。
随着了氢气的析出,溶液的pH上升,最终形成铁锈。
(1)实验探究——钢铁的电化学腐蚀原理

①向铁粉中加入碳粉的目的是
②实验现象:a装置右边的小试管中液面
(2)钢铁的电化学腐蚀
根据钢铁表面水溶液薄膜的酸碱性不同,钢铁的电化学腐蚀分为析氢腐蚀和吸氧腐蚀,如下图所示:

①钢铁的吸氧腐蚀:
通常情况下,在潮湿的空气中,钢铁表面凝结了一层溶有氧气的水膜,将会发生
负极反应式:
总反应式:
Fe(OH)2被进一步氧化成Fe(OH)3:
②钢铁的析氢腐蚀:
当钢铁表面的电解质溶液
负极反应式:
总反应式:
随着了氢气的析出,溶液的pH上升,最终形成铁锈。
您最近一年使用:0次
2023高二上·全国·专题练习
解题方法
10 . 实验探究:电化学腐蚀
| 实验操作 | 实验现象 | 实验解释 |
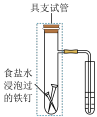 | 导管中 | 装置中铁、碳和饱和食盐水构成原电池,铁钉发生 |
 | ①试管中产生气泡的速率 | Zn与CuSO4反应生成Cu,Zn、Cu和稀盐酸构成 |
您最近一年使用:0次



