名校
1 . (1)某课外活动小组同学用如图装置进行实验,试回答下列问题:
①若开始时开关K与a连接,则铁发生电化学腐蚀中的________ 腐蚀。
②若开始时开关K与b连接,则总反应的离子方程式为____________________________ 。
(2)芒硝化学式为Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念。
①该电解槽的阳极反应式为______________________________________ 。
此时通过阴离子交换膜的离子数________ (填“大于”、“小于”或“等于”)通过阳离子交换膜的离子数
②制得的氢氧化钠溶液从出口(填写“A”、“B”、“C”或“D”)________ 导出。

③通电开始后,阴极附近溶液pH会增大,请简述原因:____________________________ 。
④若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为______________________________________________________________________________ 。
①若开始时开关K与a连接,则铁发生电化学腐蚀中的
②若开始时开关K与b连接,则总反应的离子方程式为
(2)芒硝化学式为Na2SO4·10H2O,无色晶体,易溶于水,是一种分布很广泛的硫酸盐矿物。该小组同学设想,如果模拟工业上离子交换膜法制烧碱的方法,用如图所示装置电解硫酸钠溶液来制取氢气、氧气、硫酸和氢氧化钠,无论从节省能源还是从提高原料的利用率而言都更加符合绿色化学理念。
①该电解槽的阳极反应式为
此时通过阴离子交换膜的离子数
②制得的氢氧化钠溶液从出口(填写“A”、“B”、“C”或“D”)

③通电开始后,阴极附近溶液pH会增大,请简述原因:
④若将制得的氢气、氧气和氢氧化钠溶液组合为氢氧燃料电池,则电池负极的电极反应式为
您最近一年使用:0次
2018-10-28更新
|
193次组卷
|
4卷引用:福建省连城县第一中学2021-2022学年高二上学期第一次月考化学试题
名校
2 . 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀________________ 。

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①A电极对应的金属是________ (写元素名称),
B电极的电极反应式是___________________________________ 。
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为________ mol。
③镀层破损后,不易被腐蚀的是___________ (填A或B)。
A.镀铜铁 B.镀锌铁 C. 镀锡铁
(1)下列哪个装置可防止铁棒被腐蚀

(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:

①A电极对应的金属是
B电极的电极反应式是
②若电镀前A、B两金属片质量相同,电镀完成后将它们取出洗净、烘干、称量,二者质量差为5.12 g,则电镀时电路中通过的电子为
③镀层破损后,不易被腐蚀的是
A.镀铜铁 B.镀锌铁 C. 镀锡铁
您最近一年使用:0次
2018-10-19更新
|
328次组卷
|
2卷引用:【全国百强校】福建省上杭县第一中学2018-2019学年高二上学期10月月考化学试题
名校
3 . 某蓄电池的反应为NiO2+Fe+2H2O Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2
(1)该蓄电池充电时,发生还原反应的物质是________ (填选项字母)。放电时生成Fe(OH)2的质量为18g,则外电路中转移的电子数是________________ 。
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常在船体上镶嵌Zn块,或与该蓄电池的________ (填“正”或“负”)极相连。
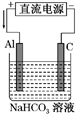
(3)以该蓄电池作电源,用如图所示的装置进行电解,一段时间后发现溶液逐渐变浑浊,Al电极附近有气泡生成,写出此过程中阳极的电极反应式______________________ 。
 Fe(OH)2+Ni(OH)2
Fe(OH)2+Ni(OH)2 (1)该蓄电池充电时,发生还原反应的物质是
A.NiO2 B.Fe C.Fe(OH)2 D.Ni(OH)2
(2)为防止远洋轮船的钢铁船体在海水中发生电化学腐蚀,通常在船体上镶嵌Zn块,或与该蓄电池的
(3)以该蓄电池作电源,用如图所示的装置进行电解,一段时间后发现溶液逐渐变浑浊,Al电极附近有气泡生成,写出此过程中阳极的电极反应式

您最近一年使用:0次
名校
4 . 简要回答下列问题。
(1)铝制器具不宜存放酸、碱溶液的原因是_____________________________ 。
(2)钢铁腐蚀给生活生产带来很多不便,并造成巨大的经济损失。请你提出一种防止钢铁腐蚀的合理措施:______________________________________________ 。
(3)工业燃煤常进行脱硫处理,其目的是________________________________________ ;
(1)铝制器具不宜存放酸、碱溶液的原因是
(2)钢铁腐蚀给生活生产带来很多不便,并造成巨大的经济损失。请你提出一种防止钢铁腐蚀的合理措施:
(3)工业燃煤常进行脱硫处理,其目的是
您最近一年使用:0次
名校
5 . 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢材占世界钢铁年产量的四分之一。
I.如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于_________ 腐蚀。

(1)红墨水柱两边的液面变为左低右高,则______ (填“a”或“b”)边盛有食盐水。
(2) b试管中铁发生的是______ 腐蚀,生铁中碳上发生的电极反应式___________ 。
II.下面两个图都是金属防护的例子。
(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用_____ (从下面选项中选择),此方法叫做______________ 保护法。
A.铜 B.钠 C.锌 D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的_____ 极。
(5)采取以上两种方法,_____ (填“甲”或“乙”)种能使铁闸门保护得更好。
I.如图装置中,U形管内为红墨水,a、b试管内分别盛有氯化铵(显酸性)溶液和食盐水,各加入生铁块,放置一段时间均被腐蚀,这两种腐蚀都属于

(1)红墨水柱两边的液面变为左低右高,则
(2) b试管中铁发生的是
II.下面两个图都是金属防护的例子。

(3)为了降低某水库的铁闸门被腐蚀的速率,可以采用图甲所示的方案,其中焊接在铁闸门上的固体材料R可以采用
A.铜 B.钠 C.锌 D.石墨
(4)图乙方案也可以降低铁闸门腐蚀的速率,其中铁闸门应该连接在直流电源的
(5)采取以上两种方法,
您最近一年使用:0次
名校
6 . 钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。
请回答钢铁在腐蚀、防护过程中的有关问题。
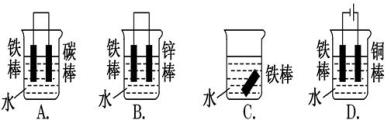
(1)下列哪些装置不能防止铁棒被腐蚀________________ ;
(2)实际生产可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答:
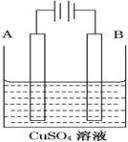
①B电极对应的金属是________ (写元素名称),
A电极的电极反应式是___________________ 。
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因_____________________ 。
请回答钢铁在腐蚀、防护过程中的有关问题。

(1)下列哪些装置不能防止铁棒被腐蚀
(2)实际生产可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答:

①B电极对应的金属是
A电极的电极反应式是
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
您最近一年使用:0次
2016-12-09更新
|
199次组卷
|
2卷引用:福建省晋江市南侨中学2019-2020学年高二上学期第一阶段考试化学试题
7 . 在实际生产中,可在铁件的表面镀铜防止铁被腐蚀.装置示意图如图.请回答:
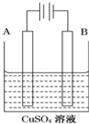
①B电极的电极反应式是_____ .
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因_____ .

①B电极的电极反应式是
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因
您最近一年使用:0次
8 . 钢铁容易生锈的主要原因是因为钢铁在炼制过程中混有少量的碳杂质,在潮湿的空气中容易形成原电池,发生电化学腐蚀.金属发生电化学腐蚀时,可分为析氢腐蚀和吸氧腐蚀.两者的本质相同,该腐蚀过程中负极电极反应式为_____ ,但正极反应不同,析氢腐蚀的正极反应为_____ ,钢铁腐蚀主要是吸氧腐蚀,吸氧腐蚀的正极反应为_____ .
您最近一年使用:0次
名校
9 . 钢铁是目前应用最广泛的金属材料,了解钢铁腐蚀的原因与防护方法具有重要意义,对钢铁制品进行抗腐蚀处理,可适当延长其使用寿命。

(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为_________ 。
(2)利用如图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于________ 处。
②若X为锌,开关K置于M处,该电化学防护法称为_______ 。
(3)图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2 g时,X电极溶解的铜的质量________ 3.2 g(填“<”“>”或“=”)。
(4)图中若X为铜,容器中海水替换为FeCl3溶液,开关K置于M处,铜电极发生的反应是______________ ,若将开关K置于N处,发生的总反应是___________ 。

(1)抗腐蚀处理前,生产中常用盐酸来除铁锈。现将一表面生锈的铁件放入盐酸中,当铁锈除尽后,溶液中发生的化合反应的化学方程式为
(2)利用如图装置,可以模拟铁的电化学防护。
①若X为碳棒,为减缓铁件的腐蚀,开关K应置于
②若X为锌,开关K置于M处,该电化学防护法称为
(3)图中若X为粗铜,容器中海水替换为硫酸铜溶液,开关K置于N处,一段时间后,当铁件质量增加3.2 g时,X电极溶解的铜的质量
(4)图中若X为铜,容器中海水替换为FeCl3溶液,开关K置于M处,铜电极发生的反应是
您最近一年使用:0次
2016-12-09更新
|
376次组卷
|
7卷引用:福建省南安第一中学2017-2018学年高二上学期期中考试化学试题
10 . 炒过菜的铁锅未及时洗净,不久便会因腐蚀而出现红褐色锈斑。请回答:
(1)铁锅的锈蚀是_______ 腐蚀(填“析氢"或“吸氧”)
(2)写出铁锅腐蚀时负极的电极反应式:_______
(3)写出铁锅在中性条件下正极的电极反应式_______ 。
(4)写出电化学反应的总方程式_______
(1)铁锅的锈蚀是
(2)写出铁锅腐蚀时负极的电极反应式:
(3)写出铁锅在中性条件下正极的电极反应式
(4)写出电化学反应的总方程式
您最近一年使用:0次



